A kutatók új módot fedeztek fel a rákos sejtek elhalására a kemoterápia során
Utolsó ellenőrzés: 14.06.2024

Minden iLive-tartalmat orvosi szempontból felülvizsgáltak vagy tényszerűen ellenőriznek, hogy a lehető legtöbb tényszerű pontosságot biztosítsák.
Szigorú beszerzési iránymutatásunk van, és csak a jó hírű média oldalakhoz, az akadémiai kutatóintézetekhez és, ha lehetséges, orvosilag felülvizsgált tanulmányokhoz kapcsolódik. Ne feledje, hogy a zárójelben ([1], [2] stb.) Szereplő számok ezekre a tanulmányokra kattintható linkek.
Ha úgy érzi, hogy a tartalom bármely pontatlan, elavult vagy más módon megkérdőjelezhető, jelölje ki, és nyomja meg a Ctrl + Enter billentyűt.
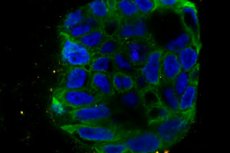
A kemoterápia elpusztítja a rákos sejteket. De az a mód, ahogy ezek a sejtek elpusztulnak, eltér a korábbi felfogástól. A Holland Rákkutató Intézet kutatói, Thein Brummelkamp vezetésével a rákos sejtpusztulás egy teljesen új módját fedezték fel: a Schlafen11 gén miatt.
"Ez egy nagyon váratlan felfedezés. A rákos betegeket közel egy évszázada kezelték kemoterápiával, de ezt a sejthalálhoz vezető utat még soha nem figyelték meg. Ahol és azt, hogy ez mikor fordul elő betegeknél, tovább kell vizsgálni. Eredményeiket a Science-ben.
publikáltákSok rákkezelés károsítja a sejtek DNS-ét. Túl sok visszafordíthatatlan károsodás után a sejtek elindíthatják saját halálukat. Az iskolabiológia azt tanítja nekünk, hogy a p53 fehérje irányítja ezt a folyamatot. A p53 közvetíti a sérült DNS helyreállítását, de sejtöngyilkosságot kezdeményez, ha a károsodás túl súlyossá válik. Ez megakadályozza az ellenőrizetlen sejtosztódást és a rák kialakulását.
Meglepetés: megválaszolatlan kérdés
Ez megbízható rendszernek tűnik, de a valóság ennél összetettebb. "A daganatok több mint felében a p53 már nem működik" - mondja Brummelkamp. "A p53 fő szereplője nem játszik ott semmilyen szerepet. Miért halnak el tehát a rákos sejtek p53 nélkül, ha kemoterápiával vagy sugárzással károsítják a DNS-üket? Meglepetésemre ez megválaszolatlan kérdésnek bizonyult."
Kutatócsoportja ezután Revuen Agami kollégájával együtt felfedezte azt a korábban ismeretlen módot, ahogyan a sejtek elpusztulnak DNS-károsodás után. A laboratóriumban kemoterápiát fecskendeztek a sejtekbe, amelyekben gondosan módosították a DNS-t. Brummelkamp azt mondja: "Olyan genetikai változást kerestünk, amely lehetővé teszi a sejtek túlélését a kemoterápiában. Csoportunknak nagy tapasztalata van a gének szelektív kikapcsolása terén, amit itt teljes mértékben alkalmazhatunk."
Új főszereplő a sejthalálban A gének kiiktatásával a kutatócsoport felfedezte a sejthalálhoz vezető új utat a Schlafen11 (SLFN11) gén által. Nicholas Boon vezető kutató a következőket mondta: "Amikor a DNS megsérül, az SLFN11 kikapcsolja a sejtek fehérjegyárait: a riboszómákat. Ez óriási stresszt okoz ezekben a sejtekben, ami halálukhoz vezet. Az általunk felfedezett új útvonal teljesen megkerüli a p53-at."
Az SLFN11 gén nem újdonság a rákkutatásban. Brummelkamp szerint gyakran inaktív az olyan betegek daganataiban, akik nem reagálnak a kemoterápiára. "Most meg tudjuk magyarázni ezt az összefüggést. Ha a sejtekből hiányzik az SLFN11, nem pusztulnak el ilyen módon válaszul a DNS-károsodásra. A sejtek túlélnek, és a rák folytatódik."
A rákkezelésre gyakorolt hatás
"Ez a felfedezés sok új kutatási kérdést nyit meg, ami általában az alapkutatásban így van" - mondja Brummelkamp.
"Felfedezésünket laboratóriumban növesztett rákos sejtekben mutattuk be, de sok fontos kérdés továbbra is fennáll: Hol és mikor fordul elő ez az út a betegeknél? Hogyan hat ez az immunterápiára vagy a kemoterápiára? Befolyásolja-e a rákkezelés mellékhatásait? Ha a sejthalálnak ez a formája a betegek számára is jelentős lesz, ez a felfedezés hatással lesz a rák kezelésére. Ezek fontos kérdések a további tanulmányozáshoz."
A gének kikapcsolása, egyenként Az embereknek több ezer génje van, amelyek közül sok olyan funkcióval rendelkezik, amelyet nem értünk. Génjeink szerepének meghatározására Brummelkamp kutató egy haploid sejteket használó módszert dolgozott ki. Ezek a sejtek minden génből csak egy példányt tartalmaznak, ellentétben a testünkben lévő normál sejtekkel, amelyek két kópiát tartalmaznak. Két másolat kezelése nehéz lehet genetikai kísérletekben, mert gyakran csak az egyikben fordulnak elő változások (mutációk). Ez megnehezíti ezeknek a mutációknak a hatásainak megfigyelését.
Más kutatókkal együtt Brummelkamp sok évet töltött azzal, hogy ezzel a sokoldalú módszerrel feltárja a betegségek szempontjából kritikus folyamatokat. Csoportja például nemrég fedezte fel, hogy a sejtek a korábban ismerttől eltérő módon is képesek lipideket termelni.
Felfedezték, hogy bizonyos vírusok, köztük a halálos Ebola-vírus hogyan jutnak be az emberi sejtekbe. Belemerültek a rákos sejtek bizonyos terápiákkal szembeni rezisztenciájába, és azonosítottak olyan fehérjéket, amelyek fékezőként hatnak az immunrendszerre, ami hatással van a rák immunterápiájára.
Az elmúlt években csapata két olyan enzimet fedezett fel, amelyek négy évtizedig ismeretlenek maradtak, és amelyekről kiderült, hogy létfontosságúak az izomműködéshez és az agy fejlődéséhez.
