A cikk orvosi szakértője
Új kiadványok
Osteoarthritis: A meniszektómia hatása az ízületi porcra
Utolsó ellenőrzés: 04.07.2025

Minden iLive-tartalmat orvosi szempontból felülvizsgáltak vagy tényszerűen ellenőriznek, hogy a lehető legtöbb tényszerű pontosságot biztosítsák.
Szigorú beszerzési iránymutatásunk van, és csak a jó hírű média oldalakhoz, az akadémiai kutatóintézetekhez és, ha lehetséges, orvosilag felülvizsgált tanulmányokhoz kapcsolódik. Ne feledje, hogy a zárójelben ([1], [2] stb.) Szereplő számok ezekre a tanulmányokra kattintható linkek.
Ha úgy érzi, hogy a tartalom bármely pontatlan, elavult vagy más módon megkérdőjelezhető, jelölje ki, és nyomja meg a Ctrl + Enter billentyűt.
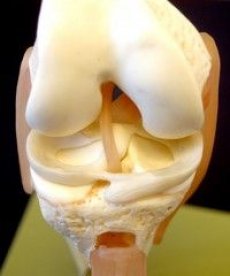
Amint azt korábban említettük, az ízületi meniscusok fontos szerepet játszanak a normális ízületi működésben. A meniscusok olyan struktúrák, amelyek növelik a combcsont és a sípcsont ízületi felszíneinek egybeesését, fokozzák az oldalirányú stabilitást, és javítják az ízületi folyadék eloszlását és a tápanyagok cseréjét az ízületi porccal. A teljes vagy részleges meniscectomia a sípcsont ízületi felszínére nehezedő terhelés irányának megváltozásához vezet, ami az ízületi porc degenerációjához vezet.
Számos tanulmány foglalkozott a meniscectomia ízület biomechanikájára gyakorolt hatásának, valamint az ízületi porcban és a porc alatti csontban kiváltott degeneratív folyamatoknak az állatokban (általában kutyákban és juhokban). Kezdetben a kutatók a térdízület mediális meniszkuszának ektómiáját végezték, de később kiderült, hogy a laterális meniszkusz ektómiája az osteoarthritis gyorsabb kialakulásához vezet.
Little és munkatársai (1997) juhok laterális meniscectomiája során vizsgálták az ízületi porc és a porc alatti csont változásait a térdízület több területén. A műtét után 6 hónappal az ízületi porcban kiváltott változásokat illusztráló tipikus szövettani leletek a porc rojtosodása, a proteoglikán-koncentráció csökkenése és a porcsejtek számának csökkenése voltak. A porc alatti csontban a megváltozott porcterületek alatt kapilláris növekedést figyeltek meg a meszes porczónába, a "hullámos határ" kifelé történő elmozdulását és a porc alatti csont szivacsos anyagának megvastagodását.
P. Ghosh és munkatársai (1998) tanulmányában kimutatták, hogy juhoknál a laterális meniscectomia után 9 hónappal a porc alatti csontátépülés jelei figyelhetők meg, és az ízületi porc degenerációja következtében megnő az ásványi sűrűsége. Az oldalsó meniszkusz eltávolítása miatt rendellenesen nagy mechanikai terhelésnek kitett területeken (a combcsont laterális condylusa és a sípcsont laterális lemeze) a dermatán-szulfátot tartalmazó proteoglikánok fokozott szintézise volt megfigyelhető, bár az azonos típusú proteoglikánok fokozott szintézise a mediális lemez porcában is megfigyelhető volt. Kiderült, hogy a dermatán-szulfátot tartalmazó proteoglikánokat főként a dekorin képviseli. Legmagasabb koncentrációját az ízületi porc középső és mély zónáiban találták.
A laterális meniszkusz eltávolítása miatt a nagy terhelésnek kitett porcterületeken a dermatán-szulfátot tartalmazó proteoglikánok szintézisének fokozódásával együtt az aggrekán fokozott katabolizmusát is kimutatták, amit a fragmensek porc explantátumokból a táptalajba történő felszabadulása, valamint az MMP és az aggrekanázok magas aktivitása is bizonyít. Mivel az oszteoartrózis ezen modelljében a gyulladásos aktivitás minimális volt, a szerzők azt feltételezték, hogy az enzimek forrása a porcsejtek.
Bár sok megválaszolatlan kérdés maradt, a fent leírt tanulmányok feltárják a biomechanikai tényezők lehetséges szerepét az osteoarthritis patogenezisében. Egyértelmű, hogy a porcsejtek képesek „érzékelni” környezetük mechanikai tulajdonságait, és a változásokra úgy reagálva, hogy nagyobb terhelést elbíró ECM-et (extracelluláris mátrixot) szintetizálnak, így megelőzve a porckárosodást. Fiatal állatokban a mérsékelt testmozgás aggrekánban gazdag ECM szintézisét indukálta. A porcsejtek válaszának ez a hipertrófiás (vagy adaptív) fázisa több évig is eltarthat, stabil mechanikai terhelést biztosítva az ízületi porc számára. Azonban, ha ez az egyensúly felborul a terhelés intenzitásának vagy időtartamának növekedése, vagy a normál ízületi biomechanika megváltozása sérülés vagy műtét után, vagy a porcsejtek ECM-szintézis fokozására való képességének csökkenése miatt a megnövekedett terhelésre (öregedés során) válaszul, az endokrin faktorok hatása jelentős változásokat von maga után a sejtek és a mátrix szintjén: a proteoglikánok és a II. típusú kollagén szintézise gátlódik, és a dekorin, valamint az I., III. és X. típusú kollagén szintézise stimulálódik. A bioszintézis változásával egyidejűleg fokozódik az ECM katabolizmusa, valamint az MMP-k és az aggrekanázok szintje. Nem ismert, hogy a mechanikai terhelés hogyan segíti elő a környező ECM (magas-középmag-szövet) felszívódását a porcsejtek által; ezt a folyamatot valószínűleg prosztanoidok, citokinek (például IL-1p vagy TNF-α) és szabad oxigéngyökök közvetítik. Itt kell megemlíteni a szinovitisz szerepét az osteoarthritisben, mivel a fent említett katabolizmus mediátorok legvalószínűbb forrása a makrofágszerű szinovociták és a leukociták lehetnek, amelyek az ízület szinoviális membránjába infiltrálódnak.
OD Chrisman és munkatársai (1981) tanulmánya kimutatta, hogy a traumás ízületi sérülés stimulálja a prosztaglandin prekurzor, az arachidonsav termelődését. A sérült porcsejtek membránjait tekintik az arachidonsav forrásának. Közismert, hogy az arachidonsavat a ciklooxigenáz (COX) enzim gyorsan prosztaglandinokká alakítja. Kimutatták, hogy a prosztaglandinok, különösen a PGE2 , kölcsönhatásba lépnek a porcsejtek receptoraival, megváltoztatva génjeik expresszióját. Az azonban továbbra sem világos, hogy az arachidonsav stimulálja vagy gátolja-e a proteinázok és aggrekanázok termelődését. Korábbi tanulmányok kimutatták, hogy a PGE2 fokozza az MMP-termelést és az ízületi porc lebomlását okozza. Más tanulmányok eredményei szerint a PGE2 anabolikus hatással van az ECM-re, és elősegíti az ECM integritását, gátolva a porcsejtek citokintermelését. Lehetséges, hogy e tanulmányok ellentmondásos eredményei a bennük alkalmazott PGE2 eltérő koncentrációinak tudhatók be.
Az ízületi porc károsodására válaszul kis mennyiségű IL-1β (a fő citokin, amely serkenti az MMP-k szintézisét és felszabadulását, valamint gátolja természetes inhibitoraik aktivitását) képződhet, ami további szöveti degradációhoz vezet.
Így az ebben a szakaszban ismertetett vizsgálatok kimutatták, hogy az ízületre nehezedő, küszöb alatti dinamikus terhelés fenntartása az új mechanikai körülményeket elviselni képes porcsejtek proliferációját okozza, ami az oszteoartrózis hipertrófiás stádiumának kezdetét jelenti. A hipertrófiás porcsejtek a differenciálódás utolsó szakaszában lévő sejtek, ami azt jelenti, hogy a fő mátrixelemek génjeinek expressziója megváltozik bennük. Ennek következtében az aggrekán proteoglikánok és a II. típusú kollagén szintézise gátlódik, és a dekorin, az I., III. és X. típusú kollagének szintézise fokozódik.
Az aggrekán és a II-es típusú kollagén tartalmának csökkenése az ECM-ben, ami a szintézis és a lebontás folyamatai közötti egyensúlyhiánnyal jár, az ízületi porcnak azt a tulajdonságát adja, hogy nem reagál megfelelően a mechanikai stresszre. Ennek eredményeként a porcsejtek védtelenné válnak, a folyamat a harmadik, katabolikus szakaszba lép, amelyet túlzott proteolitikus aktivitás és autokrin és parakrin szabályozó faktorok szekréciója jellemez. Morfológiailag ezt a szakaszt az ízületi porc ECM-jének pusztulása jellemzi; klinikailag ez manifeszt oszteoarthrosisnak felel meg. Ez a hipotézis természetesen az oszteoarthrosisban lejátszódó összes komplex folyamat leegyszerűsített képét képviseli, de általánosítja az oszteoarthrosis patobiológiájának modern koncepcióját.
 [ 1 ], [ 2 ], [ 3 ], [ 4 ], [ 5 ], [ 6 ], [ 7 ], [ 8 ], [ 9 ], [ 10 ], [ 11 ], [ 12 ]
[ 1 ], [ 2 ], [ 3 ], [ 4 ], [ 5 ], [ 6 ], [ 7 ], [ 8 ], [ 9 ], [ 10 ], [ 11 ], [ 12 ]

