A cikk orvosi szakértője
Új kiadványok
Szokásos vetélés - okok
Utolsó ellenőrzés: 04.07.2025

Minden iLive-tartalmat orvosi szempontból felülvizsgáltak vagy tényszerűen ellenőriznek, hogy a lehető legtöbb tényszerű pontosságot biztosítsák.
Szigorú beszerzési iránymutatásunk van, és csak a jó hírű média oldalakhoz, az akadémiai kutatóintézetekhez és, ha lehetséges, orvosilag felülvizsgált tanulmányokhoz kapcsolódik. Ne feledje, hogy a zárójelben ([1], [2] stb.) Szereplő számok ezekre a tanulmányokra kattintható linkek.
Ha úgy érzi, hogy a tartalom bármely pontatlan, elavult vagy más módon megkérdőjelezhető, jelölje ki, és nyomja meg a Ctrl + Enter billentyűt.
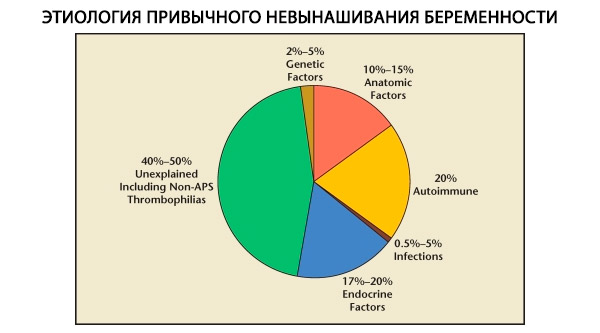
A habituális vetélések struktúrájában genetikai, anatómiai, endokrin, immunológiai és fertőző tényezőket különböztetünk meg. Ha a fenti okok mindegyikét kizárjuk, akkor marad egy olyan betegcsoport, akiknél a habituális vetélés eredete nem tisztázott (idiopátiás vetélések). C. Coulam és munkatársai (1996) szerint az idiopátiás vetélések 80%-a fel nem ismert immunrendszeri rendellenességeken alapul.
Nincs meggyőző bizonyíték arra, hogy az endometriózis ismételt vetélést okozna, vagy hogy az endometriózis gyógyszeres vagy sebészeti kezelése csökkentené az ismételt vetélések előfordulását.
A jelenlegi elképzelések szerint a genetikai és részben fertőző okok mellett, amelyek abnormális embrió kialakulásához vezetnek, más tényezők (anatómiai, endokrin, immunológiai) káros hatásának megvalósítása abban áll, hogy kedvezőtlen hátteret teremtenek a genetikailag teljes megtermékenyített petesejt fejlődéséhez, ami a chorion tartalékkapacitásának kimerüléséhez és a fejlődés (embriogenezis) leállásához vezet. A terhesség első trimeszterében a kritikus időszakokat 6-8 hétnek (az embrió halála) és 10-12 hétnek (a megtermékenyített petesejt kilökődése) tekintik.
 [ 1 ]
[ 1 ]
A rendszeres vetélés genetikai okai
A genetikai tényezők a szokásos vetélés okainak 3–6%-át teszik ki. Az első trimeszterben bekövetkező szórványos terhességmegszakítások esetén az abortuszok körülbelül 50%-ában kromoszóma-rendellenességek fordulnak elő. Ezek többsége (95%) a kromoszómák számának változása - monoszómia (egy kromoszóma elvesztése), triszómia (egy további kromoszóma jelenléte), amelyek a meiózis hibáinak eredményei, valamint poliploidia (a kromoszóma-összetétel növekedése egy teljes haploid készlettel), amely akkor fordul elő, amikor egy petesejtet két vagy több spermium megtermékenyít. Sporadikus vetélések esetén a triszómia fordul elő leggyakrabban - az összes mutáció 60%-a (leggyakrabban a 16. kromoszómán, valamint a 13., 18., 21., 22. kromoszómán), a második helyen a Shereshevsky-Turner szindróma (45 X0 kromoszóma) áll - 20%, a fennmaradó 15%-ot a poliploidia (különösen a triploidia) okozza.
Abortusz során bekövetkező kromoszómaszám-változás esetén a szülők kariotípusának vizsgálata leggyakrabban nem mutat ki semmilyen patológiát, és a magzat kromoszómabetegségének valószínűsége a későbbi terhesség során 1%. Ezzel szemben a habituális vetélést mutató párok abortuszainak vizsgálatakor az esetek 3-6%-ában figyelhetők meg a kromoszómák szerkezeti változásai (intra- és interkromoszómális). A szülők kariotípusának vizsgálatakor az esetek 7%-ában kiegyensúlyozott kromoszóma-átrendeződéseket találnak. Leggyakrabban ezek reciprok transzlokációk, amelyekben az egyik kromoszóma egy szegmense egy nem homológ kromoszóma egy másik szegmensének helyén helyezkedik el, valamint a nemi kromoszómák mozaikossága, inverziója és a kromoszómák gyűrű formájában történő kimutatása. Az egyik házastárs ilyen átrendeződéseinek jelenléte esetén a meiózis során a kromoszómák párosodási és szétválási folyamatai gátoltak, ami a ivarsejtekben a kromoszóma-szakaszok elvesztéséhez (deléciójához) vagy megduplikálódásához (duplikációjához) vezet. Ez úgynevezett kiegyensúlyozatlan kromoszóma-átrendeződésekhez vezet, amelyek során az embrió vagy életképtelen, vagy súlyos kromoszóma-patológia hordozója. Az egyik szülő kariotípusában kiegyensúlyozott kromoszóma-átrendeződések jelenlétében 1–15% annak a valószínűsége, hogy a gyermek kiegyensúlyozatlan kromoszóma-rendellenességekkel születik. Az adatok közötti különbségek összefüggenek az átrendeződések jellegével, az érintett szegmensek méretével, a hordozó nemével és a családi kórtörténettel.
Diagnosztika
Anamnézis
- Örökletes betegségek a családtagoknál.
- Veleszületett rendellenességek jelenléte a családban.
- Értelmi fogyatékossággal élő gyermekek születése.
- Ismeretlen eredetű meddőség és/vagy vetélés jelenléte házaspárnál vagy rokonoknál.
- A perinatális halálozás tisztázatlan eseteinek jelenléte.
Speciális kutatási módszerek
- A szülők kariotípusának vizsgálata különösen ajánlott házaspárok számára olyan újszülöttek születésekor, akiknél a vetélés mellett fejlődési rendellenességek is előfordultak, valamint a terhesség korai szakaszában bekövetkezett habituális vetélés esetén.
- Az abortusz citogenetikai elemzése halvaszületés vagy újszülöttkori halálozás esetén.
Javallatok más szakemberekkel való konzultációra
Ha a szülőknél kariotípus-változásokat észlelnek, genetikussal kell konzultálni, hogy felmérjék a patológiás gyermek születésének kockázatát, vagy ha szükséges, döntsenek a petesejt vagy sperma adományozásának kérdéséről.
A beteg további ellátása
Ha egy házaspárnak kóros kariotípusa van, még az egyik szülőnél is, terhesség alatt ajánlott prenatális diagnosztikát végezni - koriongybopsziát vagy amniocentézist - a magzati fejlődési rendellenességek magas kockázata miatt.
A rendszeres vetélés anatómiai okai
A rendszeres vetélés anatómiai okai a következők:
- veleszületett rendellenességek a méh fejlődésében (a méh teljes megkettőződése; kétszarvú, nyereg alakú, egyszarvú méh; részleges vagy teljes méhen belüli sövény);
- szerzett anatómiai rendellenességek;
- méhen belüli összenövések (Asherman-szindróma);
- szubmukózus méhmiómák;
- isthmiás-méhnyaki elégtelenség.
Az anatómiai rendellenességek gyakorisága a habituális vetélésben szenvedő betegeknél 10 és 16% között mozog. Az olyan méhfejlődési rendellenességek előfordulási gyakorisága, amelyek vetélést (de nem meddőséget) okozhatnak, az összes méhfejlődési rendellenességhez viszonyítva a következő: kétszarvú méh - 37%, nyereg alakú méh - 15%, méhen belüli sövény - 22%, a méh teljes megkettőződése - 11%, egyszarvú méh - 4,4%.
A szokásos vetélés diagnózisa
Anamnézis
A méh anatómiai patológiája esetén gyakrabban figyelhető meg a terhesség késői befejeződése és a koraszülés, azonban a méhen belüli septumba vagy a myomatózus csomó közelébe történő beültetéssel a terhesség korai befejezése is lehetséges.
Isthmiás-méhnyaki elégtelenség esetén a patognomonikus jel a terhesség spontán megszűnése a második trimeszterben vagy korai koraszülés, amely viszonylag gyorsan és kevés fájdalommal jár.
A méh rendellenességei esetén figyelmet kell fordítani a húgyúti patológia anamnesztikus jeleire (gyakran a méh veleszületett rendellenességeivel együtt) és a menstruációs funkció fejlődésének jellegére (a méh működőképes kezdetleges szarvával járó hematometra jelei).
Speciális vizsgálati módszerek
- Jelenleg a diagnózis felállításához hiszteroszalpingográfiát végeznek, amely lehetővé teszi a méhüreg alakjának tanulmányozását, a submucosus miómák, összenövések, szeptumok jelenlétének azonosítását, valamint a petevezetékek áteresztőképességének meghatározását. A méh patológiájának diagnosztizálásához a hiszteroszalpingográfiát a menstruáció és az ovuláció közötti időszakban célszerű elvégezni, azaz a menstruációs ciklus első fázisában, a vérzés megszűnése után (a ciklus 7-9. napja). Az isthma-méhnyak elégtelenség diagnosztizálásához a vizsgálatot a menstruációs ciklus második fázisában (18-20. nap) végzik a méhnyak belső nyílásának állapotának meghatározása érdekében. A hiszteroszalpingográfia elvégzése előtt ki kell zárni a kismedencei szervek gyulladásos betegségeit, vagy kezelni kell azokat.
- A hiszteroszkópia az utóbbi években elterjedt, és az intrauterin patológia diagnosztizálásának arany standardjává vált. A hiszteroszalpingográfiához képest magasabb költségei miatt azonban a módszert olyan nőknél alkalmazzák, akiknél az előzetes ultrahangadatok alapján intrauterin patológia gyanúja merül fel. A hiszteroszkópia segítségével megvizsgálható a méh ürege, meghatározható a méhen belüli patológia jellege, és ha a szükséges felszerelés (reszektoszkóp) rendelkezésre áll, minimálisan invazív sebészeti beavatkozás végezhető - összenövések, szubmukózus mióma csomók és endometrium polipok eltávolítása. Intrauterin septum eltávolításakor előnyben részesítik a laparoszkópos kontrollal végzett hiszteroreszektoszkópiát, amely megakadályozza a méhfal perforációjának lehetőségét.
- Az ultrahangvizsgálatot a menstruációs ciklus első fázisában végzik, amely lehetővé teszi a szubmukózus méhmióma és a méhen belüli összenövések feltételezett diagnózisát, a ciklus második fázisában pedig a méhen belüli sövény és a kétszarvú méh azonosítását. Ez a módszer különösen fontos a terhesség korai szakaszában, amikor az érzékenysége ezen állapotok diagnosztizálásában 100%, specificitása pedig 80%. Terhességen kívül a diagnózis további megerősítést igényel más módszerekkel.
- Külföldi szerzők rámutatnak a szonohiszterográfia (transzvaginális érzékelővel végzett ultrahangvizsgálat, amelyhez előzetesen 0,9%-os nátrium-klorid-oldatot juttatnak a méh üregébe) előnyére a hiszteroszalpingográfiával szemben, mivel lehetővé teszi a méhen belüli sövény és a kétszarvú méh közötti differenciáldiagnosztikát. A szonohiszterográfiával nemcsak a méhüreg alakját lehet vizsgálni, hanem a méhtest fundusának konfigurációját is meg lehet határozni. Hazánkban ez a módszer még nem terjedt el széles körben.
- Egyes bonyolult esetekben a medencei szervek MRI-vizsgálatát alkalmazzák a diagnózis megerősítésére. A módszer értékes információk megszerzését teszi lehetővé a méh fejlődési rendellenességei esetén, amelyeket a medence szerveinek atipikus elrendezése kísér. Az MRI fontos kezdetleges méhszarv esetén annak eldöntésére, hogy célszerű-e eltávolítani. A kezdetleges méhszarv eltávolításának szükségessége akkor merül fel, ha az a petevezetékkel és a petefészekkel van összeköttetésben, hogy megakadályozza a megtermékenyített petesejt kialakulását és fejlődését benne. A méh anatómiai rendellenességei esetén a terhességmegszakítás összefüggésben állhat a megtermékenyített petesejt sikertelen beágyozódásával (a méhen belüli sövényen, a submucosus mióma csomó közelében), az endometrium elégtelen vaszkularizációjával és befogadásával, a méhüregben lévő szoros térbeli viszonyokkal (például mióma csomó okozta üregdeformáció esetén), amelyeket gyakran ICI kísér, valamint hormonális zavarokkal.
A szokásos vetélés kezelése
Sebészeti kezelés
Méhen belüli sövény, submucosus mióma nyirokcsomók és összenövések esetén a leghatékonyabb sebészeti kezelés a hiszteroreszektoszkópia. A kezelés utáni későbbi vetélések gyakorisága ebben a nőcsoportban 10%, szemben a műtét előtti 90%-kal. A laparotomiával és a transzcervikális hiszteroreszektoszkópiával végzett metroplasztika eredményeinek összehasonlításakor P. Heinonen (1997) kisebb traumára és a hiszteroreszektoszkópia nagyobb hatékonyságára utaló eredményeket kapott; az életképes gyermek születésével végződő terhességek aránya 68, illetve 86% volt.
A méhen belüli sövény, az összenövések és a submucosus mióma csomók sebészeti eltávolítása az esetek 70–80%-ában megszünteti a vetélést. Azonban hatástalan azoknál a méhfejlődési rendellenességekkel küzdő nőknél, akiknél normális szülések, majd ezt követően ismétlődő vetélések voltak. Valószínű, hogy ilyen esetekben az anatómiai tényező nem a vezető ok, és a vetélés egyéb okait kell keresni.
Bizonyított tény, hogy a hasi metroplasztika jelentős posztoperatív meddőség kockázattal jár, és nem javítja a későbbi terhesség prognózisát. Ezért jobb előnyben részesíteni a hiszteroszkópiát és a laparoszkópos műtéteket.
Gyógyszeres kezelés
Az IUD bevezetésének, a nagy dózisú ösztrogén gyógyszereknek, a Foley-katéter méhüregbe történő bevezetésének hatékonysága összenövések eltávolítására irányuló műtétek, valamint a méhen belüli sövény eltávolítása után még nem bizonyított. A terhességet legkorábban a műtét után 3 hónappal ajánlott megtervezni. Az endometrium növekedésének javítása érdekében 3 menstruációs cikluson keresztül ciklikus hormonterápiát végeznek [14]. A ciklus első 14 napjában 3 hónapig 2 mg 17-béta-ösztradiolt tartalmazó gyógyszer szedése ajánlott, a következő 14 napban pedig 2 mg 17-béta-ösztradiolt és 20 mg didrogeszteront (10 mg didrogeszteron kombinált gyógyszer részeként plusz 10 mg didrogeszteron külön tabletta formájában).
A beteg további ellátása
A terhesség lefolyásának jellemzői kétszarvú méh esetén vagy a méh megduplázódása esetén (ha 2 méhüreg van):
- a terhesség korai szakaszában a vérzés gyakran az "üres" szarvból vagy a méhüregből jelentkezik a kifejezett deciduális reakció miatt; ebben az esetben a taktikának konzervatívnak kell lennie, és görcsoldó és vérzéscsillapító szerek alkalmazásából kell állnia;
- a terhesség különböző szakaszaiban történő megszakításának veszélye;
- iszmikus-méhnyaki elégtelenség kialakulása;
- méhlepényi elégtelenség okozta intrauterin növekedési retardáció.
A terhesség korai szakaszában, vérzés esetén ágynyugalom és félig ágynyugalom ajánlott, valamint vérzéscsillapító, görcsoldó és nyugtató gyógyszerek adása, és gesztagénekkel (napi 20-40 mg-os didrogeszteron dózisban) végzett terápia a terhesség 16-18. hetéig.
A rendszeres vetélés endokrin okai
Különböző szerzők szerint a vetélés endokrin okai 8-20%-ban állnak a háttérben. Ezek közül a legjelentősebbek a sárgatestfázis-hiány (LPD), az LH-hiperszekréció, a pajzsmirigy-diszfunkció és a cukorbetegség.
A súlyos pajzsmirigybetegség vagy a cukorbetegség ismételt vetélésekhez vezethet. Kompenzált cukorbetegség esetén azonban a rendszeres vetélések kockázata nem különbözik az átlagpopulációban tapasztaltaktól.
Ugyanakkor a populációban a pajzsmirigy-alulműködés magas előfordulása miatt szűrésre van szükség a TSH-szint mérésével. A szokásos vetélésben szenvedő betegeknél a sárgatestfázis-elégtelenség az esetek 20–60%-ában, a policisztás petefészkek ultrahangjelei pedig 44–56%-ában fordulnak elő. Az irodalom szerint az egyes hormonális zavarok hatása a szokásos vetélés tünetegyüttesének kialakulására továbbra is vitatott. M. Ogasawara és munkatársai (1997) tanulmányai nem mutattak ki megbízható különbségeket a terhességmegszakítás gyakoriságában LPI-vel és anélkül olyan betegeknél, akiknél két vagy több korábbi vetélés szerepelt az anamnézisben, kizárva az autoimmun, anatómiai és fertőző okokat.
A sárgatest elégtelen működését számos kedvezőtlen tényező okozhatja:
- az FSH és LH szekréciójának zavarai a menstruációs ciklus első fázisában;
- az LH felszabadulásának korai vagy éppen ellenkezőleg, túl késői csúcsa;
- hipoösztrogénizmus a nem megfelelő follikulogenézis következtében. Mindezen állapotok nem korrigálhatók gesztagén gyógyszerekkel végzett helyettesítő terápiával a posztovulációs időszakban. L. Regan és munkatársai által végzett prospektív vizsgálatok kimutatták a vetélések gyakoriságának jelentős növekedését az LH-hiperszekrécióval rendelkező betegeknél a menstruációs ciklus 8. napján a normális vér LH-szinttel rendelkező nőkhöz képest (a vetélések 65%, illetve 12%-a). Az LH idő előtti megemelkedésének káros hatása a második meiotikus osztódás korai újraindulásával és az éretlen petesejt ovulációjával, valamint a theca sejtek általi androgéntermelés indukciójával, valamint az endometrium ingerületfelvételének károsodásával jár a gesztagén-elégtelenség hatása alatt. Azonban a preovulációs LH-szint előzetes csökkentése gonadotropin-felszabadító hormon agonistákkal a későbbi terhesség meghosszabbítását célzó további intézkedések nélkül nem biztosítja a vetélések gyakoriságának várható csökkenését.
Az NLF diagnosztizálásának arany standardja az endometrium biopsziából nyert anyag szövettani vizsgálata a ciklus második fázisában, két menstruációs cikluson keresztül.
Az ovulációs diszfunkció egyéb okainak, például a hiperprolaktinémia, a hipotireózis, az androgének (petefészek vagy mellékvese) funkcionális feleslege diagnózisát megfelelő kezelés előírásával kell kísérni.
Diagnosztika
Anamnézis és fizikális vizsgálat
- Kórtörténet. Figyelembe veendő tényezők: késői menstruáció, szabálytalan menstruációs ciklus (oligomenorrhoea, amenorrhoea, hirtelen súlygyarapodás, súlycsökkenés, meddőség, rendszeres korai vetélések).
- Vizsgálat: testalkat, magasság, testsúly, hirsutizmus, másodlagos nemi jellegek súlyossága, striák jelenléte, emlőmirigyek vizsgálata galaktorrhea szempontjából.
- Funkcionális diagnosztikai tesztek: végbélhőmérséklet mérése 3 menstruációs ciklus alatt.
Speciális kutatási módszerek
- Hormonális vizsgálat:
- a menstruációs ciklus első fázisában (7–8. nap) – FSH, LH, prolaktin, TSH, tesztoszteron, 17-hidroxiprogeszteron (17-OP), DHEAS tartalmának meghatározása;
- a menstruációs ciklus 2. fázisában (21–22 nap) – a progeszterontartalom meghatározása (a progeszteronszint normatív mutatói nagyon változóak, a módszer nem alkalmazható más tényezők figyelembevétele nélkül).
- Ultrahang:
- a menstruációs ciklus első fázisában (5-7. nap) – endometrium patológiájának, policisztás petefészkek diagnosztizálása;
- a menstruációs ciklus második fázisában (20–21 nap) – a méhnyálkahártya vastagságának mérése (normális érték 10–11 mm, korrelál a progeszteron tartalmával).
- Az NLF igazolására endometrium biopsziát végeznek a várható menstruáció előtt 2 nappal (28 napos ciklus esetén a 26. napon). Ezt a módszert olyan esetekben alkalmazzák, amikor a diagnózis nem egyértelmű. Az endometriumban bekövetkező változások vizsgálatára az úgynevezett "beágyazódási ablak" időszakban az ovuláció utáni 6. napon biopsziát végeznek.
Kezelés
Az NLF diagnosztizálásakor (a végbélhőmérséklet-diagramok szerint a 2. fázis időtartama kevesebb, mint 11 nap, fokozatos hőmérséklet-emelkedés figyelhető meg, az endometrium szekréciós átalakulása nem megfelelő az endometrium biopsziás adatai szerint, alacsony a progeszteronszint a vérszérumban) meg kell határozni az ilyen rendellenességek okát.
Ha az NLF-et hiperprolaktinémia kíséri, akkor az agy MRI-vizsgálatát végzik. Alternatív módszer a koponya röntgenvizsgálata (sella turcica régió).
A hiperprolaktinémia első szakasza az agyalapi mirigy adenoma kizárása, amely sebészeti kezelést igényel. Jelentős változások hiányában a hiperprolaktinémiát funkcionálisnak tekintjük, és a prolaktinszint normalizálására bromokriptin kezelést írnak fel. A bromokriptin kezdeti adagja 1,25 mg/nap 2 héten keresztül, a prolaktinszint monitorozása után, ha a mutatók nem normalizálódnak, az adagot 2,5 mg/napra emelik. A prolaktinszint jelentős emelkedése esetén a kezdeti adag 2,5 mg/nap. Terhesség esetén a bromokriptin szedését abba kell hagyni.
Pajzsmirigy-alulműködés kimutatása esetén az endokrinológussal közösen határozzák meg a pajzsmirigy-patológia jellegét. Mindenesetre napi nátrium-levotiroxin-terápia javasolt, az adagot egyénileg választják ki, amíg a TSH-szint normalizálódik. Terhesség esetén a nátrium-levotiroxin-kezelést folytatni kell. A terhesség első trimeszterében az adag emelésének célszerűségét az endokrinológussal közösen döntik el a hormonális vizsgálat eredményeinek (TSH-szint, szabad tiroxin) kézhezvétele után.
Az NLF korrekcióját kétféleképpen végezzük. Az első módszer az ovuláció stimulálása, a második módszer a progeszteronkészítményekkel végzett helyettesítő terápia.
Az első kezelési lehetőség az ovuláció stimulálása klomifén-citráttal. Ez a kezelési módszer azon a tényen alapul, hogy a luteális fázis zavarainak többsége a ciklus follikuláris fázisában alakul ki. A progeszteronszint állandó csökkenése a második fázisban a ciklus első fázisában a follikulogenézis zavarának következménye. Ez a rendellenesség nagyobb sikerrel korrigálható alacsony dózisú klomifén-citráttal a korai follikuláris fázisban, mint progeszteron felírásával a ciklus második fázisában.
Az első ciklusban a klomifén-citrát adagja 50 mg/nap a menstruációs ciklus 5. és 9. napja között. A hatékonyságot végbélhőmérséklet mérésével, a progeszteronszint mérésével a ciklus 2. fázisában vagy dinamikus ultrahanggal követik nyomon. Ha a második ovuláció stimulációs ciklusában nincs elegendő hatás, a klomifén-citrát adagját a ciklus 5. és 9. napja között 100 mg/napra kell emelni. A harmadik ovuláció stimulációs ciklusában a maximálisan lehetséges adag 150 mg/nap. Az adag ilyen emelése csak akkor lehetséges, ha a gyógyszer jól tolerálható (nincs intenzív fájdalom az alhasban és a derékban, és nincsenek egyéb petefészek-hiperstimulációs tünetek).
A második kezelési lehetőség: a progeszteronkészítményekkel végzett szubsztitúciós terápia, amely elősegíti az endometrium teljes szekréciós átalakulását, ami a szükséges hatást biztosítja a megőrzött ovulációjú, habituális vetélésben szenvedő betegeknél. Ezenkívül az utóbbi években megállapították, hogy a progeszteronkészítmények adagolása nemcsak hormonális, hanem immunmoduláló hatással is bír, elnyomva az endometrium immunkompetens sejtjeinek kilökődési reakcióit. Különösen hasonló hatást írtak le a dihidrogeszteron esetében 20 mg/nap dózisban. Szubsztitúciós terápia céljából a didrogeszteront 20 mg/nap dózisban orálisan, vagy mikronizált progeszteront hüvelyileg 200 mg/nap dózisban alkalmazzák. A kezelést az ovuláció utáni 2. napon (a végbélhőmérséklet emelkedését követő napon) végzik, és 10 napig folytatják. Terhesség esetén a progeszteronkészítményekkel végzett kezelést folytatni kell.
A modern kutatások nem erősítették meg az emberi koriongonadotropin hatékonyságát az ismétlődő vetélés kezelésében.
Hiperandrogenizmus (petefészek vagy mellékvese eredetű) esetén rendszeres vetélés esetén gyógyszeres kezelés javasolt az androgének ovuláció teljességére és az endometrium állapotára gyakorolt hatása miatt. A mellékvese androgének bioszintézisének zavara esetén virilizáló hatásuk lehetséges a női magzatra, ezért a magzat érdekében szteroidterápiát végeznek.
A petefészek eredetű hiperandrogenizmus (policisztás petefészkek)
Kórtörténet, fizikális vizsgálat és speciális vizsgálatok eredményei
- Kórtörténet: késői menstruáció, menstruációs ciklus zavarai, például oligomenorrhoea (általában primer, ritkábban szekunder). A terhességek ritkák, általában spontán megszakítódnak az első trimeszterben, a terhességek között hosszú meddőségi időszakokkal.
- Vizsgálat: hirsutizmus, akne, striák, magas testtömegindex (opcionális).
- Rektális hőmérsékleti grafikonok: anovulációs ciklusok váltakoznak ovulációs és NLF-es ciklusokkal.
- Hormonvizsgálat: magas tesztoszteronszint, emelkedett FSH és LH szint is lehet, az LH/FSH arány nagyobb, mint 3. Ultrahang: policisztás ováriumok.
Kezelés
Nem gyógyszeres kezelés
Fogyás - diétaterápia, fizikai aktivitás.
Gyógyszeres kezelés
- Orlisztát 120 mg-os dózisban minden főétkezéskor. A kúra időtartamát a hatás és a tolerálhatóság figyelembevételével határozzák meg.
- Előzetes tesztoszteronszint-csökkentés ciproteron-acetátot (2 mg) és EE-t (35 mcg) tartalmazó készítményekkel 3 menstruációs cikluson keresztül.
- Fogamzásgátlás abbahagyása, a ciklus második fázisának hormonális támogatása (gesztagén terápia) - didrogeszteron 20 mg/nap dózisban a menstruációs ciklus 16. és 25. napja között. Ha nincs spontán ovuláció, folytassa a következő szakaszba.
- Az ovuláció stimulálása klomifén-citráttal, kezdeti 50 mg/nap dózisban a menstruációs ciklus 5. és 9. napja között, gesztagénekkel (napi 20 mg-os didrogeszteron dózisban a ciklus 16. és 25. napja között) és dexametazonnal (0,5 mg) történő egyidejű terápiával.
- Terhesség hiányában a klomifén-citrát adagját napi 100–150 mg-ra emelik, a ciklus második fázisában gesztagének és dexametazon (0,5 mg) adagolásával. Megállapították, hogy bár a dexametazon csak a mellékvese-androgének szintjét csökkenti, az ovuláció és a fogamzás szignifikánsan gyakrabban fordul elő klomifén-citrát és dexametazon együttes alkalmazásával, mint a klomifén-citrát önmagában történő alkalmazásával [12].
- Három ovulációs stimulációs ciklust hajtanak végre, majd három menstruációs ciklus szünetét javasolják gesztagén támogatással, és döntést kell hozni a laparoszkópos hozzáféréssel végzett sebészeti kezelésről (a petefészkek ék alakú reszekciója, lézeres párologtatás).
A beteg további ellátása
A terhesség 16 hetes kezelését gesztagén terápiával kell kísérni (napi 20 mg-os didrogeszteron vagy napi 200 mg-os mikronizált progeszteron), a dexametazont csak a terhesség első trimeszterében írják fel. Az isthma-cervicalis elégtelenség időben történő diagnosztizálása és szükség esetén sebészeti korrekciója érdekében monitorozás szükséges.
Mellékvese-hiperandrogenizmus (pubertás és posztpubertás adrenogenitális szindróma)
Az adrenogenitális szindróma (AGS) egy örökletes betegség, amely a mellékvesekéreg hormonjainak szintézisének zavarával jár, amelyet számos enzimrendszer szintéziséért felelős gének károsodása okoz. A betegség autoszomális recesszív módon öröklődik, mindkét szülőtől, akik egészséges hordozók, mutáns gének átadásával.
Az esetek 90%-ában az adrenogenitális szindrómát a CYP21B gén mutációi okozzák, ami a 21-hidroxiláz szintézisének zavarához vezet.
Kórtörténet, fizikális vizsgálat és speciális vizsgálatok eredményei
- Kórtörténet: késői menstruáció, enyhén megnyúlt menstruációs ciklus, lehetséges oligomenorrhoea, spontán vetélés az első trimeszterben, lehetséges meddőség.
- Vizsgálat: akne, hirsutizmus, android testalkat (széles vállak, keskeny medence), csiklómegnagyobbodás.
- Rektális hőmérsékleti grafikonok: anovulációs ciklusok váltakoznak ovulációs és NLF-es ciklusokkal.
- Hormonális teszt: magas 17-OP, DHEAS szint.
- Ultrahang: a petefészkek változatlanok.
A terhességen kívüli patognomonikus jel a 17-OP koncentrációjának növekedése a vérplazmában.
Jelenleg az ACTH-val végzett tesztet alkalmazzák a mellékvese hiperandrogenizmus látens, nem klasszikus formájának diagnosztizálására. Ehhez a teszthez a Synacthen-t használják - egy szintetikus polipeptidet, amely az endogén ACTH tulajdonságaival rendelkezik, azaz serkenti a szteroid hormonok koleszterinből történő szintézisének kezdeti fázisait a mellékvesékben.
Synacthen teszt (ACTH analóg): 1 ml (0,5 mg) Synacthen-t fecskendeznek bőr alá a vállba, majd a reggeli 9 órás vérplazmamintában először a kezdeti 17-OP és kortizol szintet határozzák meg. Az injekció beadása után 9 órával kontroll vérmintát vesznek a 17-OP és a kortizol szintjének meghatározására. A meghatározási indexet (D) ezután a következő képlettel számítják ki:
D = 0,052 × 17-OP + 0,005 × kortizol/17-OP - 0,018 × kortizol/17-OP
Ha a D-együttható értéke kisebb vagy egyenlő, mint 0,069, az a mellékvese hiperandrogenizmusának hiányát jelzi. Ha a D-együttható értéke nagyobb, mint 0,069, akkor a hiperandrogenizmust a mellékvesék diszfunkciója okozza.
Gyógyszeres kezelés
A 21-hidroxiláz-hiány okozta hiperandrogenizmus kezelésének fő eleme a glükokortikoidok, amelyeket a túlzott androgénszekréció elnyomására használnak.
A beteg további ellátása
Az anyai androgének magzatra gyakorolt virilizáló hatása miatt, a mellékvese-hiperandrogenizmus megállapított diagnózisa esetén a terhesség előtt 0,25 mg-os kezdeti dózisban dexametazonnal kezelik, és a terhesség teljes időtartama alatt egyénileg kiválasztott dózisban (0,5-1 mg) folytatják. Mellékvese-hiperandrogenizmusban szenvedő, rendszeres vetélésben szenvedő nőknél nem helyénvaló a kezelés megszakítása, mivel a vetélések gyakorisága kezelés hiányában eléri a 14%-ot, a folytatás pedig a 9%-ot.
Tekintettel arra, hogy az adrenogenitális szindrómában szenvedő betegek átadhatják ezt a gént a magzatnak, prenatális diagnosztikát kell végezni: a terhesség 17-18. hetében vérvizsgálatot írnak elő az anya 17-OP-tartalmának meghatározására. Ha a hormon szintje a vérben megemelkedik, meghatározzák a koncentrációját a magzatvízben. Ha a 17-OP-tartalom a magzatvízben megemelkedik, a magzatnál adrenogenitális szindrómát diagnosztizálnak. Sajnos az adrenogenitális szindróma súlyosságát (enyhe vagy sópazarló súlyos forma) a magzatvíz 17-OP-szintje alapján nem lehet meghatározni. A terhesség fenntartásának kérdését ebben a helyzetben a szülők döntik el.
Ha a gyermek apja az adrenogenitális szindróma génjének hordozója, és a családban előfordultak ilyen szindrómával született gyermekek, akkor a beteg, még mellékvese-hiperandrogenizmus nélkül is, a magzat érdekében (a lánymagzat virilizációjának megelőzése érdekében) dexametazont kap 20 mcg/testtömegkg dózisban, legfeljebb 1,5 mg/nap 2-3 adagban, étkezés után. A 17-18. héten, a magzat nemének és az adrenogenitális szindróma gén expressziójának meghatározása után (az amniocentézis eredményei alapján), a kezelést a terhesség végéig folytatják, ha a magzat adrenogenitális szindrómában szenvedő lány. Ha a magzat fiú vagy lány, aki nem hordozza az adrenogenitális szindróma génjét, a dexametazon adagolása leállítható.
Ha egy rendszeres vetélésben szenvedő nő mellékvese-hiperandrogenizmusban szenved, akkor a dexametazon-kezelést a terhesség teljes ideje alatt végzik, és csak a szülés után hagyják abba. A szülés utáni 3. napon a dexametazon adagját fokozatosan csökkentik (3 naponta 0,125 mg-mal), amíg a szülés utáni időszakban teljesen le nem állítják.
Vegyes eredetű hiperandrogenizmus (petefészek és mellékvese)
Kórtörténet, fizikális vizsgálat és speciális vizsgálatok eredményei
- Kórtörténet: késői menstruáció, menstruációs ciklus zavarai, például oligomenorrhoea (általában primer, ritkábban másodlagos), amenorrhoea, esetleges sérülések, agyrázkódások. A terhességek ritkák, általában spontán megszakadnak az első trimeszterben, a terhességek között hosszú meddőségi időszakok vannak.
- Fizikális vizsgálat: hirsutizmus, akne, striák, acanthosis nigricans, magas testtömegindex, magas vérnyomás.
- Rektális hőmérsékleti grafikonok: anovulációs ciklusok váltakoznak ovulációs és NLF-es ciklusokkal.
- Hormonvizsgálat: magas tesztoszteronszint, emelkedett FSH és LH szint, 3-nál nagyobb LH/FSH arány, magas DHEAS, 17-OP szint, hiperprolaktinémia is előfordulhat.
- Ultrahang: policisztás petefészkek.
- Elektroencefalográfia: az agy bioelektromos aktivitásának változásai.
- Hiperinzulinémia, lipidanyagcsere-zavar (magas koleszterinszint, alacsony sűrűségű lipoproteinek és nagyon alacsony sűrűségű lipoproteinek), csökkent glükóztolerancia vagy emelkedett vércukorszint.
Kezelés
Nem gyógyszeres kezelés
Fogyás (alacsony kalóriatartalmú étrend, fizikai aktivitás).
Gyógyszeres kezelés
Az első szakasz - inzulinrezisztencia jelenlétében ajánlott a metformint napi 1000-1500 mg-os dózisban felírni az inzulinérzékenység növelése érdekében.
A második szakasz - súlyos menstruációs cikluszavarok és magas tesztoszteronszint esetén ajánlott 3 hónapig antiandrogén hatású, ciproteron-acetátot (2 mg) és etinil-ösztradiolt (35 mcg) tartalmazó gyógyszereket felírni.
A harmadik szakasz az ovuláció stimulálása, majd gesztagén támogatás (a sémát fentebb ismertettük) és dexametazon szedése napi 0,25–0,5 mg dózisban.
Hiperprolaktinémia és pajzsmirigy-alulműködés esetén megfelelő gyógyszerkorrekciót kell végezni az ovulációt stimuláló ciklusokban. Terhesség esetén a bromokriptin szedését abba kell hagyni, és a levotiroxin szedését folytatni kell.
Ha az ovuláció stimulálása hatástalan, el kell dönteni a közvetlen ovulációinduktorok felírásának kérdését, a policisztás petefészkek sebészeti kezelésének vagy az in vitro megtermékenyítés célszerűségét.
A beteg további ellátása
Metabolikus szindrómában szenvedő betegeknél a terhességet gyakran bonyolítja az artériás magas vérnyomás, a nephropathia és a hypercoagulatio, amelyekkel összefüggésben a terhesség korai szakaszától kezdve monitorozni kell a vérnyomást, a hemostasiogramokat, és a felmerülő rendellenességeket (szükség esetén) vérnyomáscsökkentő gyógyszerekkel, vérlemezke-gátlókkal és antikoagulánsokkal kell korrigálni. A gesztagén gyógyszereket a terhesség 16. hetéig írják fel - didrogeszteront 20 mg/nap dózisban vagy mikronizált progeszteront 200 mg/nap dózisban, 2 adagban.
Minden hiperandrogenizmusban szenvedő nő kockázati csoportot képvisel az isthmás-méhnyaki elégtelenség kialakulására. A méhnyak állapotának monitorozását a terhesség 16. hetétől kell elvégezni, szükség esetén az isthmás-méhnyaki elégtelenség sebészeti korrekcióját.
A rendszeres vetélés immunológiai okai
Jelenleg ismert, hogy az összes korábban megmagyarázhatatlan, ismételt vetélés körülbelül 80%-a (a genetikai, anatómiai, hormonális okok kizárása után) immunrendszeri rendellenességekkel jár. Megkülönböztetünk autoimmun és alloimmun betegségeket, amelyek a habituális vetéléshez vezetnek.
Az autoimmun folyamatok során az immunrendszer saját szövetei válnak az agresszió tárgyává, azaz az immunválasz a saját antigénjei ellen irányul. Ebben a helyzetben a magzat másodlagosan szenved az anya szöveteinek károsodása következtében.
Alloimmun betegségek esetén a nő immunválasza az apától kapott embrionális/magzati antigének ellen irányul, amelyek potenciálisan idegenek az anya szervezete számára.
A habituális vetélésben szenvedő betegeknél leggyakrabban előforduló autoimmun betegségek közé tartozik az antifoszfolipid, antitiroid és antinukleáris autoantitestek jelenléte a szérumban. Így megállapították, hogy a terhességen kívüli habituális vetélésben szenvedő nők 31%-ánál vannak tireoglobulin és pajzsmirigy-peroxidáz elleni autoantitestek (pajzsmirigy mikroszomális [pajzsmirigy-peroxidáz] autoantitestek); ezekben az esetekben a spontán vetélés kockázata a terhesség első trimeszterében 20%-ra nő. Habituális vetélés esetén az antinukleáris és antitiroid antitestek jelenléte további vizsgálatok szükségességét jelzi az autoimmun folyamat azonosítása és a diagnózis megerősítése érdekében.
Az antifoszfolipid szindróma (APS) továbbra is egy általánosan elismert autoimmun állapot, amely embrió-/magzati halálhoz vezet.
Alloimmun betegségek
Jelenleg a magzati kilökődéshez vezető alloimmun folyamatok közé tartozik a házastársakban a fő hisztokompatibilitási komplex rendszer közös antigénjeinek megnövekedett (több mint 3) száma (gyakran megfigyelhető vérrokon házasságokban); az anya szérumában a blokkoló faktorok alacsony szintje; a természetes ölősejtek (NK-sejtek CD56, CD16) szintjének növekedése az anya endometriumában és perifériás vérében, mind a terhességen kívül, mind a terhesség alatt; számos citokin magas koncentrációja az endometriumban és a vérszérumban, különösen a γ-interferon, a tumor nekrózis faktor a, az interleukinok-1 és -2.
Jelenleg a korai vetélésekhez vezető alloimmun tényezőket és a fenti állapotok korrigálásának módjait vizsgálják. A terápiás módszerekről nincs konszenzus. Egyes kutatók szerint a donor limfocitákkal végzett aktív immunizálás nem eredményez jelentős hatást, míg más szerzők jelentős pozitív hatást írnak le az ilyen immunizálás és az immunglobulinokkal történő kezelés során.
Jelenleg a korai terhesség egyik immunmoduláló szere a progeszteron. Különösen a didrogeszteron szerepét bizonyították napi 20 mg-os dózisban olyan nőknél, akiknél a terhesség első trimeszterében rendszeres vetélés történt, és a méhnyálkahártyában megnövekedett a CD56-sejtek száma.
 [ 11 ], [ 12 ], [ 13 ], [ 14 ], [ 15 ], [ 16 ]
[ 11 ], [ 12 ], [ 13 ], [ 14 ], [ 15 ], [ 16 ]
Genetikailag meghatározott trombofíliák
A genetikailag meghatározott trombofíliák következő formáit tekintik terhesség alatti trombofíliás állapotoknak, amelyek habituális vetéléshez vezetnek.
- Antitrombin III hiány.
- V. faktor mutáció (Leiden mutáció).
- C-protein hiány.
- S-fehérje hiány.
- Protrombin génmutáció G20210A.
- Hiperhomociszteinémia.
A trombofília ritka okainak azonosítására irányuló vizsgálat szükséges azokban az esetekben, amikor:
- családi anamnézis - tromboembólia 40 éves kor előtt rokonoknál;
- megbízható vénás és/vagy artériás trombózis epizódok 40 éves kor előtt;
- visszatérő trombózis a betegben és közvetlen hozzátartozóiban;
- tromboembóliás szövődmények terhesség alatt és szülés után hormonális fogamzásgátlás alkalmazása esetén;
- ismételt vetélések, halvaszületések, méhen belüli növekedési retardáció, méhlepényleválás;
- korai preeclampsia, HELLP szindróma.
A rendszeres vetélés fertőző okai
A fertőző faktor szerepe a rendszeres vetélés okaként jelenleg széles körben vitatott. Ismert, hogy a terhesség korai szakaszában bekövetkező elsődleges fertőzés az élettel összeegyeztethetetlen embriókárosodást okozhat, ami szórványos spontán vetéléshez vezethet. Azonban a fertőzés ismételt vetélésekkel egyidejűleg történő újraaktiválódásának valószínűsége elhanyagolható. Ezenkívül jelenleg nem találtak olyan mikroorganizmusokat, amelyek rendszeres vetélést provokálnának. Az elmúlt évek tanulmányai kimutatták, hogy a rendszeres vetéléssel és krónikus endometritiszben szenvedő nők többségénél 2-3 vagy több típusú obligát anaerob mikroorganizmus és vírus előfordulása figyelhető meg az endometriumban.
V. M. Sidelnikova és munkatársai szerint a terhességen kívüli krónikus endometritisz diagnózisát az esetek 73,1%-ában szövettanilag igazolták, és 86,7%-ában opportunista mikroorganizmusok perzisztenciáját figyelték meg az endometriumban, ami kétségtelenül az immunpatológiai folyamatok aktiválódásának oka lehet. A kevert perzisztáló vírusfertőzés (herpes simplex vírus, Coxsackie A, Coxsackie B, enterovírusok 68–71, citomegalovírus) szignifikánsan gyakrabban fordul elő a rendszeres vetélésben szenvedő betegeknél, mint a normális szülészeti előzményű nőknél. K. Kohut és munkatársai (1997) kimutatták, hogy az elsődlegesen ismétlődő vetélésben szenvedő betegeknél a méhnyálkahártya és a deciduális szövet gyulladásos változásainak százalékos aránya szignifikánsan magasabb, mint a vetélés utáni nőknél, akiknek legalább egy teljes idejükre született gyermekeik voltak a kórtörténetükben.
Az endometrium bakteriális és vírusos kolonizációja általában az immunrendszer és a szervezet nem specifikus védőerőinek (komplementrendszer, fagocitózis) a fertőző ágens teljes eliminálására való képtelenségéből adódik, ugyanakkor terjedését a T-limfociták (T-helperek, természetes ölősejtek) és a makrofágok aktiválódása korlátozza. Mindezen esetekben mikroorganizmusok perzisztenciája következik be, amelyet a krónikus gyulladás helyéhez vonzódó mononukleáris fagociták, természetes ölősejtek, T-helperek jellemeznek, amelyek különböző citokineket szintetizálnak. Nyilvánvalóan az endometrium ilyen állapota megakadályozza a lokális immunszuppresszió kialakulását a beágyazódás előtti időszakban, ami a védőgát kialakításához és a félig idegen magzat kilökődésének megakadályozásához szükséges.
E tekintetben a terhesség előtt a rendszeres vetélésben szenvedő nőknél krónikus endometritist kell diagnosztizálni. A diagnózis felállításához vagy kizárásához a menstruációs ciklus 7-8. napján endometrium biopsziát végeznek, amelyhez szövettani, PCR- és bakteriológiai vizsgálatot végeznek a méhüregből vett anyagból. A diagnózis megerősítésekor a krónikus endometritist a medencei szervek gyulladásos betegségeinek kezelésére vonatkozó standardok szerint kezelik.

