A cikk orvosi szakértője
Új kiadványok
Gyógyszerek
Neuroleptikumok vagy antipszichotikumok
Utolsó ellenőrzés: 04.07.2025

Minden iLive-tartalmat orvosi szempontból felülvizsgáltak vagy tényszerűen ellenőriznek, hogy a lehető legtöbb tényszerű pontosságot biztosítsák.
Szigorú beszerzési iránymutatásunk van, és csak a jó hírű média oldalakhoz, az akadémiai kutatóintézetekhez és, ha lehetséges, orvosilag felülvizsgált tanulmányokhoz kapcsolódik. Ne feledje, hogy a zárójelben ([1], [2] stb.) Szereplő számok ezekre a tanulmányokra kattintható linkek.
Ha úgy érzi, hogy a tartalom bármely pontatlan, elavult vagy más módon megkérdőjelezhető, jelölje ki, és nyomja meg a Ctrl + Enter billentyűt.
Az antipszichotikumok (neuroleptikumok) a pszichotróp gyógyszerek egy csoportja, amelyeket elsősorban a skizofrénia kezelésére használnak. Jelenleg két gyógyszercsoportot (vagy kategóriát) szokás megkülönböztetni: tipikus és atipikus antipszichotikumokat. Az alábbiakban információkat talál ezen gyógyszercsoportok farmakológiai tulajdonságairól, alkalmazási javallatairól és a terápia mellékhatásairól.
A tipikus antipszichotikumok alkalmazásának indikációi
Jelenleg a hagyományos neuroleptikumok felírásának főbb indikációi, a pszichofarmakoterápia területén tevékenykedő mérvadó kutatók ajánlásai szerint, a következők.
- Súlyos pszichotikus tünetek okozta pszichomotoros agitáció és viselkedési zavarok enyhítése. Ezekben az esetekben antipszichotikus hatású gyógyszerek orális vagy parenterális formáinak alkalmazása javasolt, mind globális (klopromazin, levomepromazin, tioproperazin, zuklopentixol), mind szelektív - hallucinációs-paranoid zavarokra gyakorolt hatás formájában (haloperidol, trifluoperazin).
- Relapszusgátló (megelőző) terápia. Erre a célra depó gyógyszereket írnak fel, különösen a rossz gyógyszer-együttműködésű betegeknél (haloperidol-dekanoát, flupentixol tartós formája), vagy kis vagy közepes dózisú gyógyszereket a diszinhibitoros (antinegatív) hatás elérése érdekében, azok közül a gyógyszerek közül, amelyek nagy dózisait az akut pszichotikus rendellenességek enyhítésére használják (flupentixol, zuklopentixol). Az ilyen típusú terápiában úgynevezett kis neuroleptikumok (tioridazin, klórprotixén, szulpirid) felírása is ajánlott, amelyek pszichotróp aktivitása a depressziós pólus és az álmatlansági rendellenességek megnyilvánulásaira gyakorolt hatásban áll.
- Az atipikus antipszichotikumokkal szembeni terápiás rezisztencia leküzdése akut pszichotikus állapotok kezelésében. Erre a célra általában a hagyományos antipszichotikumok parenterális formáit alkalmazzák, amelyek globális (klórpromazin, levomepromazin stb.) és szelektív (haloperidol) antipszichotikus hatásúak.
Ezek a gyógyszerek különféle mellékhatásokat okoznak, amelyek jellege az egyes gyógyszerek farmakológiai profiljának jellemzőitől függ. A kifejezettebb kolinolitikus hatású antipszichotikumok gyakrabban okoznak akkomodációs zavarokat, székrekedést, szájszárazságot és vizeletretenciót. A szedatív hatás inkább a kifejezett antihisztamin hatású antipszichotikumokra jellemző, míg az ortosztatikus hipotenzió az α1-adrenerg receptorokat blokkoló gyógyszerekre jellemző. A kolinerg, noradrenerg és dopaminerg transzmisszió tipikus neuroleptikumok általi blokkolása számos szexuális szférabeli rendellenességhez vezethet, mint például amenorrhoea vagy dysmenorrhoea, anorgasmia, galaktorrhoea, az emlőmirigyek duzzanata és fájdalma, valamint a potencia csökkenése. A szexuális szférában jelentkező mellékhatások főként ezen gyógyszerek kolinolitikus és adrenoblokkoló tulajdonságaihoz, valamint a dopamin-anyagcsere blokkolása miatti prolaktin szekréció növekedéséhez kapcsolódnak. A tipikus neuroleptikumok legsúlyosabb mellékhatásai a motoros diszfunkciók. Ezek a leggyakoribb oka annak, hogy a betegek abbahagyják a gyógyszerek szedését. A motoros szférára gyakorolt hatással összefüggő három fő mellékhatás a korai extrapiramidális szindrómák, a tardív diszkinézia és az NMS.
Az extrapiramidális szindrómákról úgy tartják, hogy a bazális ganglionokban található D2 receptorok blokádjával járnak. Ilyenek például a disztónia, a neuroleptikus parkinsonizmus és az akathisia. Az akut disztóniás reakció (korai diszkinézia) tünetei közé tartozik a hirtelen kialakuló hiperkinézis, az oculogriás krízisek, az arc és a törzs izmainak összehúzódásai, az opisthotonus. Ezek a rendellenességek dózisfüggőek, és gyakran 2-5 napos, erős neuroleptikumokkal, például haloperidollal és flufenazinnal végzett kezelés után jelentkeznek. A korai diszkinézia enyhítésére a neuroleptikum adagját csökkentik, és antikolinerg szereket (biperiden, trihexifenidil) írnak fel. A tardív diszkinézia általában a nyakizmokat érinti, és az akut disztóniás reakcióval ellentétben kevésbé reagál az antikolinerg kezelésre. A neuroleptikus parkinsonizmust a spontán motoros készségek csökkenése, a hipo- és amimia, a nyugalmi tremor és a rigiditás jellemzi. Fontos megkülönböztetni ezeket a tüneteket a skizofrénia külsőleg hasonló negatív rendellenességeitől, amelyeket az érzelmi elidegenedés, az érzelmek tompulása és az energia hiánya képvisel. Ezen mellékhatások korrigálására antikolinerg szerek alkalmazása, a neuroleptikum adagjának csökkentése vagy atipikus antipszichotikummal való helyettesítése javasolt. Az akathisia belső szorongásban, a hosszú ideig egy helyben maradás képtelenségében és a karok vagy lábak folyamatos mozgatásának szükségességében nyilvánul meg. Enyhítésére antikolinerg szereket és központi béta-blokkolókat (propranololt) alkalmaznak.
A késői diszkinézia bármely izomcsoport, leggyakrabban a nyelv és a száj izmainak akaratlan mozgásában nyilvánul meg. Klinikailag számos formáját különböztetik meg: az arc, a nyelv, a száj izmainak diszkinéziája (a rágóizmok periodikus összehúzódásai, grimaszoló személy benyomását keltve, a nyelv akaratlanul kiállhat a beteg szájából); tardív disztónia és tardív akathisia; (a beteg koreoathetoid mozgásokat végez a fejében, a törzsében, a felső és az alsó végtagokban). Ez a rendellenességi forma főként a hagyományos neuroleptikumokkal történő hosszú távú kezelés során jelentkezik, és a fenntartó terápiaként szedő betegek körülbelül 15-20%-ánál észlelhető. Valószínűleg egyes betegeknél megnő a diszkinézia tünetei kialakulásának kockázata, mivel néhányukat a skizofrénia klinikáján már a "neuroleptikus korszak" előtt is megfigyelték. Ezenkívül tardív diszkinéziát írtak le idős nőknél és affektív zavarokban szenvedő betegeknél is. A tardív diszkinézia feltehetően a striatumban található dopaminreceptorok számának növekedésével jár, bár valószínűleg a GABAerg és más neurotranszmitter rendszerek is szerepet játszanak a patogenezisében. Az ilyen mellékhatásokra nincs hatékony univerzális kezelés. Felmerült, hogy a dopamin-blokkoló hatású, nagy hatékonyságú neuroleptikumok vagy az E-vitamin alacsony dózisai mérsékelten jótékony hatással lehetnek ezekre a rendellenességekre. A tardív diszkinézia leghatékonyabb intézkedése egy tipikus neuroleptikum dózisának csökkentése vagy egy atipikus antipszichotikummal való helyettesítése.
A jelenlegi adatok szerint a neuroleptikus malignus szindróma a pszichofarmakoterápiás esetek körülbelül 0,5%-ában fordul elő. Valószínűleg az ilyen életveszélyes szövődmény ritka előfordulása jelenleg az atipikus antipszichotikumok széles körű gyakorlati bevezetésével magyarázható, mivel az NMS kialakulásának kockázata ezekkel a gyógyszerekkel történő kezelés során elhanyagolható. Általánosan elfogadott, hogy az NMS kialakulásának fő oka a dopaminerg rendszer túlzott blokádja a neuroleptikumokkal végzett terápia során, különösen egy erős antipszichotikum adagjának emelése után. Az NMS fő tünetei a hipertermia, a vázizomzat és az ínreflexek fokozott tónusa, a kómába való átmenettel járó tudatzavar. A vérvizsgálatok leukocitózist, fokozott eritrocita-süllyedést és máj transzamináz aktivitást mutatnak ki; a vizeletvizsgálatok albuminuria jelenlétét mutatják ki. A víz- és elektrolit-egyensúly zavarai gyorsan bekövetkeznek, ami megteremti az agyödéma kialakulásának előfeltételeit. Az NMS egy akut állapot, amely a beteg sürgős kórházi kezelését igényli intenzív infúziós terápia céljából. Az NMS kezelésében a legfontosabb a hidratáció és a tüneti kezelés. Ebben a helyzetben minden felírt neuroleptikum azonnali leállítását igényli. Bizonyos esetekben a dopaminreceptor-agonisták (például a bromokriptin) vagy az izomrelaxánsok pozitív hatást fejtenek ki, bár hatékonyságukat nem vizsgálták. Az NMS megszüntetése után a neuroleptikum szedését legalább két hétig nem szabad újrakezdeni. Ezt követően alacsony hatékonyságú antipszichotikum írható fel, lehetőleg egy új generációs gyógyszer. Az újonnan felírt gyógyszer adagját rendkívül óvatosan kell emelni, az életfunkciók állapotának és a laboratóriumi adatok (vér- és vizeletvizsgálatok) monitorozásával.
A tipikus neuroleptikumok ritkán okoznak veszélyes, halálos szövődményeket. A túladagolás tünetei főként a gyógyszer antiadrenerg és antikolinerg hatásának egyéni profiljához kapcsolódnak. Mivel ezek a gyógyszerek erős hányingercsillapító hatással rendelkeznek, a szervezetből való eltávolításukhoz gyomormosás javasolt, nem pedig hánytatók adagolása. Az artériás hipotenzió általában az adrenerg receptor blokád következménye, és dopamin és noradrenalin adagolásával kell korrigálni. Szívritmuszavar esetén lidokain alkalmazása javasolt.
A tipikus antipszichotikumok hatásmechanizmusa és farmakológiai hatásai
A pszichofarmakológia fejlődésével számos lehetőséget javasoltak az antipszichotikumok neuroreceptorokra gyakorolt hatásának vizsgálatára. A fő hipotézis továbbra is az, hogy a dopamin neurostruktúrákat (elsősorban a D2 receptorokat) befolyásolják, a pszichózisokban az agyi struktúrákban a normális dopamin-anyagcsere zavaraira vonatkozó adatok alapján. A dopamin D2 receptorok a bazális ganglionokban, a nucleus accumbensben és a frontális kéregben találhatók; vezető szerepet játszanak az agykéreg és a talamusz közötti információáramlás szabályozásában.
Az ábra részletesebben bemutatja a dopaminátvitel zavarait az agy kérgi és kéreg alatti területein, valamint e zavarok szerepét a skizofrénia tüneteinek kialakulásában (Jones RB, Buckley PF, 2006 monográfiájából adaptálva).
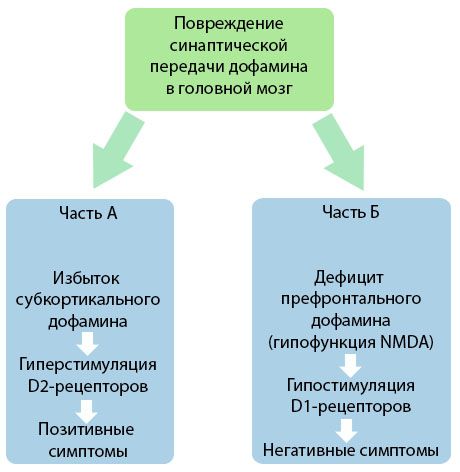
Az A rész a klasszikus, korai dopamin-elméletet tükrözi, amely a dopamin feleslegét feltételezi a kéreg alatti területeken, valamint a D2 receptorok hiperstimulációját, ami produktív tünetek megjelenéséhez vezet. A B rész az elmélet későbbi modernizációját mutatja be az 1990-es évek elején. Az addigra megszerzett adatok azt mutatták, hogy a dopamin hiánya a D receptorokban, valamint ezen receptorok elégtelen stimulációja a prefrontális kéregben negatív tünetek és kognitív deficitek megjelenéséhez vezet. Ezért a modern felfogás szerint mindkét típusú dopaminerg transzmissziós zavar – a kéreg alatti dopamin feleslege és hiánya a prefrontális kéregben – a prefrontális területen a szinaptikus transzmisszió zavarának együttes eredménye, és az N-metil-N-aszpartát hipofunkciójával jár. Az eredetileg izolált dopamin mellett később más, a skizofrénia patogenezisében részt vevő neurotranszmittereket is azonosítottak, mint például a szerotonin, a gamma-aminovajsav, a glutamát, a noradrenalin, az acetilkolin és a különféle neuropeptidek. Bár ezen mediátorok szerepét még nem vizsgálták teljes mértékben, a tudás bővülésével azonban világossá válik, hogy számos neurokémiai eltolódás manifesztálódik a szervezetben. Ezért egy antipszichotikus gyógyszer klinikai hatása a különböző receptorképződésekre gyakorolt hatások összegzése, és a homeosztázis zavarainak megszüntetéséhez vezet.
Az utóbbi években az olyan új kutatási módszerek megjelenésének köszönhetően, mint a radioizotópos ligandkötés és a PET-vizsgálat, jelentős előrelépés történt a neuroleptikumok finom biokémiai hatásmechanizmusának tisztázásában. Különösen a gyógyszerek összehasonlító erősségét és tropizmusát határozták meg az agy különböző területein és struktúráiban található egyes neuroreceptorokhoz való kötődés tekintetében. Kimutatták, hogy a gyógyszer antipszichotikus hatásának súlyossága közvetlenül függ a különböző dopaminerg receptorokra gyakorolt blokkoló hatásának erősségétől. A közelmúltban négy ilyen receptortípust azonosítottak:
- A D1 túlnyomórészt a substantia nigra és a striatum (az úgynevezett nigrostriatális régió), valamint a prefrontális régió területén helyezkednek el;
- D2 - a nigrostriatális, mezolimbikus régiókban és az elülső agyalapi mirigyben (prolaktin szekréció);
- D3 (preszinaptikus) - különböző agyi struktúrákban a negatív visszacsatolás törvénye szerint szabályozza a dopaminerg aktivitást;
- D4 (preszinaptikus) - túlnyomórészt a nigrostriatális és mezolimbikus területeken található.
Ugyanakkor ma már bizonyítottnak tekinthető, hogy a D2 receptorok blokádja okozza az antipszichotikus, másodlagos szedatív hatások, valamint az extrapiramidális mellékhatások kialakulását. Az ilyen típusú receptorok blokádjának további klinikai megnyilvánulásai a neuroleptikumok fájdalomcsillapító és hányáscsillapító hatása (hányinger, hányás csökkenése a hányásközpont elnyomása következtében), valamint a növekedési hormon tartalmának csökkenése és a prolaktin termelésének növekedése (neuroendokrin mellékhatások, beleértve a galaktorrheát és a menstruációs zavarokat). A nigrostriatális D2 receptorok hosszú távú blokádja túlérzékenységük megjelenéséhez vezet, ami felelős a tardív diszkinéziák és a "túlérzékenységi pszichózisok" kialakulásáért. A preszinaptikus D3 és D4 receptorok blokádjának valószínűsíthető klinikai megnyilvánulásai főként a neuroleptikumok stimuláló hatásával kapcsolatosak. A nigrostriatális és mezolimbokortikális területeken található receptorok részleges blokádja miatt az aktiváló és incizív (erős, nagy aktivitású) neuroleptikumok kis dózisban stimulálhatják, nagy dózisban pedig gátolhatják a dopaminerg transzmissziót.
Az utóbbi években az agy szerotonerg rendszereinek, beleértve a szerotoninreceptorok működését is, jelentősen megnőtt az érdeklődés. A helyzet az, hogy az agy különböző részein a szerotonerg rendszer moduláló hatással van a dopaminerg struktúrákra. Különösen a mezokortikális régióban gátolja a szerotonin a dopamin felszabadulását, és ennek megfelelően a posztszinaptikus 5-HT receptorok blokádja a dopamintartalom növekedéséhez vezet. Mint ismert, a skizofrénia negatív tüneteinek kialakulása az agykéreg prefrontális struktúráiban található dopamin neuronok alulműködésével jár. Jelenleg körülbelül 15 típusú központi 5-HT receptor ismert. Kísérletileg felfedezték, hogy a neuroleptikumok főként az első három típusú 5-HT receptorokhoz kötődnek.
Ezek a gyógyszerek főként stimuláló (agonista) hatást fejtenek ki az 5-HT1a receptorokra. Valószínűsíthető klinikai következmények: fokozott antipszichotikus aktivitás, a kognitív zavarok súlyosságának csökkenése, a negatív tünetek korrigálása, antidepresszáns hatás és az extrapiramidális mellékhatások előfordulásának csökkenése.
A neuroleptikumok 5-HT2 receptorokra, különösen az 5-HT2a altípusokra gyakorolt hatása kiemelkedő jelentőségű. Ezek főként az agykéregben helyezkednek el, és érzékenységük fokozott a skizofréniában szenvedő betegeknél. Az új generációs neuroleptikumok azon képessége, hogy csökkentsék a negatív tünetek súlyosságát, javítsák a kognitív funkciókat, szabályozzák az alvást a lassú hullámú (D-hullámú) alvási szakaszok teljes időtartamának növelésével, csökkentsék az agressziót, valamint enyhítsék a depressziós tüneteket és a migrénszerű (agyi érrendszeri rendellenességekből eredő) fejfájást, az 5-HT2a receptorok blokádjával jár. Másrészt az 5-HT2a receptorok blokádjával vérnyomáscsökkentő hatások és ejakulációs zavarok jelentkezhetnek férfiaknál.
Úgy vélik, hogy a neuroleptikumok 5-HT2c receptorokra gyakorolt hatása nyugtató (anxiolitikus) hatást, fokozott étvágyat (testsúlynövekedéssel együtt) és a prolaktin termelés csökkenését okozza.
Az 5-HT3 receptorok túlnyomórészt a limbikus régióban helyezkednek el, és amikor blokkolják őket, először a hányingercsillapító hatás alakul ki, és az antipszichotikus és szorongásoldó hatások is fokozódnak.
A Parkinson-kórhoz hasonló tünetek előfordulása a gyógyszer muszkarin kolinerg receptorokra gyakorolt blokkoló erejétől is függ. A kolinolitikus és a dopamin-blokkoló hatások bizonyos mértékig kölcsönös kapcsolatban állnak. Ismert például, hogy a nigrostriatális régióban a D2 receptorok gátolják az acetilkolin felszabadulását. Amikor a nigrostriatális régióban a D2 receptorok több mint 75%-a blokkolódik, az egyensúly a kolinerg rendszer javára felborul. Ez az oka az antikolinerg gyógyszerek (korrektorok) korrekciós hatásának a neuroleptikus extrapiramidális mellékhatásokra. A klórprotixén, a klozapin és az olanzapin nagy affinitással rendelkezik a muszkarin receptorokhoz, és gyakorlatilag nem okoznak extrapiramidális mellékhatásokat, mivel egyszerre blokkolják a kolinerg és dopaminerg receptorokat. A haloperidol és a piperazin-fenotiazin-származékok kifejezett hatást gyakorolnak a dopamin receptorokra, de nagyon gyenge hatást gyakorolnak a kolinreceptorokra. Ez annak köszönhető, hogy képesek kifejezett extrapiramidális mellékhatásokat okozni, amelyek nagyon nagy dózisok alkalmazásakor csökkennek, amikor a kolinolitikus hatás észrevehetővé válik. A nigrostriatális régió D2 receptoraira gyakorolt dopamin-blokkoló hatás csökkentése és az extrapiramidális mellékhatások kiegyenlítése mellett az erős kolinerg hatás a kognitív funkciók romlását okozhatja, beleértve a memóriazavarokat, valamint a perifériás mellékhatásokat (száraz nyálkahártyák, károsodott vizuális akkomodáció, székrekedés, vizeletretenció, zavartság stb.). A neuroleptikumok meglehetősen erős blokkoló hatást fejtenek ki az I. típusú hisztaminreceptorokra, ami elsősorban a szedatív hatás súlyosságával, valamint a megnövekedett étvágy miatti testsúlynövekedéssel jár. A neuroleptikumok antiallergiás és viszketéscsillapító hatása is összefüggésben áll antihisztamin tulajdonságaikkal.
A dopaminblokkoló, antiszerotonerg, kolinolitikus és antihisztamin hatások mellett a legtöbb neuroleptikum adrenolitikus tulajdonságokkal is rendelkezik, azaz mind a központi, mind a perifériás a1-adrenoreceptorokat blokkolja. Az adrenoblokkolók, mint például a klórpromazin és a klórprotixén, kifejezett szedatív hatásúak. Ezenkívül ezen gyógyszerek blokkoló hatása neurovegetatív mellékhatásokat (artériás hipotenzió, tachycardia stb.) okozhat, valamint fokozhatja az adrenoblokkolók vérnyomáscsökkentő hatását.
Számos szerző munkái szolgáltatnak adatokat az egyes neuroleptikumok különböző típusú neuroreceptorokhoz való kötődési erősségéről (affinitásáról).
Neurokémiai hatásprofiljuk alapján a klinikai gyakorlatban túlnyomórészt alkalmazott tipikus és atípusos antipszichotikumok feltételesen hat csoportba sorolhatók.
Az első csoportot a benzamid és butirofenon származékok csoportjából származó szelektív D2 és D4 receptor blokkolók (szulpirid, amiszudprid, haloperidol stb.) alkotják. Kis dózisokban, főként a preszinaptikus D4 receptorok blokkolása miatt, aktiválják az idegimpulzusok dopaminerg transzmisszióját, és stimuláló (disinhibitoros) hatást fejtenek ki, nagy dózisokban az agy minden területén blokkolják a D2 receptorokat, ami klinikailag kifejezett antipszichotikus hatásban, valamint extrapiramidális és endokrin (prolaktinémia miatt) mellékhatásokban nyilvánul meg.
A második csoportba tartoznak a nagy aktivitású D2-receptor blokkolók, valamint az 5-HT2a- és 5-HT1a-receptorokat gyengén vagy mérsékelten blokkoló gyógyszerek (flupentixol, flufenazin, zuklopentixol stb.), azaz főként a fenotiazin piperazin-származékai vagy a sztereokémiai szerkezetükben hozzájuk közel álló tioxantének. Az első csoport gyógyszereihez hasonlóan ezek a neuroleptikumok elsősorban kifejezett antipszichotikus (incizív) hatással rendelkeznek, emellett extrapiramidális légzési zavarokat és prolaktinémiát is okoznak. Kis dózisokban mérsékelten aktiváló (pszichostimuláló) hatást fejtenek ki.
A harmadik csoportot a polivalens szedatív neuroleptikumok alkotják, amelyek a legtöbb neuroreceptort differenciálatlanul blokkolják. Ezek a gyógyszerek egyértelműen kifejezett blokkoló hatással vannak a dopaminreceptorokra, és erős adrenolitikus és kolinolitikus hatásokat is okoznak. Ide tartozik a legtöbb szedatív neuroleptikum, elsősorban a fenotiazin alifás és piperidin-származékai, valamint a sztereokémiai szerkezetükben hozzájuk közel álló tioxantének (klórpromazin, levomepromazin, klórprotixén stb.). Ezen gyógyszerek pszichotróp aktivitásának spektrumát elsősorban a kifejezett primer szedatív hatás uralja, amely az alkalmazott dózistól függetlenül kialakul, valamint a mérsékelt antipszichotikus hatás. Ezenkívül a kifejezett antikolinerg hatásuk miatt az ebbe a csoportba tartozó gyógyszerek gyenge vagy közepes extrapiramidális és neuroendokrin mellékhatásokat okoznak, de gyakran ortosztatikus hipotenzió és más autonóm reakciók kialakulásához vezetnek az α1-adrenerg receptorok kifejezett blokádja miatt.
A negyedik csoportba azok a neuroleptikumok tartoznak, amelyek kiegyensúlyozottan blokkolják a D2- és 5-HT2a-receptorokat, azaz azonos mértékben (utóbbit valamivel nagyobb mértékben), és mérsékelten az α1-adrenoreceptorokat. Ez a csoport az atipikus antipszichotikumok (risperidon, ziprasidon, sertindol) új generációs képviselőit foglalja magában, amelyek eltérő kémiai szerkezettel rendelkeznek. A neurokémiai hatásmechanizmus elsősorban az agy mezolimbikus és mezokortikális területeire gyakorolt szelektív hatásukat határozza meg. A kifejezett antipszichotikus hatás, az extrapiramidális mellékhatások hiánya vagy gyenge kifejeződése (terápiás dózisok alkalmazása esetén), a gyenge vagy közepes prolaktinémia és a mérsékelt adrenolitikus tulajdonságok (hipotenzív reakciók) mellett ez a neuroleptikumcsoport képes a negatív tünetek korrigálására az agykéreg dopaminerg transzmissziójának közvetett stimulálásával.
Az ötödik csoportot a triciklusos dibenzodiazepin vagy hasonló szerkezetű (klozapin, olanzapin és kvetiapin) polivalens atipikus antipszichotikumok alkotják. A harmadik csoport gyógyszereihez hasonlóan ezek is differenciálatlanul blokkolják a legtöbb neuroreceptort. Az 5-HT2a receptorok azonban erősebben blokkolódnak, mint a D2 és D4 receptorok, különösen a nigrostriatális régióban találhatók. Ez határozza meg az extrapiramidális hatás tényleges hiányát vagy gyengeségét, valamint a fokozott prolaktintermeléssel járó neuroendokrin mellékhatások hiányát, amelyek határozott antipszichotikus hatással és a negatív tünetek súlyosságának csökkentésére való képességgel rendelkeznek. Ezenkívül a csoport összes gyógyszere kifejezett adrenolitikus és antihisztamin tulajdonságokkal rendelkezik, ami meghatározza a szedatív és vérnyomáscsökkentő hatásukat. A klozapin és az olanzapin szintén meglehetősen kifejezett blokkoló hatással bír a muszkarin receptorokra, és kolinolitikus mellékhatások kialakulásához vezet.
Így a posztszinaptikus dopaminerg receptorok blokkolásának képessége a dopamin szintézisének és metabolizmusának kompenzáló növekedésével az egyetlen közös biokémiai tulajdonság az ezekben a csoportokban figyelembe vett összes neuroleptikum esetében.
A hatodik csoportba tartozik az egyetlen atipikus antipszichotikum, az aripiprazol, amely viszonylag nemrég jelent meg a hazai pszichofarmakológiai piacon. Ez a gyógyszer a D2-dopamin receptorok parciális agonistája, és hiperdopaminerg állapotban funkcionális antagonistaként, hipodopaminerg profilban pedig funkcionális agonistaként működik. Az aripiprazol ilyen egyedi receptorprofilja lehetővé teszi az extrapiramidális rendellenességek és a hiperprolaktinémia kockázatának csökkentését alkalmazása során. Ezenkívül az aripiprazol az 5-HT1a receptorok parciális agonistájaként, ugyanakkor az 5-HT2a receptorok antagonistájaként is működik. Feltételezhető, hogy a receptorokkal való ilyen kölcsönhatás a szerotonin és a dopamin rendszerek általánosságban kiegyensúlyozott működéséhez vezet, így az aripiprazol hatásmechanizmusa a dopamin-szerotonin rendszer stabilizálásaként írható le.
Így a neuroleptikumok neurokémiai hatásmechanizmusaival kapcsolatos jelenlegi ismeretek lehetővé teszik számunkra, hogy új, patogenetikailag megalapozottabb farmakodinamikai osztályozást javasoljunk e pszichotróp gyógyszercsoport számára. Ezen osztályozás használata lehetővé teszi számunkra, hogy nagymértékben megjósoljuk egy adott gyógyszer pszichotróp aktivitásának spektrumát, toleranciáját és valószínűsíthető gyógyszerkölcsönhatásait. Más szóval, egy gyógyszer neurokémiai aktivitásának jellemzői nagymértékben meghatározzák klinikai aktivitásának jellemzőit, amelyeket egy adott antipszichotikus gyógyszer kiválasztásakor kell figyelembe venni egy adott beteg számára.
Bármely neuroleptikum globális antipszichotikus hatásának hatékonyságát az úgynevezett klórpromazin-ekvivalens segítségével becsülik meg, amelyet 1-nek vesznek. Például a haloperidol klórpromazin-ekvivalense = 50. Ez azt jelenti, hogy 1 mg haloperidol antipszichotikus hatékonysága összehasonlítható 50 mg klórpromazinnal. Ezen mutató alapján kidolgoztak egy osztályozást, amely a magas (klórpromazin-ekvivalens> 10,0), közepes (klórpromazin-ekvivalens = 1,0-10,0) és alacsony (klórpromazin-ekvivalens = 1,0) antipszichotikus aktivitású neuroleptikumok elosztását biztosítja, amelyet szabadalomnak neveznek. A tipikus neuroleptikumokat (első generációs antipszichotikumokat) közel fél évszázada széles körben alkalmazzák a klinikai pszichofarmakoterápiában. Terápiás aktivitásuk spektruma a következőket foglalja magában:
- globális antipszichotikus hatás, amely a pszichózis különböző megnyilvánulásainak egyenletes és differenciált csökkentésére való képesség formájában jelentkezik:
- elsődleges nyugtató (gátló) hatás - a gyógyszerek azon képessége, hogy gyorsan enyhítsék a pszichomotoros agitációt;
- szelektív, szelektív antipszichotikus hatás, amely az egyes tünetek befolyásolásának képességében nyilvánul meg: delírium, hallucinációk, a hajtóerők gátlásának megszűnése stb.;
- aktiváló (disinhibitoros, disinhibitoros, antiautista) neurotrop hatás, amely extrapiramidális tünetek kialakulásában nyilvánul meg;
- szomatotróp hatás neuroendokrin és vegetatív mellékhatások kialakulásának formájában;
- depresszáns hatás, amelyet egyes antipszichotikumok depressziós tünetek kiváltására való képességében fejeznek ki.
Az első generációs antipszichotikumok hatékonysága nemcsak a pszichotikus rendellenességek, hanem a határeseti pszichiátrián belüli rendellenességek kezelésében is sokszor bizonyított és vitathatatlan. Ezért a terápia magas mellékhatásainak gyakorisága ellenére, amikor felírják őket, továbbra is alkalmazzák az orvosi gyakorlatban.
Atipikus antipszichotikumok
A modern irányelvek adatokat tartalmaznak a második generációs antipszichotikumok farmakoterápiában való alkalmazásának előnyeiről. Az "atipikus" kifejezés (szinonimája - második generációs antipszichotikumok) feltételes, és elsősorban az új generáció megjelölésének kényelme érdekében használják. A hagyományos neuroleptikumokhoz képest az ebbe a csoportba tartozó gyógyszerek hatékonyabbak a negatív, affektív és kognitív zavarok korrigálásában, ami jobb tolerálhatósággal és az extrapiramidális tünetek alacsonyabb kockázatával párosul. Az atipikus antipszichotikumok sorozatából származó egyik vagy másik gyógyszer terápiás hatásának jellegében mutatkozó különbségeket, akárcsak a tipikus neuroleptikumok csoportjában, az egyedi farmakológiai hatásprofiljuk magyarázza.
Az atipikus antipszichotikumokkal végzett pszichofarmakoterápia lehetőségeinek tisztázása érdekében célszerű az Oroszországban regisztrált e csoportba tartozó gyógyszerekre összpontosítani.
 [ 28 ], [ 29 ], [ 30 ], [ 31 ], [ 32 ], [ 33 ]
[ 28 ], [ 29 ], [ 30 ], [ 31 ], [ 32 ], [ 33 ]
Klozapin (dibenzodiazepin)
Az atipikus antipszichotikumok csoportjának alapítója. A klozapin hatásmechanizmusát a D2 receptorok enyhe blokkolása jellemzi, egyidejűleg magas antagonizmussal az 5-HT2a receptorokkal, az α1, α2-adrenerg és H1-hisztamin receptorokkal szemben. Hatékony antipszichotikumnak bizonyult más antipszichotikumokkal (a tartalék csoport gyógyszere) szembeni rezisztencia esetén, és krónikus mánia, pszichotikus agitáció, agresszió kezelésére is javallt. A hazai gyakorlatban a klozapint gyakran írják fel szedáció elérésére és altatóként pszichotikus betegeknél. Fel kell ismerni, hogy a klozapin ilyen jellegű alkalmazása nem felel meg a terápiás alkalmazás fő indikációs profiljának. Valószínűleg felül kell vizsgálni az antipszichotikumhoz, mint másodlagos jelentőségű gyógyszerhez való hozzáállást, mivel ma ez az egyetlen olyan gyógyszer, amely bizonyítottan hatékony a rezisztens betegeknél.
A klozapin, a tipikus neuroleptikumokkal ellentétben, nem okoz súlyos extrapiramidális zavarokat a fent említett alacsony O2 receptor affinitás miatt. Az is kiderült, hogy késői disztónia és súlyos akathisia kezelésére is alkalmazható. Az NMS kialakulásának alacsony kockázata miatt a klozapin választott gyógyszernek tekinthető azoknál a betegeknél, akik korábban már szenvedtek ettől a szövődménytől.
A klozapin-terápia során azonban számos súlyos mellékhatás alakulhat ki. Ezek közül a legveszélyesebb (még kis dózisok felírása esetén is) az agranulocitózis, amely a betegek 0,5-1,0%-ánál fordul elő. A gyógyszer alkalmazása során előforduló egyéb fontos mellékhatások közé tartozik az álmosság, a fokozott nyáltermelés és a testsúlygyarapodás, amely gyakran már emelkedett a klozapin felírásakor a korábbi antipszichotikus terápia hatása alatt. Figyelmet kell fordítani a tachycardia, az artériás hipotenzió és az epilepsziás rohamok kialakulásának lehetőségére is a szedése során. A rohamok valószínűsége az adagtól függ. Kockázatuk jelentősen megnő, ha a klozapin adagja meghaladja a napi 600 mg-ot. A rohamok kialakulása nem ellenjavallata a gyógyszer további alkalmazásának, de az adag felére csökkentését és görcsoldók, például valproinsav felírását igényli. A klozapin-kezelés mellékhatásainak megelőzése magában foglalja a fehérvérsejtszám, valamint az EKG és az endokrin paraméterek gondos monitorozását.
A klozapin túladagolása tudatzavart okozhat, akár kóma kialakulásáig, valamint kolinolitikus hatással összefüggő tüneteket (tachycardia, delírium), epilepsziás rohamokat, légzésdepressziót, extrapiramidális szindrómákat. Halálos kimenetelű lehet a gyógyszer 2500 mg-ot meghaladó adagjának bevétele.
 [ 34 ], [ 35 ], [ 36 ], [ 37 ], [ 38 ], [ 39 ], [ 40 ], [ 41 ]
[ 34 ], [ 35 ], [ 36 ], [ 37 ], [ 38 ], [ 39 ], [ 40 ], [ 41 ]
Riszperidon
Egy benzizoxazol-származék, amely nagy affinitással rendelkezik a szerotonin és a dopamin Dj receptorok iránt, és domináns hatással van a szerotonin rendszerre. A gyógyszer széles körű alkalmazási javallatokkal rendelkezik, beleértve az exacerbációk enyhítését, a relapszus elleni kezelést, az első pszichotikus epizód terápiáját és a skizofrénia negatív tüneteinek korrekcióját. A gyógyszerről kimutatták, hogy javítja a kognitív funkciókat skizofréniában szenvedő betegeknél. Előzetes adatok szerint a riszperidon csökkenti a szkizofréniában szenvedő betegek komorbid affektív tüneteit is, és a bipoláris affektív zavarok kezelésében választott gyógyszer lehet.
A riszperidon-terápia mellékhatásai, különösen az extrapiramidális zavarok, dózisfüggőek, és gyakrabban fordulnak elő napi 6 mg-ot meghaladó dózisok esetén. Egyéb mellékhatások közé tartozik a hányinger, hányás, szorongás, álmosság és a megnövekedett szérum prolaktinszint. A riszperidon hosszú távú alkalmazása súlygyarapodáshoz és 2-es típusú cukorbetegség kialakulásához vezethet, de kisebb valószínűséggel, mint a klozapin, az olanzapin.
A túladagolás aluszékonyságot, epilepsziás görcsrohamokat, a QT-intervallum megnyúlását és a QRS-komplexus kiszélesedését, valamint artériás hipotenziót okozhat. Leírtak halálos kimenetelű eseteket a riszperidon túladagolása miatt.
A gyógyszer kétségtelen előnye a folyékony és gyorsan oldódó (szublingvális) formák elérhetősége, amelyek alkalmazása felgyorsítja a gyógyszer bejutását a beteg szervezetébe, és megkönnyíti a bevitelének kontrollját. A gyógyszernek van egy hosszan tartó formája is - por intramuszkuláris beadásra szánt szuszpenzió előállítására (mikroszférákban lévő consta-risperidon). Skizofréniában szenvedő betegek fenntartó kezelésére ajánlott, különösen a rosszul együttműködő betegek esetében. Figyelembe kell venni azt a tényt, hogy a gyógyszernek körülbelül három hétre van szüksége a véráramba jutáshoz, ezért a consta-risperidonnal végzett terápia megkezdésekor a betegnek az első injekció beadása után legalább 3 hétig kell szednie a riszperidon orális formáját.
Olanzapin
Farmakológiai hatás tekintetében közel áll a klozapinhoz, mivel pleiomorf receptorprofillal rendelkezik, jelentős affinitással a szerotonin, muszkarin, α1-adrenerg és hisztamin receptorok iránt. Az olanzapin terápiás aktivitása hasonló tulajdonságokkal rendelkezik, mint a klozapin és a riszperidon hatékonysága a skizofrénia pozitív, negatív és depressziós tüneteire gyakorolt hatás tekintetében. Ugyanakkor adatokat kaptak az olanzapin nagyobb hatékonyságáról más atipikus antipszichotikumokhoz képest az első pszichotikus epizóddal rendelkező betegeknél és a kognitív működési mutatók korrekciójában. Figyelembe kell venni, hogy a gyógyszer tabletta formájával történő terápia kezdetén gyors gátláscsökkentő hatás jelentkezhet fokozott pszichomotoros agitációval és szorongással. Ezért a súlyos pszichomotoros agitációval járó rohamok kezelésében a gyógyszer injekciós formájának alkalmazása javasolt.
Az olanzapin ritkán okoz extrapiramidális zavarokat vagy tardív diszkinéziát, és a leggyakoribb mellékhatások az anyagcserezavarok és a súlygyarapodás. Megállapították, hogy az olanzapint szedő betegeknél gyakran emelkedett koleszterinszint, plazmalipidek és 2-es típusú cukorbetegségre való hajlam tapasztalható, de ezek a hatások ugyanolyan gyakoriak voltak az olanzapint és a klozapint is kapó betegeknél. Ugyanakkor olyan adatokat is kaptak, amelyek azt mutatják, hogy a súlygyarapodás korrelál az olanzapinra adott pozitív válasszal (azaz a terápia fontos prognosztikai indikátora), és csak a kezelés során túlsúlyos betegek 20-30%-ánál alakul ki elhízás.
A túladagolás szedációt, toxikus antikolinerg hatásokat, epilepsziás görcsöket és artériás hipotenziót okozhat. Jelenleg nincsenek meggyőző adatok a túladagolás okozta halálozás kockázatának felmérésére.
Kvetiapin
Dibenzotiazepin vegyületként osztályozzák. Receptorprofilja nagyrészt hasonló a klozapinéhoz. A kvetiapin D2 receptorokhoz való kötődési szintje alacsony (kevesebb, mint 50%) és rövid távú, még nagy dózisok alkalmazása esetén is. A gyógyszer hatékony a skizofrénia pozitív, negatív és általános tüneteinek kezelésében. Bizonyítékok vannak sikeres alkalmazására mind a terápiával szembeni nagyfokú rezisztencia esetén, mind a betegek kognitív funkcióinak javítására, ami jogosítja fel arra, hogy első vonalbeli antipszichotikumként ajánlják a skizofrénia fenntartó terápiájában. Végül a kvetiapin mérsékelt antidepresszáns, aktiváló hatással rendelkezik. Ezért depressziós-téveszmés rohamok és a senesto-hypochondriás kör zavarainak kezelésében javallt.
A kvetiapin megállapított magas timotrop aktivitása magyarázza azt a tényt, hogy a depressziós rendellenességek enyhítésére és másodlagos megelőzésére szolgáló eszközként regisztrálták. Az I. és II. típusú bipoláris zavarok mániás epizódjainak kezelésére a kvetiapint kiegészítő szerként alkalmazzák. Az injekciós formák hiánya némileg korlátozza alkalmazását izgatottságban és agresszív viselkedésben szenvedő betegeknél.
A kvetiapin jól tolerálható, gyakorlatilag nem okoz extrapiramidális szindrómákat, kivéve azokat az eseteket, amikor maximális dózisokat alkalmaznak. A kvetiapin nem okoz hiperprolaktinémiát, ritkábban, mint az olanzapin és a klozapin, súlygyarapodáshoz és a glükóztolerancia károsodásához vezet.
Ziprasidon
Egyedi receptor aktivitási profillal rendelkezik. Mivel az 5HT2a és D2 receptorok erős antagonistája, a szerotonin és a noradrenalin újrafelvételének aktív inhibitora is. Klinikai vizsgálatok kimutatták, hogy a ziprasidon jelentősen jobb hatást gyakorol a pszichotikus tünetekre és az agresszió megnyilvánulásaira a haloperidolhoz képest. Adatok vannak a ziprasidon pozitív hatásáról a skizofréniában szenvedő betegek kognitív funkcióira, valamint a komorbid affektív tünetekre és a szociális működés mutatóira is. A ziprasidon általában jól tolerálható, és nagyon ritkán okoz extrapiramidális szindrómákat, súlygyarapodást és anyagcserezavarokat. Gyakrabban fordul elő a QT-intervallum 460 ms feletti megnyúlása, ezért a gyógyszert szedő betegeknél célszerű EKG-vizsgálatot végezni mind a gyógyszer felírása előtt, mind a kezelés alatt kontrollmonitorozást végezni. Különös figyelmet kell fordítani az egyidejű terápiára (antiaritmiás gyógyszerek szedése), amely súlyosbíthatja a QT-intervallum megnyúlását, és szívritmuszavar, kamrafibrilláció kialakulásához vezethet.
Sertindol
Fenilindol-származékokhoz tartozik. Nagyfokú funkcionális antagonizmust mutat a D2-, szerotonin- (különösen az 5-HT2a-receptorok) és az α1-adrenerg receptorokkal szemben. Elektroneurokémiai vizsgálatok szerint a szertindol szelektíven gátolja a dopaminreceptorokat a ventrális szegmentális régióban. Ez a szelektivitás minden valószínűség szerint alacsony extrapiramidális szindrómák és hiperprolaktinémia kockázatát biztosítja a gyógyszer alkalmazása során. Összehasonlító vizsgálatok eredményei kimutatták, hogy a szertindol antipszichotikus aktivitás tekintetében összehasonlítható a haloperidollal. A gyógyszer kifejezett diszinhibitor hatást fejt ki negatív és depressziós tünetekkel küzdő betegeknél, ami meghaladja a rispolept hasonló hatását. Vannak bizonyítékok a szertindol hatékonyságára a szkizofréniában szenvedő betegek kognitív károsodásának korrekciójában is. A szertindolt a betegek általában jól tolerálják, ritkán okoz szedációt, ezért helyettesítő gyógyszerként ajánlott, ha más modern antipszichotikumokkal végzett terápia során mellékhatások jelentkeznek.
A súlyos mellékhatások közé tartozik a gyógyszer QT-intervallum megnyúlása, ami szívritmuszavarhoz vezethet. A forgalomba hozatalt követő vizsgálatok elemzése során világossá vált, hogy a szertindol szívprofilja nem különbözik más új generációs antipszichotikumokétól.
Aripiprazol
Antipszichotikus aktivitással rendelkezik, amely összehasonlítható más atipikus szerekkel, de nagyobb hatással van a skizofréniában szenvedő betegek kognitív működésének paramétereire. A gyógyszer fent említett egyedi farmakológiai hatása - a D2 receptorok részleges agonistája - lehetővé teszi az extrapiramidális szindrómák és a hiperprolaktinémia kockázatának csökkentését alkalmazása során.
 [ 42 ], [ 43 ], [ 44 ], [ 45 ], [ 46 ], [ 47 ]
[ 42 ], [ 43 ], [ 44 ], [ 45 ], [ 46 ], [ 47 ]
Amisulprid
A szubsztituált benzamidok osztályába tartozik. A gyógyszer szelektíven kötődik a D2 és D3 dopaminerg receptorok altípusaihoz, nincs affinitása a D1, D4 és D5 altípusokhoz, valamint a szerotonin, H1-hisztamin, α1-adrenerg és kolinerg receptorokhoz. Nagy dózisokban blokkolja a posztszinaptikus D2 receptorokat. Alacsony dózisokban diszinhibitoros hatása a preszinaptikus D2, D3 receptorok blokádja miatt jelentkezik, aminek köszönhetően alkalmazása a negatív tünetek kezelésében is hatékony, bár nem kombinált D2 receptorok és szerotonin receptorok antagonistája. Számos vizsgálat eredményei a gyógyszer kifejezett antipszichotikus aktivitását mutatják nagy dózisokban alkalmazva, ami meghaladja a hagyományos gyógyszerekét.
 [ 48 ], [ 49 ], [ 50 ], [ 51 ], [ 52 ], [ 53 ], [ 54 ], [ 55 ]
[ 48 ], [ 49 ], [ 50 ], [ 51 ], [ 52 ], [ 53 ], [ 54 ], [ 55 ]
Az antipszichotikus terápia mellékhatásai
A táblázat az atipikus antipszichotikumok főbb mellékhatásait sorolja fel.
Készítmény |
Extrapiramidális |
Vezetési zavar az EKG-n |
Anyagcserezavarok (súlygyarapodás, megnövekedett glükóz-, koleszterin- és trigliceridszint a vérben) |
||
Klozapin |
. |
++ |
++ |
++- |
|
Riszperidon |
++ |
+/- |
++ |
+/- |
|
Olanzapin |
+ |
+/- |
+++ |
++ |
+++ |
Kvetiapin |
+/- |
+ |
+/- |
--- |
|
Ziprasidon |
+ |
++ |
+/- |
+/- |
+/- |
Sertindol |
++ |
-- |
+/- |
-- |
|
Ariliprazol |
-- |
--- |
+/- |
-- |
-- |
Amisulprid |
++ |
+/- |
|||
Megjegyzés. Mellékhatások súlyossága: "+++" - magas; "++" - átlagos; "+" - alacsony; "+/-" - kétes; "-" - nincs.
Extrapiramidális szindrómák
Az atipikus antipszichotikumok egyik fő jellemzője a hagyományosakkal ellentétben az extrapiramidális szindrómák kiváltására való alacsony képességük, ami áttörést jelentett a skizofrénia fenntartó farmakoterápiájában. Azonban, amint az a táblázatban szereplő adatokból is következik, az e sorozat egyes gyógyszereinek (risperidon, amiszulprid) alkalmazásakor ilyen tünetek jelentkezhetnek, amelyek különös figyelmet igényelnek felírásukkor.
 [ 3 ], [ 4 ], [ 5 ], [ 6 ], [ 7 ], [ 8 ], [ 9 ], [ 10 ]
[ 3 ], [ 4 ], [ 5 ], [ 6 ], [ 7 ], [ 8 ], [ 9 ], [ 10 ]
EKG-eltérések
A szívvel kapcsolatos mellékhatások kialakulásának lehetősége komoly problémát jelent egyes modern antipszichotikumok terápiás alkalmazásakor. Ezekben az esetekben a QT-intervallum megnyúlásáról beszélünk, ami aritmia kialakulásához vezethet. A vezetési zavarok, elsősorban a QT-intervallum megnyúlása, leggyakrabban klozapinnal, szertindollal és ziprasidonnal végzett kezelés során figyelhetők meg. A fent említett gyógyszerekkel végzett terápia során a bradycardia, a pitvar-kamrai blokk és a hipotireózis formájában jelentkező egyidejű patológia hozzájárulhat ennek a szövődménynek a kialakulásához. Jelenleg az atipikus antipszichotikumokkal fenntartó terápiában részesülő betegeknél körülbelül 3 havonta egyszer ajánlott EKG-monitorozást végezni.
 [ 11 ], [ 12 ], [ 13 ], [ 14 ], [ 15 ]
[ 11 ], [ 12 ], [ 13 ], [ 14 ], [ 15 ]
Endokrin rendellenességek
Jelenleg a legnagyobb aggodalmat az atipikus antipszichotikumok súlygyarapodást okozó képessége okozza. A megnövekedett testsúly, a vércukor- és trigliceridszint anyagcserezavarokhoz és a 2-es típusú cukorbetegség kialakulásához vezethet. A klozapinnal és olanzapinnal végzett terápia során különös óvatosságra és a biokémiai paraméterek heti monitorozására van szükség. J. Geddes és munkatársai (2000), PB Jones, PF Buckley (2006) szerint helyénvalónak kell tekinteni a betegek alapos vizsgálatát, mielőtt egy adott modern generációs antipszichotikumot felírnának nekik, mivel ismert, hogy az anyagcserezavarok gyakrabban fordulnak elő azoknál a betegeknél, akiknél a kezelés megkezdése előtt örökletes hajlam, túlsúly, lipidspektrum-zavarok és hiperglikémia állt fenn. A PB Jones, PF Buckley (2006) által javasolt monitorozási algoritmus több pontot is tartalmaz.
- Kórtörténet és családi tényezők gyűjtése az anyagcserezavarok kockázatával kapcsolatban.
- A kezelés megkezdése előtt regisztrálni kell a testtömegindexet, az EKG-t, a vérnyomást és a pulzust.
- Laboratóriumi adatok (glükóz, lipidprofil, koleszterin) gyűjtése a terápia megkezdése előtt.
- A kezelés során rendszeresen ellenőrizni kell a testtömegindexet és az életjeleket.
- Laboratóriumi adatok monitorozása a kezelés során.
Az antipszichotikus terápia során a hiperprolaktinémia előfordulása a hipotalamuszban található dopaminreceptorok központi blokádjának köszönhető, ami prolaktin felszabadulásához vezet az agyalapi mirigy elülső lebenyéből. A hiperprolaktinémia leggyakrabban olanzapinnal, riszperidonnal és amiszulpriddal történő kezelés során fordul elő.
 [ 16 ], [ 17 ], [ 18 ], [ 19 ], [ 20 ]
[ 16 ], [ 17 ], [ 18 ], [ 19 ], [ 20 ]
Agranulocitózis
Az antipszichotikus terápia egy másik súlyos szövődménye. Klozapinnal és olanzapinnal végzett kezelés során figyelhető meg. J. Geddes és munkatársai (2000) szerint a betegek 1-2%-ánál, akik ezeket a gyógyszereket szedik, az első 3 hónapban diagnosztizálták. E tekintetben a terápia első 18 hetében ezeket a gyógyszereket szedő betegeknél heti vérvizsgálat ajánlott, majd ezt követően havi ellenőrzés. Kimutatták, hogy a fent említett neuroleptikumok adagjának csökkentésekor a klinikai vérvizsgálat normalizálódik. Ugyanakkor fel kell ismerni, hogy a mai napig nincs egyértelmű stratégia azoknak a betegeknek, akiknél a fent említett, anyagcserezavarokkal összefüggő mellékhatások jelentkeznek. Leggyakrabban az egyik atipikus antipszichotikumot egy másik váltja fel. Egy másik ígéretes irány a speciális korrekciós terápia kijelölése, különösen a bromokriptin alkalmazása a hiperprolaktinémia korrigálására. Az ideális helyzet az, amikor az ilyen rendellenességekben szenvedő beteg ellátása belgyógyászok, különösen endokrinológusok, kardiológusok és más szakemberek időszakos bevonásával történik.
Összefoglalva, meg kell jegyezni, hogy ha a betegek mentális, hanem fizikai állapotának felírására és monitorozására vonatkozó megadott algoritmusokat követik, a második generációs gyógyszerek alkalmazása biztonságosabb, mint a tipikus neuroleptikumok.
Számos más antipszichotikum van jelenleg fejlesztés alatt. A következő generációs gyógyszerek valószínűleg eltérő hatásmechanizmussal rendelkeznek majd (például GABAerg profillal), és képesek lesznek befolyásolni a skizofrénia különböző megnyilvánulásait, beleértve magát a deficitzavart is.
Figyelem!
Az információk észlelésének egyszerűsítése érdekében a gyógyszer "Neuroleptikumok vagy antipszichotikumok " gyógyszerre vonatkozó utasítását a gyógyszer orvosi használatára vonatkozó hivatalos utasítások alapján külön formában lefordítják és bemutatják. Használat előtt olvassa el a gyógyszerhez közvetlenül hozzárendelt megjegyzést.
A tájékoztatás tájékoztató jellegű, és nem vezet az öngyógyításhoz. Ennek a gyógyszernek a szükségességét, a kezelés rendjét, módszereit és a gyógyszer adagját kizárólag a kezelőorvos határozza meg. Az öngyógyítás veszélyes az egészségére.

