A cikk orvosi szakértője
Új kiadványok
Az osteoarthritis diagnózisa: mágneses rezonancia képalkotás
Utolsó ellenőrzés: 04.07.2025

Minden iLive-tartalmat orvosi szempontból felülvizsgáltak vagy tényszerűen ellenőriznek, hogy a lehető legtöbb tényszerű pontosságot biztosítsák.
Szigorú beszerzési iránymutatásunk van, és csak a jó hírű média oldalakhoz, az akadémiai kutatóintézetekhez és, ha lehetséges, orvosilag felülvizsgált tanulmányokhoz kapcsolódik. Ne feledje, hogy a zárójelben ([1], [2] stb.) Szereplő számok ezekre a tanulmányokra kattintható linkek.
Ha úgy érzi, hogy a tartalom bármely pontatlan, elavult vagy más módon megkérdőjelezhető, jelölje ki, és nyomja meg a Ctrl + Enter billentyűt.
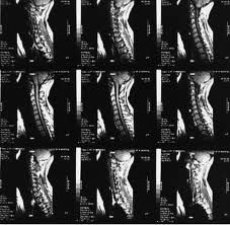
A mágneses rezonancia képalkotás (MRI) az utóbbi években az osteoarthritis non-invazív diagnosztikai módszereinek egyik vezetőjévé vált. Az 1970-es évek óta, amikor a mágneses rezonancia (MR) elveit először alkalmazták az emberi test vizsgálatára, ez az orvosi képalkotási módszer drámaian megváltozott, és továbbra is gyorsan fejlődik.
A technikai berendezéseket és szoftvereket fejlesztik, a képalkotási módszereket és az MR-kontrasztanyagokat is fejlesztik. Ez lehetővé teszi, hogy az MRI alkalmazásának folyamatosan új területeit találják meg. Ha kezdetben az alkalmazása a központi idegrendszer vizsgálatára korlátozódott, ma már az orvostudomány szinte minden területén sikeresen alkalmazzák.
1946-ban a Stanford és a Harvard egyetemek kutatócsoportjai egymástól függetlenül felfedezték a mágneses magrezonancia (NMR) nevű jelenséget. Lényege az volt, hogy egyes atomok magjai mágneses térben, külső elektromágneses tér hatására képesek energiát elnyelni, majd rádiójel formájában kibocsátani. Ezért a felfedezésért F. Bloch és E. Parmel 1952-ben Nobel-díjat kaptak. Az új jelenséget hamarosan biológiai struktúrák spektrális elemzésére (NMR-spektroszkópia) alkalmazták. 1973-ban Paul Rautenburg elsőként bizonyította az NMR-jelek segítségével történő képalkotás lehetőségét. Így jelent meg az NMR-tomográfia. Az élő ember belső szerveinek első NMR-tomogramjait 1982-ben mutatták be a párizsi Nemzetközi Radiológus Kongresszuson.
Két pontosítást kell tenni. Annak ellenére, hogy a módszer az NMR-jelenségen alapul, mágneses rezonanciának (MR) nevezik, elhagyva a „nukleáris” szót. Ezt azért teszik, hogy a betegeknek ne legyenek gondolataik az atommagok bomlásával kapcsolatos radioaktivitásról. És a második körülmény: az MR-tomográfok nem véletlenül vannak „hangolva” protonokra, azaz hidrogénmagokra. Ebből az elemből sok van a szövetekben, és magjai rendelkeznek a legnagyobb mágneses momentummal az összes atommag közül, ami meglehetősen magas MR-jelszintet határoz meg.
Ha 1983-ban még csak néhány klinikai kutatásra alkalmas eszköz volt a világon, akkor 1996 elejére világszerte körülbelül 10 000 tomográf működött. Évente 1000 új eszközt vezetnek be a gyakorlatba. Az MR-tomográfok parkjának több mint 90%-át szupravezető mágnesekkel (0,5-1,5 T) ellátott modellek teszik ki. Érdekes megjegyezni, hogy ha a 80-as évek közepén az MR-tomográfokat gyártó cégeket a "minél nagyobb a térerő, annál jobb" elv vezérelte, az 1,5 T és annál nagyobb térerővel rendelkező modellekre összpontosítva, akkor a 80-as évek végére világossá vált, hogy az alkalmazási területek többségében nincsenek jelentős előnyeik az átlagos térerősségű modellekkel szemben. Ezért az MR tomográfok fő gyártói (General Electric, Siemens, Philips, Toshiba, Picker, Bruker stb.) jelenleg nagy figyelmet fordítanak a közepes, sőt alacsony térerejű modellek gyártására, amelyek kompaktságukban és gazdaságosságukban különböznek a nagy térerejű rendszerektől, kielégítő képminőséggel és jelentősen alacsonyabb költséggel. A nagy térerejű rendszereket elsősorban kutatóközpontokban használják MR spektroszkópiához.
Az MRI módszer alapelve
Az MRI-szkenner fő alkotóelemei: egy szupererős mágnes, egy rádióadó, egy vevő rádiófrekvenciás tekercs, egy számítógép és egy vezérlőpanel. A legtöbb eszköz mágneses mezővel rendelkezik, amelynek mágneses momentuma párhuzamos az emberi test hossztengelyével. A mágneses térerősséget teslában (T) mérik. Klinikai MRI-hez 0,2-1,5 T erősségű mezőket használnak.
Amikor egy beteget erős mágneses térbe helyeznek, minden proton, amely mágneses dipólus, a külső tér irányába fordul (mint egy iránytű, amely a Föld mágneses mezője felé néz). Ezenkívül minden proton mágneses tengelye elkezd forogni a külső mágneses tér iránya körül. Ezt a specifikus forgó mozgást folyamatnak, frekvenciáját pedig rezonanciafrekvenciának nevezzük. Amikor rövid elektromágneses rádiófrekvenciás impulzusok haladnak át a beteg testén, a rádióhullámok mágneses mezeje az összes proton mágneses momentumát a külső tér mágneses momentuma körül forogásra készteti. Ehhez a rádióhullámok frekvenciájának meg kell egyeznie a protonok rezonanciafrekvenciájával. Ezt a jelenséget mágneses rezonanciának nevezik. A mágneses protonok orientációjának megváltoztatásához a protonok és a rádióhullámok mágneses mezőinek rezonálniuk kell, azaz azonos frekvenciával kell rendelkezniük.
A beteg szöveteiben nettó mágneses momentum keletkezik: a szövetek mágnesezettek, és mágnesességük szigorúan párhuzamos a külső mágneses térrel. A mágnesesség arányos a szövet térfogategységére jutó protonok számával. A legtöbb szövetben található hatalmas protonszám (hidrogénmag) azt jelenti, hogy a nettó mágneses momentum elég nagy ahhoz, hogy elektromos áramot indukáljon a betegen kívül elhelyezkedő vevőtekercsben. Ezeket az indukált MR-jeleket használják az MR-kép rekonstruálására.
Az atommag elektronjainak gerjesztett állapotból egyensúlyi állapotba való átmenetének folyamatát spin-rács relaxációs folyamatnak vagy longitudinális relaxációnak nevezzük. Jellemzője a T1 - spin-rács relaxációs idő - az az idő, amely ahhoz szükséges, hogy az atommagok 63%-a egyensúlyi állapotba kerüljön 90°-os gerjesztés után. Megkülönböztetjük a T2 - spin-spin relaxációs időt is.
Több módszer létezik az MR-tomogramok készítésére. Ezek a rádiófrekvenciás impulzusok generálásának sorrendjében és jellegében, valamint az MR-jel elemzésének módszereiben különböznek. A két legelterjedtebb módszer a spin-rács és a spin-echo. A spin-rács elsősorban a T1 relaxációs időt elemzi. A különböző szövetek (az agy szürke- és fehérállománya, az agy-gerincvelői folyadék, a tumorszövet, a porc, az izmok stb.) eltérő T1 relaxációs idejű protonokat tartalmaznak. Az MR-jel intenzitása összefügg a T1 időtartamával: minél rövidebb a T1, annál intenzívebb az MR-jel, és annál világosabb a kép adott területe a TV-monitoron. Az MR-tomogramokon a zsírszövet fehér, ezt követi az agy és a gerincvelő, a sűrű belső szervek, az érfalak és az izmok az MR-jel intenzitásának csökkenő sorrendjében. A levegő, a csontok és a meszesedések gyakorlatilag nem termelnek MR-jelet, ezért feketén jelennek meg. Ezek a T1 relaxációs idő összefüggések teremtik meg az előfeltételeket a normál és a megváltozott szövetek MRI-vizsgálatokon történő megjelenítéséhez.
Egy másik MRI-módszer, az úgynevezett spin-echo, során rádiófrekvenciás impulzusok sorozatát irányítják a betegre, amelyek 90°-kal elforgatják a precesszióban lévő protonokat. Az impulzusok leállása után a válasz MRI-jeleket rögzítik. A válaszjel intenzitása azonban másképp viszonyul a T2 időtartamához: minél rövidebb a T2, annál gyengébb a jel, és ennek következtében annál kisebb a TV-képernyőn megjelenő fényerő. Így a T2 módszerrel készült végső MRI-kép ellentétes a T1 módszerrel készült képpel (mivel a negatív a pozitív ellentéte).
Az MRI tomográfiák jobban ábrázolják a lágy szöveteket, mint a CT-vizsgálatok: az izmokat, a zsírrétegeket, a porcot és az ereket. Egyes készülékek kontrasztanyag befecskendezése nélkül is képesek képet készíteni az erekről (MRI angiográfia). A csontszövet alacsony víztartalma miatt ez utóbbi nem hoz létre árnyékoló hatást, mint a röntgen CT-vizsgálat, azaz nem zavarja például a gerincvelő, a csigolyaközi porckorongok stb. képét. Természetesen a hidrogénatomok nemcsak a vízben találhatók, hanem a csontszövetben is nagyon nagy molekulákban és sűrű szerkezetekben rögzülnek, és nem zavarják az MRI-vizsgálatot.
Az MRI előnyei és hátrányai
Az MRI fő előnyei közé tartozik a nem invazív hatás, az ártalmatlanság (nincs sugárterhelés), a képalkotás háromdimenziós jellege, a mozgó vértől való természetes kontraszt, a csontszövetből származó műtermékek hiánya, a lágy szövetek magas differenciáltsága, valamint az MP spektroszkópia elvégzésének lehetősége in vivo szöveti anyagcsere-vizsgálatokhoz. Az MRI lehetővé teszi az emberi test vékony rétegeinek képalkotását bármely szakaszban - frontális, sagittális, axiális és ferde síkban. Lehetőség van a szervek térfogati képeinek rekonstruálására, a tomogramok felvételének szinkronizálására az elektrokardiogram fogaival.
A fő hátrányok általában a képek készítéséhez szükséges viszonylag hosszú idő (általában percek), ami a légzésmozgásokból származó műtermékek megjelenéséhez vezet (ez különösen csökkenti a tüdővizsgálat hatékonyságát), aritmiák (szívvizsgálat során), a kövek, meszesedések, bizonyos típusú csontpatológiák megbízható kimutatásának képtelensége, a berendezések és üzemeltetésük magas költsége, az eszközök elhelyezésére szolgáló helyiségekre vonatkozó speciális követelmények (árnyékolás az interferenciától), a klausztrofóbiás betegek vizsgálatának képtelensége, mesterséges pacemakerek, nem orvosi fémekből készült nagy fémimplantátumok.
 [ 8 ], [ 9 ], [ 10 ], [ 11 ], [ 12 ], [ 13 ], [ 14 ], [ 15 ]
[ 8 ], [ 9 ], [ 10 ], [ 11 ], [ 12 ], [ 13 ], [ 14 ], [ 15 ]
Kontrasztanyagok MRI-hez
Az MRI alkalmazásának kezdetén azt hitték, hogy a különböző szövetek közötti természetes kontraszt szükségtelenné teszi a kontrasztanyagokat. Hamarosan felfedezték, hogy a különböző szövetek közötti jelek különbsége, azaz az MR-kép kontrasztja jelentősen javítható kontrasztanyagok segítségével. Amikor az első MR-kontrasztanyag (paramágneses gadolíniumionokat tartalmazó) kereskedelmi forgalomba került, az MRI diagnosztikai információtartalma jelentősen megnőtt. Az MR-kontrasztanyagok használatának lényege a szövet- és szervprotonok mágneses paramétereinek megváltoztatása, azaz a T1 és T2 protonok relaxációs idejének (TR) megváltoztatása. Napjainkban az MR-kontrasztanyagoknak (vagy inkább kontrasztanyagoknak - CA) többféle osztályozása létezik.
A relaxációs időre gyakorolt domináns hatás szerint az MR-KA a következőkre oszlik:
- T1-CA, amelyek lerövidítik a T1-et, és ezáltal növelik a szöveti MP-jel intenzitását. Pozitív CA-nak is nevezik őket.
- A T2-t megrövidítő T2-CA-k, amelyek csökkentik az MR-jel intenzitását. Ezek negatív CA-k.
Mágneses tulajdonságaik alapján az MR-CA-k paramágneses és szuperparamágneses kategóriába sorolhatók:
 [ 16 ], [ 17 ], [ 18 ], [ 19 ], [ 20 ]
[ 16 ], [ 17 ], [ 18 ], [ 19 ], [ 20 ]
Paramágneses kontrasztanyagok
A paramágneses tulajdonságokkal az egy vagy több párosítatlan elektronnal rendelkező atomok rendelkeznek. Ezek a gadolínium (Gd), króm, nikkel, vas és mangán mágneses ionjai. A gadolíniumvegyületek kapták a legszélesebb körű klinikai alkalmazást. A gadolínium kontraszthatása a T1 és T2 relaxációs idők lerövidülésének köszönhető. Alacsony dózisokban a T1-re gyakorolt hatás dominál, növelve a jel intenzitását. Nagy dózisokban a T2-re gyakorolt hatás dominál, csökkentve a jel intenzitását. A paramágneses anyagokat ma már a klinikai diagnosztikai gyakorlatban alkalmazzák legszélesebb körben.
Szuperparamágneses kontrasztanyagok
A szuperparamágneses vas-oxid domináns hatása a T2 relaxáció lerövidülése. A növekvő dózissal a jel intenzitása csökken. A ferromágneses CA-k, amelyek közé tartoznak a magnetitferrithez (Fe2+OFe23+O3) szerkezetileg hasonló ferromágneses vas-oxidok ,szintén ebbe a CA - csoportba sorolhatók.
A következő osztályozás a CA farmakokinetikáján alapul (Sergeev PV et al., 1995):
- extracelluláris (szövet-nem specifikus);
- gyomor-bélrendszeri;
- organotrop (szövetspecifikus);
- makromolekuláris, amelyeket az érrendszer meghatározására használnak.
Ukrajnában négy MR-CA ismert, amelyek extracelluláris, vízben oldódó paramágneses CA-k, amelyek közül a gadodiamidot és a gadopentetinsavat széles körben alkalmazzák. A CA fennmaradó csoportjai (2-4) külföldi klinikai vizsgálatok alatt állnak.
Extracelluláris vízoldható MR-CA
Nemzetközi név |
Kémiai képlet |
Szerkezet |
Gadopentetikus sav |
Gadolínium-dimeglumin-dietilén-triamin-penta-acetát ((NMG)2Gd-DTPA) |
Lineáris, ionos |
Gadotersav |
(NMG)Gd-DOTA |
Ciklikus, ionos |
Gadodiamid |
Gadolínium-dietilén-triamin-pentaacetát-bisz-metilamid (Gd-DTPA-BMA) |
Lineáris, nemionos |
Gadoteridol |
Gd-HP-D03A |
Ciklikus, nemionos |
Az extracelluláris CA-kat intravénásan adják be, 98%-uk a veséken keresztül ürül ki, nem hatolnak át a vér-agy gáton, alacsony toxicitásúak és a paramágneses anyagok csoportjába tartoznak.
MRI ellenjavallatok
Az abszolút ellenjavallatok közé tartoznak azok az állapotok, amelyekben a vizsgálat veszélyt jelent a betegek életére. Ilyen például az elektronikusan, mágnesesen vagy mechanikusan aktiválódó implantátumok jelenléte – ezek elsősorban mesterséges pacemakerek. Az MRI-készülék rádiófrekvenciás sugárzása megzavarhatja a kérésrendszerben működő pacemaker működését, mivel a mágneses mezők változásai utánozhatják a szívműködést. A mágneses vonzás a pacemaker elmozdulását is okozhatja a foglalatában, és az elektródák elmozdulását. Ezenkívül a mágneses mező akadályozza a ferromágneses vagy elektronikus középfülbe implantátumok működését. A mesterséges szívbillentyűk jelenléte veszélyes, és csak akkor abszolút ellenjavallat, ha nagy térerősségű MRI-készülékeken vizsgálják, és ha klinikailag felmerül a billentyűkárosodás gyanúja. A vizsgálat abszolút ellenjavallatai közé tartozik a kis fém sebészeti implantátumok (vérzéscsillapító kapcsok) jelenléte a központi idegrendszerben, mivel a mágneses vonzás miatti elmozdulásuk vérzést okozhat. Jelenlétük a test más részein kisebb veszélyt jelent, mivel a kezelés után a kapcsok fibrózisa és beágyazódása segít stabilizálni azokat. A potenciális veszélyen túl azonban a mágneses tulajdonságokkal rendelkező fémes implantátumok jelenléte mindenképpen olyan műtermékeket okoz, amelyek megnehezítik a vizsgálat eredményeinek értelmezését.
MRI ellenjavallatok
Abszolút: |
Relatív: |
Pacemakerek |
Egyéb stimulánsok (inzulinpumpák, idegstimulátorok) |
Ferromágneses vagy elektronikus középfül implantátumok |
Nem ferromágneses belsőfül-implantátumok, szívbillentyű-protézisek (nagy térben, ha diszfunkció gyanúja merül fel) |
Agyi erek vérzéscsillapító klipjei |
Vérzéscsillapító klipek más helyeken, dekompenzált szívelégtelenség, terhesség, klausztrofóbia, fiziológiai monitorozás szükségessége |
A fent felsoroltakon kívül relatív ellenjavallatok közé tartozik a dekompenzált szívelégtelenség, a fiziológiai monitorozás szükségessége (gépi lélegeztetés, elektromos infúziós pumpák). A klausztrofóbia az esetek 1-4%-ában akadályozza a vizsgálatot. Ez egyrészt nyitott mágneses eszközök használatával, másrészt az eszköz és a vizsgálat menetének részletes ismertetésével leküzdhető. Nincs bizonyíték az MRI káros hatására az embrióra vagy a magzatra, de a terhesség első trimeszterében ajánlott kerülni az MRI-t. Az MRI alkalmazása terhesség alatt olyan esetekben javallt, amikor más nem ionizáló diagnosztikai képalkotó módszerek nem nyújtanak kielégítő információt. Az MRI-vizsgálat nagyobb betegrészvételt igényel, mint a komputertomográfia, mivel a beteg mozgása a vizsgálat során sokkal nagyobb hatással van a képek minőségére, így az akut patológiában, tudatzavarban, görcsös állapotban, demenciában szenvedő betegek, valamint a gyermekek vizsgálata gyakran nehézkes.

