A cikk orvosi szakértője
Új kiadványok
Glioma az agyban
Utolsó ellenőrzés: 29.06.2025

Minden iLive-tartalmat orvosi szempontból felülvizsgáltak vagy tényszerűen ellenőriznek, hogy a lehető legtöbb tényszerű pontosságot biztosítsák.
Szigorú beszerzési iránymutatásunk van, és csak a jó hírű média oldalakhoz, az akadémiai kutatóintézetekhez és, ha lehetséges, orvosilag felülvizsgált tanulmányokhoz kapcsolódik. Ne feledje, hogy a zárójelben ([1], [2] stb.) Szereplő számok ezekre a tanulmányokra kattintható linkek.
Ha úgy érzi, hogy a tartalom bármely pontatlan, elavult vagy más módon megkérdőjelezhető, jelölje ki, és nyomja meg a Ctrl + Enter billentyűt.
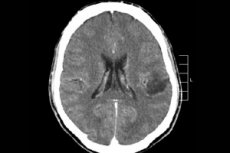
A központi idegrendszer számos daganatos folyamata közül leggyakrabban az agyi gliómát diagnosztizálják – ez a kifejezés gyűjtőfogalom, a daganat magában foglalja az összes diffúz oligodendrogliális és asztrocitás gócot, asztrocitómát, asztroblasztómát és így tovább. Az ilyen daganat különböző mértékű rosszindulatú lehet, gliális struktúrákból – neuronok körül lokalizálódó sejtekből – képződik. A gliómák fő előfordulási területe az agyféltekék, az agykamrák falai és a chiasma – a látóidegrostok részleges metszéspontjának területe. Külsőleg a daganat rózsaszínes vagy vöröses árnyalatú, kerek vagy orsó alakú, elmosódott határokkal rendelkező göbös elem. [ 1 ]
Járványtan
Az esetek körülbelül 5%-ában a gliómák örökletes patológiákkal társulnak - különösen a neurofibromatózissal és más domináns öröklődésű szindrómákkal. A szakértők rámutatnak, hogy az agyi gliómák abszolút többsége sporadikusan alakul ki - azaz egyértelmű ok nélkül.
Összességében a központi idegrendszer primer daganatai az összes daganat körülbelül 2%-át teszik ki, ami valamivel több mint 21 esetet jelent százezer lakosra vetítve. Közülük a gliómák az esetek 35-36%-ában fordulnak elő, és több mint 15%-uk glioblasztóma.
Egyes adatok szerint a glioma gyakrabban érinti a férfiakat, mint a nőket - a daganat különösen gyakori az 50 év felettiek körében.
Az elmúlt évtizedekben jelentősen megnőtt a gliómák globális előfordulása az idősek körében. A jelenség okait még nem állapították meg.
Az Egészségügyi Világszervezet definíciója szerint a gliatumoroknak három fő változatát azonosították, amelyek szövettani jellemzőikben különböznek egymástól. Ezek az oligodendrogliómák, az asztrocitómák és a kombinált oligoasztrocitómák. Az egyes alacsony malignitású patológiák előfordulási gyakoriságát nem határozták meg megbízhatóan. Egyes tanulmányok az oligodendrogliómák előfordulási gyakoriságának 5%-ról 30%-ra való növekedését, az asztrocitómák előfordulási gyakoriságának csökkenését mutatják.
A gliadaganatok képesek beszűrődni az agyszövetbe, és az alacsony malignitású gócok túlnyomó többsége néhány éven belül rosszindulatúvá válik. [ 2 ]
Okoz agyi gliómák
Az agyi glioma a daganatos folyamatok egész csoportja, amelyek közös jellemzője, hogy az agyszövetben található központi idegrendszer gliasejtjeiből alakulnak ki. Az ilyen daganatok két hisztopatológiai változatra oszlanak: magas malignitású és alacsony malignitású gliómákra.
A növekedés kialakulásának forrása a neuroglia sejtek (asztrociták, oligodendrociták), amelyek az agyi neuronok szerkezeti alapját és életképességét biztosítják.
A gliasejtes tumorfolyamatok szerkezetükben, a gének mutációs változásaiban, agresszivitásában, klinikai jellemzőiben, diagnosztikai jellemzőiben, kezelésre adott válaszában és a betegek prognózisában nagymértékben különböznek. A központi idegrendszer embrionális és ependimális daganatai - különösen a medulloblasztómák és az ependimómák - szövettani szerkezetükben különböznek, de kezelésük szempontjából hasonlóak.
A gliaelemeket először a 19. század végén sorolták az idegrendszer külön szerkezeti kategóriájába.
A neuroglia szövet olyan sejtekből áll, amelyek kiegészítő funkciókat látnak el: trofikus, támogató, védő, szekréciós. A neuronok és a gliociták együtt léteznek egymással, együtt alkotják az idegrendszert, és nagy jelentőséggel bírnak a szervezet létfontosságú tevékenységének általános folyamataiban.
A gliocitákat nagyjából több fő típusba sorolják: asztrociták, oligodendrociták, ependimális sejtek és mikrogliák.
A tudósok a mai napig nem tudnak válaszolni a neurogliális tumorképződés megbízható okaira vonatkozó kérdésre. Feltehetően bizonyos negatív hozzájárulást jelentenek a radioaktív hatások, a fertőző betegségek, a mérgezés (különösen a kémiai, foglalkozási eredetű). Az örökletes tényező is fontos.
Az agyi gliómák rendellenes neurogliocitákból alakulnak ki, amelyek genetikai hibája rendellenes növekedéshez és működéshez vezet – ezeket a struktúrákat „éretlennek” nevezik. A hiányos sejtek gyakrabban egy területen helyezkednek el, ahol a daganat kialakul.
Egyszerűen fogalmazva, a gliasejtek képződése a módosult neuroglia sejtek kaotikus és szórványos növekedésének eredménye. A folyamat ependimocitákból, oligodendrocitákból, asztrocitákból (asztrocitómák, beleértve az óriássejtes és anaplasztikus asztrocitákból) fejlődhet ki. [ 3 ]
Kockázati tényezők
Annak ellenére, hogy a szakértők nem tudják pontosan jellemezni a gliális onkopatológiák kialakulásának okait, bizonyos esetekben megjelenésük megelőzhető a fő kockázati tényezők kiküszöbölésével:
- Az ionizáló sugárzás rákkeltő hatású, leukémia kialakulását és sűrű szerkezetű rákos folyamatok kialakulását okozhatja, beleértve a fiatal korosztályt is. A gyakori és indokolatlan radiológiai orvosi beavatkozások, az ultraibolya sugárzás (beleértve a szoláriumot is) szintén potenciális rákkeltő hatásúak, és daganatok megjelenését okozhatják különböző szervekben, beleértve az agyat is.
- A foglalkozási ártalmak, a mérgezések gyakran okozati összefüggésben állnak a rákos daganatok kialakulásával. Különösen veszélyesnek tekinthető a gumi- és üveggyártás, a növényvédő szerek és üzemanyagok, a fémek és textíliák, a festékek és laboratóriumi reagensek gyártása. Veszélyeztetettek a repülőgépiparban, a szén- és fémiparban, a vegyiparban és melléktermék-gyártó üzemekben, az építőanyagok és elektródák, az üzemanyagok és kenőanyagok, a műanyagok és monomerek gyártásában dolgozók.
- A levegő-, víz- és talajszennyezés a világon az összes rákos megbetegedés akár 4%-áért is felelős. A környezetben nagy mennyiségben jelen lévő rákkeltő anyagok a belélegzett levegővel, ivóvízzel és élelmiszerrel jutnak be a szervezetbe. Különösen veszélyesnek számít az ökológiailag veszélyes területeken – nagy ipari létesítmények, forgalmas közlekedési csomópontok közelében – való élet.
- A fertőző betegségek - különösen a vírusfertőzések - szintén kedvező feltételeket teremthetnek a daganatok kialakulásához. Fontos ezt szem előtt tartani és előzetesen beoltatkozni, valamint megelőzni a fertőző és parazitás betegségeket.
- A dohányzás és az alkoholfogyasztás számos rákfajta kockázati tényezőjének számít, nem csak az agyi gliómáknak.
- Elégtelen fizikai aktivitás, túlsúly, helytelen táplálkozás, anyagcserezavarok, fejsérülések, érrendszeri patológiák - további stresszfaktorok, amelyek kiválthatják az intracelluláris rendellenességek kezdetét.
- Az idősebb kor a leggyakoribb időszak a neoplazmák kialakulására a szervezetben, ezért az 55 év felettieknek különösen vigyázniuk kell saját egészségükre.
A glioma kialakulásának fő és legjelentősebb kockázati tényezője azonban továbbra is az örökletes hajlam.
Pathogenezis
A szakértőknek a mai napig számos feltételezésük van az agyi gliómák kialakulásával kapcsolatban. Minden elméletnek megvannak a maga alapjai, de az egyetlen helyes és megbízható patogenetikai mechanizmust a tudósok még nem azonosították. A legtöbb esetben a daganatok kialakulásában a következő tényezőkről beszélünk:
Embriogenezis-elégtelenség, amely a szervlerakás megzavarásából és a "rossz" sejtszerkezetek kialakulásából áll;
- Ionizáló sugaraknak, potenciális rákkeltő anyagoknak való kitettség vegyi anyagok, élelmiszer-adalékanyagok stb. formájában;
- Fejsérülés;
- Generációról generációra öröklődő génbetegségek ("familiáris" glioma);
- Immunrendszeri diszfunkció, neuroinfekciók.
A legtöbb glióma diffúz növekedésű, behatol a környező normál agyszövetbe. A rosszindulatúság mértékétől függően a daganat több évig is kialakulhat bármilyen manifesztáció nélkül. Agresszív lefolyás esetén a tünetek több hónap alatt gyorsan fokozódnak.
A tumorgenezis egy része diszembriogenetikus változásoknak köszönhető.
Az agytörzs különböző szinteken érintett lehet: a diffúz agytörzsi glioma viszont mind anatómiai-morfológiai, mind klinikai szempontból különbözik. Néhány ilyen daganat – különösen a quadriplegia lemez gliómája – viszonylag jóindulatú lehet, progresszió jelei nélkül. A pontin gliomát ezzel szemben a rosszindulatúság, az agresszivitás és a rossz prognózis jellemzi.
Agyi struktúrák diffúz elváltozásai, amelyekben a nagy agyféltekék több mint három anatómiai zónája érintett a kóros folyamatban, lehetséges periventrikuláris divergencia és a corpuscallon keresztüli áthaladás gliomatosisban [ 4 ]
Az agyi glioma örökletes?
Az agyi glióma kialakulásának egyik jól bizonyított kockázata az örökletes – azaz hasonló vagy más intracerebrális daganatok jelenléte a közvetlen ősöknél vagy ugyanazon generáción belül. A radioaktív expozíció és a potenciális rákkeltő anyagokkal való rendszeres vagy hosszan tartó érintkezés súlyosbítja a helyzetet.
Nemcsak a gliómák öröklődhetnek, hanem azok a betegségek is, amelyek fokozott tumornövekedéssel járnak, függetlenül a lokalizációtól - ez különösen az 1-es és 2-es típusú neurofibromatózis, a Li-Fraumeni-szindróma, a Hippel-Lindau-szindróma lehet. A gliómasejtekben gyakran bizonyos gének vagy kromoszómák változásait észlelik.
Az emberi glioma kialakulásával kapcsolatos főbb patológiákat a táblázat foglalja össze:
Patológia |
Kromoszóma |
Gén |
A daganatok változatossága |
Li-Fraumeni-szindróma |
17р13 |
TR53 |
Neuroektodermális daganatok, asztrocitóma. |
Neurofibromatózis |
17q11 |
NF1 |
Látóideg glioma, pilocyta asztrocitóma, neurofibromatózis |
Turcotte-szindróma |
3p21, 7p22 |
HMLH1, HPSM2 |
Asztrocitóma |
Tuberózus szklerózis (Burneville-szindróma). |
9q34, 16p13 |
TSC1, TSC2 |
Gigantocelluláris szubependimális asztrocitóma |
Függetlenül a gliatumor jellegétől, legyen szó akár sporadikus esetről, akár örökletes patológiáról, egy kórosan megváltozott gén expressziójával járó rendellenességről van szó. A tanulási hatások eredményeként kialakult daganatokon kívül más esetekben a genetikai elváltozások okai továbbra sem tisztázottak.
Tünetek agyi gliómák
A fokális tünetek jellemzői közvetlenül függenek az agyi glioma lokalizációjának területétől, és mindenféle endokrin rendellenesség, az idegszövet összenyomódása vagy a helyi destruktív folyamatok következményeivé válnak.
Ha a daganat a parietális zónában található, akkor egy személyt olyan megnyilvánulások uralnak, mint a rohamok, érzékszervi zavarok, halláskárosodás.
Amikor a glioma a domináns agyfélteke területén lokalizálódik, beszédzavarokat, agráfiát, agnoziát észlelnek.
A temporális lebeny neoplazmáit gyakran görcsrohamok, afázia, a szaglás és a látásfunkció károsodása, valamint nehézlégzés kíséri.
Amikor a koponyán belüli nyomás megnő, a látóterek korlátozásával, a szemizmok bénulásával és a féloldali bénulással járó kép alakul ki.
A tumoros folyamat sajátossága miatt az agyi gliómát mindig kisebb-nagyobb mértékben neurológiai tünetek kísérik. Először is, általános gyengeség tapasztalható, a beteg folyamatosan aludni akar, a munkaképessége romlik, a gondolkodási folyamatok lelassulnak. Ebben a szakaszban nagy a kockázata a helytelen diagnózis felállításának, és ennek következtében a helytelen kezelés felírásának. Egyéb nem specifikus tünetek mellett:
- Vestibularis zavarok, beleértve a bizonytalan járást, az egyensúlyvesztést (pl. kerékpározás vagy lépcsőzés közben), a végtagok zsibbadását stb.;
- A látás fokozatos romlása, a vizuális kép megduplázódása;
- A hallásfunkció romlása;
- Elmosódott beszéd;
- Hányinger és hányás, ételtől vagy italtól független rohamok formájában;
- A mimikai izmok és más arcizmok gyengülése;
- Kellemetlen érzés nyeléskor;
- Rendszeres fejfájás (gyakran a reggeli órákban).
A klinikai kép fokozatosan bővül és romlik: egyes betegeknél lassan, másoknál hirtelen, szó szerint "a szemük láttára", néhány héten belül történik. Ez utóbbi esetben az agy agresszív, gyorsan fejlődő gliómájáról beszélünk.
Első jelek
Az agyi glióma a fejlődés korai szakaszában nem rendelkezik kifejezett tünetekkel. Az első megnyilvánulásokat gyakran más, kevésbé veszélyes patológiák jeleivel tévesztik össze.
Általánosságban elmondható, hogy a glioma klinikai képe változatos, és a kóros góc helye és mérete határozza meg. Ahogy a daganat növekszik, az általános agyi tünetek kialakulnak és fokozódnak:
- Tartós és rendszeres fejfájás, amely nem reagál a szokásos gyógyszerekre (nem szteroid gyulladáscsökkentő gyógyszerek);
- Időnként jelentkező hányinger, néha hányásig;
- Kellemetlen, nehéz érzés a szemgolyó területén;
- Görcsrohamok.
Az agyi manifesztációk különösen intenzívek, amikor a daganat a kamrákba vagy a liquorrendszerbe nő. Az agy-gerincvelői folyadék elvezetése károsodik, a koponyaűri nyomás megnő, és hidrocephalus alakul ki. A folyamat az agy egy bizonyos részét érinti, ami befolyásolja a megfelelő klinika kialakulását:
- Problémák vannak a vizuális funkcióval;
- Beszédkárosodás;
- Vestibularis rendellenességek (szédülés, mozgáskoordináció zavara) jelentkeznek;
- Parézis, a karok, lábak bénulása;
- A memória és a koncentráció romlik;
- A gondolkodási folyamatok károsodnak;
- Viselkedési zavarok jelennek meg.
A kezdeti stádiumban a tünetek gyakorlatilag hiányoznak, vagy annyira jelentéktelenek, hogy nem keltenek figyelmet. Éppen ezért a szakértők határozottan javasolják a rendszeres megelőző vizsgálatokat és szűrővizsgálatokat. Végül is minél korábban észlelik a daganatos folyamatot, annál nagyobb a gyógyulás és a túlélés esélye. [ 5 ]
Az agy gliómája egy gyermeknél
A gyermekkorban talált számos agydaganat közül a gliómák aránya 15-25% között mozog. A betegség a gyermekek korai tizenéves és húszas éveik elején jelentkezhet, bár a 3 év alatti csecsemőknél nagyon ritka.
A patológia a gliasejtek mutációjának hátterében kezdődik. A mai napig nincs válasz arra a kérdésre, hogy miért következik be ez a mutáció.
Az egyetlen dolog, amit megbízhatóan megtudtak, az az, hogy bizonyos örökletes betegségek, amelyek a daganatnövekedés fokozott kockázatával járnak, növelik az agyi glióma kialakulásának valószínűségét is.
Ezenkívül a tudósok felfedezték, hogy a gliasejtekben eltérések lehetnek az egyes génekben vagy kromoszómákban. E rendellenesség miatt egy mutációs mechanizmus indul be, amely nem örökletes. Lehetséges, hogy ez a fejlődés egyik legkorábbi szakaszában következik be.
Bizonyított tény, hogy az akut leukémia vagy retinoblasztóma jelenléte a gyermek kórtörténetében, vagy bármilyen más okból bekövetkezett agyi besugárzás jelentősen növeli a glioma kialakulásának kockázatát (egy bizonyos idő elteltével).
A gyermekkori tünetek a rosszindulatúság mértékétől és a kóros fókusz lokalizációjától függenek. Különbséget tesznek specifikus és nem specifikus tünetek között:
- A nem specifikus tünetek nem "kötődnek" a glioma helyéhez. Gyakori tünetek lehetnek a fejfájás, szédülés, étvágytalanság, étkezéssel össze nem függő hányás, (ismeretlen okból) fogyás, állandó fáradtságérzet, tanulmányi teljesítmény romlása, koncentrációs nehézségek, viselkedési zavarok. Ezeket a tüneteket az intrakraniális struktúrák összenyomódása okozza, ami a növekvő tömeg közvetlen nyomásaként, valamint az agy-gerincvelői folyadék keringésének zavaraként magyarázható. Fennáll az agyi hidrokéle veszélye.
- A specifikus tünetek a gliasejtes patológiás góc közvetlen helyétől függenek. Például a kisagydaganatot gyermekeknél általában járás- és egyensúlyzavar kíséri. A nagyagy sérülése görcsrohamokban, a gerincvelőben pedig izombénulásban nyilvánul meg. Előfordul, hogy a baba látása hirtelen romlik, tudatzavar, alvászavar lép fel, vagy valamilyen más fejlődési probléma merül fel.
Általános szabály, hogy gyermekkorban a rosszindulatú glioma a fejlődésének néhány hetében vagy hónapjában jelentkezik: gyakran a daganat gyors és ellenőrizetlen növekedése jellemzi.
A rosszindulatú gliadaganatokkal küzdő gyermekeket gyermekgyógyászati onkológiai központokban kezelik. Általában sebészeti beavatkozást, sugárterápiát és kemoterápiás kúrákat alkalmaznak.
A legfontosabb kezelési lépés az idegsebészet. Minél radikálisabb, annál jobbak a gyermek gyógyulási esélyei. A sebészeti beavatkozás azonban nem mindig lehetséges: különösen az agytörzsi gliómák eltávolításakor, valamint a 3 év alatti gyermekek sugárterápiájánál jelentkezhetnek problémák.
A központi agy (köztes és középagy) gliómáit nehéz teljesen eltávolítani, mivel fennáll az egészséges szövetek károsodásának veszélye. Ha a daganat teljes eltávolítása lehetetlen, a beteg palliatív kezelést kap.
A rosszindulatú gliómában szenvedő gyermekeket standardizált protokollok szerint kezelik, amelyeket szigorúan kontrollált klinikai vizsgálatok során határoztak meg. A leggyakoribb protokollok a következők:
- HIT HGG 2007: 3-17 éves gyermekek kezelését foglalja magában.
- HIT SKK: csecsemők számára alkalmas (három éves korig), és nem jár sugárkezeléssel.
A gliómák gyermekkori túlélési statisztikái általában nem túl optimisták. Azonban semmilyen esetben sem lehet előre megjósolni a kezelési intézkedések hatékonyságát egy adott gyermek esetében. Fontos, hogy gondosan kövessük az orvos összes utasítását, ami jelentősen növeli a gyógyulás esélyeit.
Forms
A gliómák lehetnek alacsony malignitásúak és magas malignitásúak, intenzív növekedéssel és áttétképződési hajlammal. Fontos megérteni, hogy az alacsony malignitás nem feltétlenül jelenti a daganatmentességet. Bármely agydaganat további térfogatot hoz létre, összenyomja az agyi struktúrákat, ami azok elmozdulásához és megnövekedett koponyaűri nyomáshoz vezet. Ennek eredményeként a beteg meghalhat.
A rosszindulatú asztrocitómáknak két fő típusa van. Ezek a glioblasztómák és az anaplasztikus asztrocitómák, amelyeket a molekuláris változások szerint osztanak fel. Az asztrocitómákból kifejlődő, alacsony malignitási fokú másodlagos rosszindulatú daganatok leggyakrabban fiatal betegeknél fordulnak elő. A kezdetben rosszindulatú gliatípusú daganatok gyakrabban fordulnak elő idős betegeknél.
A szerkezeti elhelyezkedéstől függően a gliómák a következőkre oszlanak:
- Szupratentoriális (a kisagy feletti lokalizációval az oldalsó kamrák, a nagy agyféltekék területén);
- Subtentorial (a kisagy alatti lokalizációval a hátsó koponyaüregben).
A szövettani jellemzők szerint megkülönböztetjük az ilyen típusú gliómákat:
- Az asztrocitás glioma a leggyakoribb. Ez utóbbi nodulárisra és diffúzra oszlik (ez utóbbira a gyors növekedés és a stroke-mintázat jellemző).
- Oligodendroglióma – a betegek 5%-ánál fordul elő. Megkövesedésekkel – meszesedési területekkel – rendelkezik, leggyakrabban a frontális lebenyben.
- Ependimális glioma - a gerincvelő és a kamrák központi csatornájának falait bélelő struktúrákból nő. Gyakran az agyállomány vastagságába, valamint az agy lumenébe is belenő.
Vegyes patológiai gócok, például szubependimóma, oligoasztrocitóma stb. is lehetségesek.
Minden glioma a következő stádiumokba sorolható:
- Lassan növekvő, viszonylag jóindulatú daganatok, amelyeknek nincsenek nyilvánvaló klinikai tüneteik.
- Lassan növekvő "határeseti" gliómák, amelyek fokozatosan III. stádiumba és azon túlra alakulnak.
- Malignus glioma.
- Malignus glioma intenzív, agresszív növekedéssel és terjedéssel, rossz prognózissal.
Minél alacsonyabb a rosszindulatú daganat stádiumának stádiumában lévő daganat, annál kisebb a valószínűsége az áttétképződésnek és az eltávolított daganat kiújulásának, és annál nagyobb a beteg gyógyulásának esélye. A legnagyobb veszélyt a glioblastoma multiforme jelenti, egy alacsony differenciáltságú folyamat, intenzív növekedéssel és fejlődéssel. [ 6 ]
A neuroglioma lehetséges és leggyakoribb változatai:
- Az agytörzs és a hídfő lézióival járó glióma az agy és a gerincvelő közötti összeköttetés területén található. Itt lokalizálódnak a légzési, szív- és motoros funkciókért felelős fontos neurocentrumok. Ha ez a zóna sérült, a vesztibuláris és a beszédkészülék működése zavart szenved. Gyakran gyermekkorban észlelhető.
- A vizuális glioma a látóideget körülvevő neurogliasejteket érinti. A patológia látáskárosodást és exophthalmust okoz. Gyermekeknél gyakrabban alakul ki.
- Az alacsony malignus neurogliomát lassú növekedés jellemzi, gyakrabban a nagy agyféltekékben és a kisagyban lokalizálódik. Gyakrabban fordul elő fiatalokban (serdülőknél és 20 év körüli fiatal felnőtteknél).
- A corpus callosum gliómája jellemzőbb a 40 és 60 év közötti egyénekre, és leggyakrabban a glioblasztóma képviseli.
- A chiasma gliómája a látóideg átmenetének zónájában lokalizálódik, így rövidlátással, látótérkieséssel, elzáródásos hidrocephalusszal és neuroendokrin rendellenességekkel jár. Bármely életkorban előfordulhat, de leggyakrabban az I. típusú neurofibromatózisban szenvedő betegeket érinti.
Komplikációk és következmények
Alacsony malignitású gliómák (I-II. fokozat, erősen malignus - pl. asztrocitóma, oligoasztrocitóma, oligodendroglióma, pleomorf xanthoasztrocitóma stb.) és erősen malignus (III-IV. fokozat - glioblasztóma, anaplasztikus oligodendroglióma, oligoasztrocitóma és asztrocitóma). A IV. fokozatú gliómák különösen rosszindulatúak.
Az agytörzsi glioma prognózisa igen kedvezőtlen, mivel a daganat egy olyan agyterületet érint, ahol az agy és a végtagok közötti legfontosabb idegkapcsolatok koncentrálódnak. Már egy meglehetősen kis daganat is ezen a területen elég ahhoz, hogy a beteg állapota gyorsan romoljon és bénulást provokáljon.
Nem kevésbé kedvezőtlen következmények jelentkeznek, ha más agyterületeket is érint. Gyakran az agykéreg daganatáról van szó, amely a kezelés ellenére sem ad esélyt a beteg hosszú élettartamára. Gyakran csak a halál elhalasztása lehetséges.
Az orvosi statisztikák szerint az ötéves túlélési arány gyakran csak 10-20%. Bár ezek a számok nagymértékben függenek mind a rosszindulatúság mértékétől, mind a végrehajtott sebészeti beavatkozás pontos lokalizációjától és mennyiségétől. A kóros góc teljes eltávolítása után a túlélési arány jelentősen megnő (néha akár 50%-kal is). A kezelés hiánya vagy annak lehetetlensége (egy vagy másik okból) garantáltan a beteg halálához vezet.
Az alacsony malignus gliadaganatok többsége képes beszivárogni az agyszövetbe és több év alatt rosszindulatúvá válni.
A glioma kiújulásának kockázatát a szakértők „nagyon valószínűnek” tartják. Mindazonáltal a kezelést nem szabad elhanyagolni: fontos a jó életminőség biztosítása a lehető leghosszabb ideig.
A kiújuló gliómák prognózisa mindig rosszabb, mint az elsődleges daganatoké. A terápiás optimalizálási vizsgálatokon alapuló modern kezelési protokollok azonban gyakran kellően jó eredményeket érnek el még a rendkívül rosszindulatú daganatok esetén is.
Lehetséges következmények kemoterápia után:
- Lesoványodás, fogyatkozás, emésztési zavarok, szájbetegségek;
- A központi idegrendszer fokozott ingerlékenysége, aszténia;
- Halláskárosodás, fülzúgás és fülzúgás;
- Görcsrohamok, depressziós zavarok;
- Hipertenzív krízis, a vérkép megváltozása;
- Veseelégtelenség;
- Allergiás folyamatok, hajhullás, pigmentfoltok megjelenése a testen.
A kemoterápia után a betegek az immunrendszer kifejezett gyengülését észlelik, ami különböző fertőző patológiák kialakulásához vezethet.
Diagnostics agyi gliómák
Az agyi glióma gyanúja a következő tünetek alapján alakulhat ki:
- A beteg lokalizált vagy generalizált rohamokat tapasztal, amelyek a daganat kérgi elhelyezkedésére és lassú fejlődésére jellemzőek. Epi-rohamok az alacsony malignitású gliadaganatokban szenvedő betegek 80%-ánál és a magas malignitású gliómákban szenvedő betegek 30%-ánál fordulnak elő.
- A megnövekedett koponyaűri nyomás különösen jellemző a jobb oldali frontális és parietális lebenyben elhelyezkedő elváltozásokra. A magas koponyaűri nyomáshoz kapcsolódó vérkeringési és liquorkeringési zavar állandó és fokozódó fejfájással, hányingerrel és hányással, látászavarokkal és álmossággal jár. Előfordulhat a látóideg ödémája, az elterelő ideg bénulása. A kritikus értékre emelkedett koponyaűri nyomás kóma és halál kialakulásához vezethet. A magas szemnyomás másik oka a vízfejűség.
- A betegnél növekvő fokális kép figyelhető meg. Szupratentoriális képződmények esetén a motoros és érzékszervi szférák zavart szenvednek, hemiopia, afázia és kognitív zavarok alakulnak ki.
Ha az orvos agydaganat jelenlétére gyanakszik, optimális MRI-vizsgálatot végezni kontrasztanyag (gadolínium) bevezetésével vagy anélkül, hogy meghatározná annak helyét, méretét és további jellemzőit. Ha a mágneses rezonancia képalkotás nem lehetséges, komputertomográfiát végeznek, és a mágneses rezonancia spektroszkópiát alkalmazzák a differenciálódás módszereként. Ezen diagnosztikai módszerek informatív jellege ellenére a végső diagnózist csak a daganatfókusz reszekciója során végzett szövettani megerősítés után állítják fel.
A fenti kritériumok alapján a diagnózis felállítását alapos kórtörténettel, a szomatoneurológiai és funkcionális állapot felmérésével ajánlott kezdeni. A neurológiai állapot felmérése a valószínűsíthető intellektuális és mentális zavarok meghatározásával együtt történik.
Ajánlott laboratóriumi vizsgálatok:
- Teljes körű általános klinikai vérvizsgálat;
- Teljes vérkémiai panel;
- Vizeletvizsgálat;
- Véralvadási vizsgálat;
- Onkológiai markerek elemzése (AFP, béta-hCG, LDH - releváns, ha a tobozmirigy zónájának elváltozása gyanúja merül fel).
A glioblasztómában és anaplasztikus asztrocitómában szenvedő betegek prognosztikai szempontjainak tisztázása érdekében az IDH1|2-1 génmutációt és az MGMT génmetilációt vizsgálták. Oligodendrogliómában és oligoasztrocitómában szenvedő betegeknél az 1p|19q kodellációt határozták meg.
Az instrumentális diagnosztikát elsősorban az agy (néha a gerincvelő) kötelező mágneses rezonancia képalkotása jelenti. Az MRI-t három vetületben végzik, standard T1-2, FLAIR, T1 kontrasztanyagos módokban.
Szükség esetén az érhálózat ultrahangvizsgálatát, a motoros és beszédszakaszok funkcionális mágneses rezonancia képalkotását, valamint angiográfiát, spektroszkópiát, MR-traktográfiát és perfúziót végzik.
További vizsgálatok lehetnek:
- Az agy elektroencefalográfiája;
- Konzultációk idegsebésszel, onkológussal, radiológussal, szemész szakorvossal, radiológussal.
Megkülönböztető diagnózis
A differenciáldiagnózist szükségszerűen nem daganatos patológiákkal végzik - különösen arteriovénás vagy artériás malformáció által okozott vérzéssel, valamint pszeudotumor demyelinizációs folyamatokkal, gyulladásos betegségekkel (toxoplazmózis, agytályog stb.).
Ezenkívül különbséget kell tenni az elsődleges daganatfókusz és a központi idegrendszeri áttétek között.
A modern mágneses rezonancia képalkotási lehetőségekkel a diagnosztikai intézkedések kellő pontossággal elvégezhetők, hogy megállapítsák a központi idegrendszerben lévő elsődleges góc eredetét. Az agy MRI-vizsgálatát kontrasztanyaggal vagy kontrasztanyag nélkül, T1, T2 FLAIR módban - három vetületben, vagy vékony szeletekben axiális vetületben (SPGR mód) végzik. Ezek a diagnosztikai módszerek lehetővé teszik a daganat helyének, méretének, szerkezeti jellemzőinek, az érhálózattal és a közeli agyterületekkel való kapcsolatának pontos meghatározását.
Ezenkívül CT (kontrasztanyaggal vagy anélkül), CT-angiográfia (MR-angiográfia), MR-traktográfia, MR- vagy CT-perfúzió is elvégezhető a differenciáldiagnózis részeként. Az agy CT/PET-vizsgálatát metionin, kolin, tirozin és más aminosavak jelenlétében indokolt esetben alkalmazzák.
Kezelés agyi gliómák
A specifikus terápia sebészeti, kemoterápiás és sugárterápiás beavatkozásokból áll. Amennyiben lehetséges, kötelező a daganatfókusz teljes reszekciója, ami lehetővé teszi a tünetek gyors enyhítését és a diagnózis szövettani megerősítését.
A besugárzás pozitív hatással van a betegek várható élettartamának növelésére. Standardként 58-60 Gy teljes dózist alkalmaznak, amelyet 1,8-2 Gy egyéni besugárzási dózisokra osztanak. A daganatot lokálisan besugározzák, emellett a környezetéből legfeljebb 3 cm-es sugárterhelést is besugároznak. A sugárterápia elfogadhatóbb a brachyterápiával szemben. Bizonyos esetekben radiosebészeti módszerek ajánlottak, amelyek gamma-kés vagy lineáris gázpedálos besugárzásból, valamint neutronbefogásos bórterápiából állnak.
Az adjuváns kemoterápia szükségessége vitatott. Egyes esetekben a nitrozourea készítmények akár másfél évvel is növelték a betegek várható élettartamát, de az ilyen kemopreparátumok alkalmazásának egyes eredményei negatívak voltak. Napjainkban aktívan alkalmazzák a citotoxikus szereket, a neoadjuváns terápiát (sugárterápia előtt), a kombinált gyógyszereket, az intraarteriális kemoterápiát vagy a nagy dózisú kemoterápiát további őssejt-transzplantációval.
Általánosságban elmondható, hogy a gliómák sikeres kezeléséhez nagyon fontos az átfogó megközelítés, amelynek mértéke a tömeg helyétől és rosszindulatúságának mértékétől, méretétől és a beteg általános egészségi állapotától függ.
Az agytörzsi glióma esetében ritkán alkalmaznak sebészeti beavatkozást. A műtét fő ellenjavallata a góc lokalizációja - a létfontosságú szervek közvetlen közelében. Bizonyos esetekben a törzs gliómáját mikrosebészeti módszerekkel, preoperatív és posztoperatív kemoterápiával lehet eltávolítani. Az ilyen beavatkozás nagyon összetett, és speciális idegsebészeti képesítést igényel.
A sugárterápia és különösen a nagy ionizáló dózisoknak kitett sztereotaxiás műtét meglehetősen hatékony. Az ilyen technika alkalmazása a daganat kialakulásának korai szakaszában néha lehetővé teszi a beteg hosszan tartó remissziójának vagy akár teljes gyógyulásának elérését.
A sugárterápiát gyakran kombinálják kemoterápiával, ami javítja a beavatkozások hatékonyságát és csökkenti a sugárterhelést. Gliomákban nem minden kemopreventív szer terápiásan sikeres, ezért azokat egyenként írják fel, és szükség esetén módosítják a recepteket.
A fájdalom és az intrakraniális nyomás csökkentése érdekében, a fő kezeléstől függetlenül, tüneti terápiát írnak fel - különösen kortikoszteroid gyógyszereket, fájdalomcsillapítókat, nyugtatókat.
Gyógyszerek
A kortikoszteroid gyógyszerek hatással vannak a duzzanatra, több napra csökkentik a neurológiai tünetek súlyosságát. A többszörös mellékhatások és a kemoterápiás gyógyszerekkel való káros kölcsönhatások fokozott valószínűsége miatt azonban a szteroidok minimálisan hatékony dózisait alkalmazzák, és a lehető leghamarabb (pl. műtét után) leállítják azokat.
Az antikonvulzív szereket szisztematikusan alkalmazzák másodlagos megelőző intézkedésként olyan betegeknél, akik már átestek epilepsziás rohamokon. Ezek a gyógyszerek súlyos mellékhatásokat okozhatnak, és kölcsönhatásba léphetnek a kemoterápiás gyógyszerekkel is.
Az antikoagulánsok különösen fontosak a posztoperatív stádiumban, mivel a gliómában a tromboflebitis kialakulásának kockázata meglehetősen magas (akár 25%).
Jó hatás várható antidepresszáns-szorongásoldó szerek szedésétől. A metilfenidát 10-30 mg/nap két adagban történő alkalmazása gyakran lehetővé teszi a kognitív képességek optimalizálását, az életminőség javítását és a munkaképesség fenntartását.
A neurológiai elégtelenséget és az agyödéma jeleit (fejfájdalom, tudatzavarok) kortikoszteroid gyógyszerek - különösen prednizolon vagy dexametazon - kiküszöbölik. |
A kortikoszteroidok adagolását és kezelési rendjét egyénileg választják ki, a minimálisan hatásos dózis betartásával. A kezelés végén a gyógyszereket fokozatosan visszavonják. |
A kortikoszteroidokat gyomorvédő gyógyszerekkel - protonpumpa-blokkolókkal vagy H2-hisztamin- blokkolókkal - együtt szedik. |
A diuretikumokat (furoszemid, mannit) súlyos agyi struktúrák duzzanata és elmozdulása esetén írják fel, kortikoszteroid gyógyszerek kiegészítőjeként. |
Görcsrohamok (beleértve az anamnézist is) vagy az elektroencefalogramon megjelenő epilepsziaszerű tünetek esetén kiegészítő görcsgátló terápiát írnak fel. A görcsgátlókat nem profilaktikus célra írják fel. |
Kemoterápiára utaló jelek esetén a májenzim-funkciót nem befolyásoló görcsoldók szedése javasolt. Választható gyógyszerek: Lamotrigin, Valproinsav, Levetiracetám. Nem alkalmazható: Karbamazepin, Fenobarbitál. |
Az agyi gliómákban jelentkező fejfájást kortikoszteroidokkal kezelik. |
Fejfájás esetén bizonyos esetekben nem szteroid gyulladáscsökkentő gyógyszereket vagy tramadolt lehet alkalmazni. |
Ha a beteg nem szteroid gyulladáscsökkentő gyógyszereket szed, azokat a műtét előtt néhány nappal abbahagyják, hogy minimalizálják a műtét során fellépő vérzés esélyét. |
Bizonyos fájdalomesetekben narkotikus fájdalomcsillapítók – például fentanil vagy trimeperidin – ajánlottak. |
A tüdőembólia megelőzése érdekében a posztoperatív harmadik naptól kezdve kis molekulatömegű heparinokat - különösen enoxaparin-nátriumot vagy nadroparin-kalciumot - írnak fel. |
Ha a beteg szisztematikus antikoaguláns vagy trombocitagátló kezelésben részesül, legkésőbb egy héttel a műtét előtt át kell helyezni kis molekulatömegű heparinokra, a műtét előtti napon további leállítással és a műtét után 24-48 órával újrakezdéssel. |
Ha gliomás betegnél alsó végtagi vénás trombózis alakul ki, direkt antikoagulánsokkal kezelik. Nem kizárt CAVA-szűrő behelyezésének lehetősége sem. |
Kemoterápia az agy rosszindulatú gliómáinak kezelésére
A gliómák alapvető daganatellenes kemoterápiás kezelési módjai a következők:
- Lomustin 100 mg/m² az első napon, Vincristin 1,5 mg/m² az első és nyolcadik napon, Procarbazine 70 mg/m² a nyolcadik naptól a huszonegyedik napig, hathetente ismételve.
- Lomustin 110 mg/m² hathetente.
- Temozolomid 5/23 150-200 mg/m² az első naptól az ötödik napig, 28 naponta.
- Temozolomid kemoterápiás és sugárterápiás kezelés részeként, 75 mg/m² minden egyes sugárkezelési napon.
- Temozolomid ciszplatinnal vagy karboplatinnal (80 mg/m²), és Temozolomid 150-200 mg/m² az 1-5. napon 4 hetente.
- Temozolomid 7/7, 100 mg/m² dózisban a kúra 1-8. és 15-22. napján, négyhetente ismételve.
- Bevacizumab 5-10 mg/kg az első és tizenötödik napon, és irinotekán 200 mg/m² az első és tizenötödik napon, négyhetente ismételve.
- Bevacizumab 5-10 mg/kg az első, tizenötödik és huszonkilencedik napon, valamint lomusztin 90 mg/m² az első napon hathétente.
- Bevacizumab 5-10 mg/kg az első és tizenötödik napon, lomusztin 40 mg az első, nyolcadik, tizenötödik és huszonkettedik napon, hathetente ismételve.
- Bevacizumab 5-10 mg/kg az első és a tizenötödik napon, négyhetente ismételve.
A citosztatikus gyógyszerek sok esetben sikeresen gátolják a tumorsejtek növekedését, de nem mutatnak szelektivitást az egészséges szövetekkel és szervekkel szemben. Ezért a szakértők számos olyan ellenjavallatot azonosítottak, amelyekben a glioma kemoterápiája lehetetlen:
- Túlzott egyéni érzékenység a kemopreventív szerekkel szemben;
- A szív-, vese- és májfunkció dekompenzációja;
- Depressziós vérképzés a csontvelőben;
- Mellékvese-működési problémák.
A kemoterápiát rendkívül óvatosan kell alkalmazni:
- Jelentős szívritmuszavarban szenvedő betegek;
- Cukorbetegség esetén;
- Akut vírusfertőzések esetén;
- Idős betegeknek;
- Krónikus alkoholizmusban (krónikus alkoholmérgezésben) szenvedő betegek.
A kemopreventív gyógyszerek legsúlyosabb mellékhatása a toxicitásuk: a citosztatikumok szelektíven befolyásolják a vérsejtek működését és megváltoztatják azok összetételét. Ennek következtében csökken a vérlemezke- és eritrocita-tömeg, és vérszegénység alakul ki.
Mielőtt kemoterápiás kúrát írna fel a betegnek, az orvos mindig figyelembe veszi a gyógyszerek toxicitásának mértékét és a valószínűsíthető szövődményeket használatuk után. A kemoterápiás kúrákat mindig gondosan szakemberek felügyelik, és rendszeres vérvizsgálattal ellenőrzik.
A citosztatikus terápia lehetséges következményei:
- Soványság, lesoványodás;
- Nehézség a nyelési nehézségek, száraz nyálkahártyák, fogágygyulladás, diszpepszia;
- Központi idegrendszeri instabilitás, mániás-depressziós rendellenességek, görcsrohamok szindrómája, aszténia;
- A hallásfunkció romlása;
- A vérnyomás emelkedése a hipertóniás krízis kialakulásáig;
- A vérlemezkék, vörösvértestek, fehérvérsejtek számának csökkenése, többszörös vérzések, belső és külső vérzés;
- Veseelégtelenség;
- Allergiás folyamatok;
- Hajhullás, fokozott pigmentációjú területek megjelenése.
A kemoterápiás kúrák után a betegeknél fokozott a fertőző betegségek kialakulásának kockázata, és gyakori az izom- és ízületi fájdalom.
A kemoterápiás utáni káros hatások kockázatának csökkentése érdekében további rehabilitációs intézkedéseket kell előírni, amelyek célja a normális vérkép helyreállítása, a szív- és érrendszeri aktivitás stabilizálása, a neurológiai állapot normalizálása. Megfelelő pszichológiai támogatást kell biztosítani.
Sebészeti kezelés
A műtétet a daganat fókuszának lehető legnagyobb mértékű eltávolítására végzik, ami viszont csökkentenie kell az intrakraniális nyomást, mérsékelni a neurológiai elégtelenséget, és biztosítania kell a szükséges bioanyagot a kutatáshoz.
- A műtétet egy speciális idegsebészeti osztályon vagy klinikán végzik, amelynek szakemberei tapasztalattal rendelkeznek a neuroonkológiai beavatkozásokban.
- A sebész műanyag csonttrepanációval végez hozzáférést a feltételezett glioma lokalizációjának területén.
- Ha a daganat anatómiailag motoros területek vagy pályák közelében, illetve a magokban vagy az agyidegek mentén helyezkedik el, intraoperatív neurofiziológiai monitorozást alkalmaznak.
- Neuronavigaciós rendszerek, intraoperatív fluoreszcens navigáció 5-aminolevulénsavval kívánatos a daganat eltávolításának maximalizálása érdekében.
- A beavatkozás után az 1-2. napon kontroll CT vagy MRI vizsgálatot végzünk (kontrasztanyag injekcióval vagy anélkül).
Ha a glioma sebészeti reszekciója lehetetlen, vagy kezdetben nem megfelelőnek bizonyult, vagy ha a központi idegrendszer limfómájának gyanúja merül fel, biopsziát (nyitott, sztereotaktikus, navigációs monitorozással stb.) végeznek. |
Az agyi gliomatózisban szenvedő betegeket sztereotaktikus biopsziával igazolják, mivel a terápiás taktika nagymértékben függ a szövettani képtől. |
Bizonyos helyzetekben - idős betegeknél, súlyos neurológiai rendellenességek esetén, glioma törzsben és más létfontosságú részekben történő lokalizációja esetén - a kezelést általános orvosi konzultáció után a tünetek és a képalkotó információk alapján tervezik meg. |
Piloid asztrocitómában, valamint agytörzs-daganatok noduláris formáiban és exofitikus folyamatokban szenvedő betegeknél reszekciót vagy nyílt biopsziát javasolnak. |
Diffúz pontin gliomában és a törzs egyéb diffúz daganataiban szenvedő betegeket sugárterápiával és daganatellenes gyógyszeres terápiával kezelik. Ilyen esetekben nincs szükség ellenőrzésre. |
A kvadriplegikus lemezes gliomában szenvedő betegek az agyi hidrokéle eltávolítása után szisztematikus mágneses rezonancia vizsgálaton és klinikai megfigyelésen esnek át. Ha a daganat növekedési jeleket mutat, további besugárzással eltávolítják. |
Alacsony malignus glioma részleges reszekciója vagy biopsziája esetén a két vagy több kockázati tényezővel rendelkező betegeket szükségszerűen sugárkezeléssel és/vagy kemoterápiával kezelik. |
A szubependimális óriássejtes asztrocitómában szenvedő betegeknél kötelező a teljes reszekció. |
Az everolimuszt diffúz szubependimális óriássejtes asztrocitóma kezelésére írják fel. |
A piloid asztrocitómát a beavatkozás után mágneses rezonancia képalkotással kell eltávolítani, hogy tisztázzuk a daganatszövet radikális reszekciójának minőségét. |
Glioblasztóma esetén a posztoperatív terápiát (sugárterápia + kemoterápia) Temozolomide adagolásával kell kombinálni. |
Anaplasztikus asztrocitóma esetén műtét után sugárterápiát javallottak további gyógyszeres terápiával. Lomustint és Temozolomidot használnak. |
Az anaplasztikus oligodendrogliómában vagy oligoasztrocitómában szenvedő betegek a műtét után mind sugárkezelést, mind kemoterápiát (Temozolomide vagy PCV monoterápia) kapnak. |
Az idős, kiterjedt, magas malignitású gliomában szenvedő betegeket hipofrakcionált módon besugározzák, vagy Temozolomide monoterápiát alkalmaznak. |
Glioma kiújulása esetén a reoperáció lehetőségét és a későbbi kezelési taktikát szakorvosi konzílium vitatja meg. A kiújulás optimális kezelési módja: reoperáció + szisztémás kemoterápia + ismételt sugárkezelés + palliatív intézkedések. Ha a kiújuló tumor növekedésének kisebb, lokalizált területei vannak, radiosebészeti beavatkozás alkalmazható. |
A kiújuló glioma növekedésének kezelésére választott gyógyszerek a temozolomid és a bevacizumab. |
A temozolomid kezelés indikációja a rendkívül rosszindulatú oligodendrogliómák és anaplasztikus asztrocitómák kiújulása. |
A pleomorf xanthoastrocytomát kötelező adjuváns kemoterápia nélkül távolítják el. |
A gliómák egyik sajátossága a kezelésük és eltávolításuk nehézsége. A sebész célja a daganat szöveteinek lehető legteljesebb eltávolítása, az állapot kompenzálása érdekében. Sok betegnek sikerül javítania az életminőségét és meghosszabbítania azt, de a nagyon rosszindulatú daganatok esetében a prognózis továbbra is kedvezőtlen: megnő a kóros góc újbóli növekedésének valószínűsége.
Táplálkozás az agyi glióma esetén
A rosszindulatú daganatos betegek étrendje fontos szempont, amelyre sajnos sokan nem fordítanak kellő figyelmet. Eközben az étrend változásainak köszönhetően lelassítható a glióma fejlődése, erősíthető és megrendült immunitás.
Az étrendi változtatás főbb területei:
- Az anyagcsere-folyamatok normalizálása, az immunvédelem erősítése;
- A szervezet méregtelenítése;
- Energiapotenciál optimalizálása;
- A test minden szervének és rendszerének normális működésének biztosítása ilyen nehéz időszakban.
Racionális és kiegyensúlyozott étrendre van szükség mind a rosszindulatú daganatok korai stádiumában, mind a glioblasztóma utolsó stádiumában szenvedő betegeknél. A gondosan összeállított étrend hozzájárul az általános közérzet javulásához, a sérült szövetek regenerálódásához, ami különösen fontos a citosztatikus és sugárkezelés hátterében. A tápanyag-összetevők egyensúlya és a megfelelő anyagcsere-folyamatok megakadályozzák a fertőző gócok kialakulását, blokkolják a gyulladásos reakciókat, és megelőzik a szervezet kimerülését.
A következő ételek és italok ajánlottak agyi glióma esetén:
- Piros, sárga és narancssárga színű gyümölcsök és zöldségek (paradicsom, őszibarack, sárgabarack, sárgarépa, cékla, citrusfélék), amelyek karotinoidokat tartalmaznak, amelyek védik az egészséges sejteket a sugárterápia negatív hatásaitól;
- Káposzta (karfiol, brokkoli, kelbimbó), retek, mustár és más növényi termékek, amelyek indolt tartalmaznak - egy hatóanyagot, amely semlegesíti a káros toxikus és kémiai tényezőket;
- Zöldek (kapor, petrezselyem, fiatal pitypang- és csalánlevél, rebarbara, rukkola, spenót), zöldborsó és spárga, spárgabab, valamint algák (tengeri moszat, spirulina, chlorella);
- Zöld tea;
- Fokhagyma, hagyma, ananász, amelyek daganatellenes és méregtelenítő képességgel rendelkeznek;
- Korpa, gabonafélék, teljes kiőrlésű kenyér, hüvelyesek, gabonafélék és magvak csíráztatott kelei;
- Sötét szőlő, málna, eper és eper, áfonya, szeder, gránátalma, ribizli, fekete ribizli, madárberkenye, áfonya, homoktövis, cseresznye és más bogyós gyümölcsök, amelyek természetes antioxidánsokat tartalmaznak, amelyek csökkentik a szabad gyökök, vírusok és rákkeltő anyagok negatív hatásait;
- Alacsony zsírtartalmú tejtermékek.
Ne terhelje az emésztőrendszert és az egész testet nehéz és zsíros ételekkel. Hasznos frissen facsart házi készítésű gyümölcsleveket, turmixokat, falatkákat használni. Az ételekhez omega-3 zsírsavforrásokat, például halolajat, lenmagolajat vagy lenmagot kell hozzáadni.
Jobb, ha teljesen elkerüljük a cukrot és az édességeket. De egy kanál méz egy csésze vízzel nem fog ártani: a méhészeti termékek kifejezett gyulladáscsökkentő, antioxidáns és daganatellenes hatásúak. A méz használatának egyetlen ellenjavallata a termékre való allergia.
Az étrendből ki kell zárni:
- Hús, disznózsír, belsőség;
- Vaj, zsíros tejtermékek;
- Füstölt hús, kolbász, húskonzerv és hal;
- Alkohol bármilyen formában;
- Édességek, péksütemények, torták és sütemények, cukorkák és csokoládék;
- Kényelmes ételek, gyorséttermi ételek, rágcsálnivalók;
- Sült ételek.
Naponta elegendő zöldséget, gyümölcsöt, zöldséget és tiszta vizet kell fogyasztani.
A kemoterápia alatt és azt követően egy ideig házi készítésű zöldség- és gyümölcsleveket kell inni, házi készítésű, alacsony zsírtartalmú túrót, tejet és sajtot kell fogyasztani. Fontos a bőséges folyadékfogyasztás, a fogmosás és a gyakori szájöblítés (naponta körülbelül négyszer).
Optimális étkezés agyi gliómás betegek számára:
- Zöldséges rakott ételek;
- Gabonafélékből készült köretek és levesek (lehetőleg hajdina, zabpehely, rizs, kuszkusz, bulgur);
- Gőzölt sajttorták, pudingok, rakott ételek;
- Párolt és sült zöldségek;
- Pörköltek, zöldséglevesek, hüvelyesekből (beleértve a szóját is) készült első és második ételek, pástétomok és felfújtak;
- Turmixok, zöld tea, kompótok és falatkák.
Megelőzés
Ha valaki egészséges életmódot folytat, és rokonai között nem fordult elő rákos megbetegedés, akkor minden esélye megvan arra, hogy ne kapjon agyi gliómát. Az ilyen daganatok specifikus megelőzése nincs, ezért a fő megelőző pontok a megfelelő táplálkozás, a testmozgás, a rossz szokások kerülése, a foglalkozási és háztartási veszélyek hiánya.
A szakértők számos egyszerű, de hatékony ajánlást adnak:
- Igyál több tiszta vizet, kerüld az édesített üdítőket, a csomagolt gyümölcsleveket, az energiaitalokat és az alkoholt.
- Kerülje a foglalkozási és háztartási veszélyeket: kevesebb érintkezés vegyszerekkel, maró oldatokkal és folyadékokkal.
- Próbáljon meg főzni, párolni, sütni, de ne olajban sütni. Részesítse előnyben az egészséges, minőségi, házi készítésű ételeket.
- Az étrend nagy részét növényi ételeknek kell kitenniük, beleértve a zöldségeket is, az évszaktól függetlenül.
- Egy másik negatív tényező a túlsúly, amitől meg kell szabadulni. A testsúlyszabályozás nagyon fontos az egész test egészsége szempontjából.
- A növényi olajokat mindig előnyben kell részesíteni a vajjal és a disznózsírral szemben.
- Ha lehetséges, kívánatos előnyben részesíteni a környezetbarát termékeket, a hormonmentes húst, a nitrát- és növényvédőszer-mentes zöldségeket és gyümölcsöket. Jobb teljesen elkerülni a vörös húst.
- Ne szedjen multivitamin készítményeket javallatok nélkül és nagy mennyiségben. Ne szedjen semmilyen gyógyszert orvosi rendelvény nélkül: az öngyógyítás gyakran nagyon-nagyon veszélyes.
- Ha gyanús tünetek jelentkeznek, orvoshoz kell fordulni, anélkül, hogy megvárnánk a helyzet súlyosbodását, a káros hatások és szövődmények kialakulását.
- Az édességek és a magas glikémiás indexű ételek nemkívánatos összetevői az étrendnek.
- Minél korábban fordul valaki orvoshoz, annál jobbak a gyógyulás esélyei (és ez szinte minden betegségre vonatkozik, beleértve az agyi gliómát is).
Az onkopatológia kialakulásának megelőzése érdekében elegendő időre van szükség az alváshoz és a pihenéshez, kerülni kell az alkoholtartalmú italok túlzott fogyasztását, előnyben kell részesíteni a kiváló minőségű természetes ételeket, csökkenteni kell a kütyük (különösen a mobiltelefonok) használatát.
A daganatos betegségek gyakran előfordulnak időseknél és idős embereknél. Ezért fontos, hogy már fiatal kortól odafigyeljünk az egészségünkre, és ne provokáljunk kóros folyamatokat egészségtelen életmóddal és egészségtelen szokásokkal.
Az onkológia pontos kiváltó okait még nem tisztázták. Természetesen bizonyos szerepet játszanak a kedvezőtlen munkahelyi és környezeti feltételek, az ionizáló és elektromágneses sugárzásnak való kitettség, valamint a hormonális változások. Ne tartózkodjon sokáig és rendszeresen a napon, ne engedje a környezeti hőmérséklet hirtelen változását, ne hevüljön túl a fürdőben vagy a szaunában, és ne vegyen gyakran forró fürdőt vagy zuhanyt.
Egy másik kérdés: hogyan előzhető meg az agyi glióma kiújulása a sikeres kezelés után? A daganat növekedésének kiújulása egy összetett és sajnos gyakori szövődmény, amelyet nehéz előre megjósolni. A betegeknek javasolható a rendszeres megelőző vizsgálatok és szűrővizsgálatok elvégzése, az onkológus és a kezelőorvos legalább évi kétszeri felkeresése, az egészséges életmód, az egészséges és természetes ételek fogyasztása, a mérsékelt fizikai aktivitás. További feltétel az élet szeretete, az egészséges optimizmus, a sikerhez való pozitív hozzáállás bármilyen körülmények között. Ez magában foglalja a barátságos légkört a családban és a munkahelyen, a türelmet és a feltétel nélküli támogatást a szeretteiktől.
Előrejelzés
Az agy állapota és a glioma jellemzői a kimutatásakor ugyanúgy befolyásolják a túlélési arányt, mint az alkalmazott kezelés. A beteg kielégítő általános egészségi állapota és életkora javítja a prognózist (a prognózis fiatal betegeknél optimistább). Fontos mutató a daganat szövettani képe. Így az alacsony malignitású gliómák jobb prognózissal rendelkeznek, mint az anaplasztikus gliómák, és még inkább a glioblasztómák (a legkedvezőtlenebb daganatos folyamatok). Az asztrocitómák prognózisa rosszabb, mint az oligodendrogliómáké.
A rosszindulatú asztrocitómák rosszul reagálnak a terápiára, és viszonylag alacsony, hat-öt év túlélési arányuk van. Ugyanakkor az alacsony malignitású gliómák várható élettartama 1-10 évre becsülhető.
A rosszindulatú asztrocitómák lényegében gyógyíthatatlanok. A kezelés iránya általában a neurológiai tünetek (beleértve a kognitív diszfunkciót is) csökkentését és a várható élettartam növelését foglalja magában, miközben a lehető legmagasabb életminőséget fenntartja. A tüneti terápiát a rehabilitációs intézkedések hátterében vonzzák. A pszichológus munkája is fontos.
Az elmúlt évtizedben a tudósok némi előrelépést tettek az agydaganatok természetének és kezelésének megértésében. Sokkal többet kellene tenni a betegség prognózisának optimalizálása érdekében. A szakemberek elsődleges feladata ma a következő: az agyi gliómának több rendszerrel kell rendelkeznie a probléma hatékony megszüntetésére egyszerre, mind a fejlődés korai, mind a későbbi szakaszaiban.

