A cikk orvosi szakértője
Új kiadványok
A diftéria okai és patogenezise
Utolsó ellenőrzés: 04.07.2025

Minden iLive-tartalmat orvosi szempontból felülvizsgáltak vagy tényszerűen ellenőriznek, hogy a lehető legtöbb tényszerű pontosságot biztosítsák.
Szigorú beszerzési iránymutatásunk van, és csak a jó hírű média oldalakhoz, az akadémiai kutatóintézetekhez és, ha lehetséges, orvosilag felülvizsgált tanulmányokhoz kapcsolódik. Ne feledje, hogy a zárójelben ([1], [2] stb.) Szereplő számok ezekre a tanulmányokra kattintható linkek.
Ha úgy érzi, hogy a tartalom bármely pontatlan, elavult vagy más módon megkérdőjelezhető, jelölje ki, és nyomja meg a Ctrl + Enter billentyűt.
A diftéria a toxingén fertőző betegségek egyik paradigmája. 1883-ban Klebs bebizonyította, hogy a Corynebacterium diphtheriae a diftéria kórokozója. Egy évvel később Loeffler felfedezte, hogy a mikroorganizmus csak az orrgarati üregből tenyészthető, és azt feltételezte, hogy a belső szervek károsodását egy oldható toxin okozza. 1888-ra Roux és Yersin kimutatták, hogy a C. diphtheriae steril szűrletével injektált állatokban az emberi diftéria tüneteitől megkülönböztethetetlen szervpatológia alakult ki; ez azt mutatta, hogy egy erős exotoxin volt a fő virulenciafaktor.
A diftéria leggyakrabban felső légúti fertőzés, amely lázat, torokfájást és rossz közérzetet okoz. A fertőzés helyén/helyein gyakran vastag, szürkészöld fibrin membrán, egy álmembrán alakul ki a baktériumok szaporodásának, a toxintermelésnek, az alapul szolgáló szövetek elhalásának és a gazdaszervezet immunválaszának együttes hatásának eredményeként. Annak felismerése, hogy a szisztémás szervkárosodást a diftéria toxin hatása okozza, mind az akut fertőzés kezelésére szolgáló hatékony antitoxin alapú terápia, mind a rendkívül hatékony toxoid vakcina kifejlesztéséhez vezetett.
Bár a toxoidos immunizáció ritka betegséggé tette a diftériát azokon a területeken, ahol a közegészségügyi előírások előírják a védőoltást, a diftéria járványai továbbra is előfordulnak az oltatlan és legyengült immunrendszerű csoportokban. Ezzel szemben azokon a területeken, ahol felfüggesztették az aktív immunizációs programokat, széles körű, járványszerű diftéria-járványok fordultak elő.
Más típusú korinebaktériumok
A C. diphtheriae, a C. ulcerans és a C. pseudotuberculosis mellett a C. pseudodiphtheriticum és a C. xerosis is okozhat esetenként orrgarati és bőrfertőzéseket. Az utóbbi két törzs a pirazinamidáz termelésére való képességéről ismerhető fel. Az állatgyógyászatban a C. renale és a C. kutscheri fontos kórokozók, amelyek szarvasmarhákban pyelonephritist, egerekben pedig lappangó fertőzéseket okoznak.
Okoz
A diftéria kórokozója, a Corynebacterium diphtheriae, egy vékony, enyhén ívelt pálcika, amelynek végein klubszerű megvastagodások vannak, mozdulatlan; nem képez spórákat, kapszulákat vagy ostorok, és Gram-pozitív.
A toxin mellett a diftéria korinebaktériumok életfolyamataik során neuraminidázt, hialuronidázt, hemolizint, nekrotizáló és diffúz faktorokat termelnek, amelyek a kötőszövet fő anyagának nekrózisát és elfolyósodását okozhatják.
A toxinképzési képességük alapján a diftéria korinebaktériumokat toxingén és nem toxingén csoportra osztják.
A diftéria toxin egy erős bakteriális exotoxin, amely meghatározza a betegség általános és lokális klinikai tüneteit is. A toxingenitás genetikailag meghatározott. A diftéria nem toxinképző korinebaktériumai nem okozzák a betegséget.
Kulturális és morfológiai jellemzők alapján az összes diftéria korinebaktérium 3 változatra oszlik: gravis, mitis és intermedius. A betegség súlyossága nem függ közvetlenül a diftéria korinebaktérium változatától. Minden változat tartalmaz toxingén és nem toxingén törzseket. Minden változat toxingén korinebaktériuma azonos toxint termel. [ 1 ]
Szerkezet, osztályozás és antigéntípusok
A Corynebacterium diphtheriae egy Gram-pozitív, mozdulatlan, bunkó alakú pálcika. A szövetekben vagy régebbi in vitro tenyészetekben növekvő törzsek finom foltokat tartalmaznak a sejtfalakban, amelyek elszíntelenedést tesznek lehetővé a Gram-festés során, és változó Gram-reakciót eredményeznek. A régebbi tenyészetek gyakran tartalmaznak metakromatikus granulátumokat (polimetafoszfát), amelyek metilénkékkel kékes-lilára festődnek. A sejtfalcukrok közé tartozik az arabinóz, a galaktóz és a mannóz. Ezenkívül izolálható a trehalóz toxikus 6,6'-észtere, amely ekvimoláris koncentrációban tartalmaz korinemikolsavat és korinemikolénsavat. Három különböző tenyészettípust ismerünk: mitis, intermedius és gravis.
A legtöbb törzs növekedéséhez nikotin- és pantoténsavra van szükség; egyeseknek tiaminra, biotinra vagy pimelinsavra is szükségük van. Az optimális diftériatoxin-termeléshez a táptalajt aminosavakkal kell kiegészíteni, és félre kell tenni.
Loeffler már 1887-ben leírta az avirulens (nem toxingén) C. diphtheriae izolálását, amelyek megkülönböztethetetlenek voltak az egészséges egyénekből betegekből izolált virulens (toxingén) törzsektől. Ma már elismert tény, hogy a C. diphtheriae avirulens törzsei virulens fenotípussá alakulhatnak fertőzés és a diftéria toxin strukturális génjét, a tox-ot hordozó számos különböző korinebakteriofág egyike általi lizogenizáció után. Az avirulens virulens fenotípussá való lizogén átalakulása in situ és in vitro is előfordulhat. A diftéria toxin strukturális génje nem elengedhetetlen sem a korinebakteriofág, sem a C. diphtheriae számára. Ezen megfigyelés ellenére a diftéria toxin genetikai sodródását nem figyelték meg.
Pathogenezis
A fertőzés bejutási pontjai a szájgarat, az orr, a gége nyálkahártyái, ritkábban a szem és a nemi szervek nyálkahártyája, valamint sérült bőr, seb- vagy égési felületek, pelenkakiütés, be nem gyógyult köldökzsinórseb. A bejutási ponton a diftéria corynebaktérium szaporodik és exotoxint választ ki.
A fibrinogénben gazdag váladék a hámsejtek nekrózisa során felszabaduló trombokináz hatására kiürül és fibrinné alakul. Fibrines film képződik - a diftéria jellegzetes jele.
A diftéria endémiás régióiban gyakori a tünetmentes orrgarati hordozás. Fogékony egyéneknél a toxin tartalmú törzsek a diftéria toxin orrgarati vagy bőrelváltozásokban történő replikációjával és kiválasztásával okoznak betegséget. A diftéria elváltozást gyakran fibrinből, baktériumokból és gyulladásos sejtekből álló álhártya borítja. A diftéria toxin proteolitikusan két fragmensre hasítható: N-terminális A fragmensre (katalitikus domén) és B fragmensre (transzmembrán és receptorkötő domének). Az A fragmens katalizálja az elongációs faktor 2 NAD+-függő ADP-ribozilációját, ezáltal gátolja a fehérjeszintézist az eukarióta sejtekben. A B fragmens egy sejtfelszíni receptorhoz kötődik, és elősegíti az A fragmens citoszolba juttatását.
A védő immunitás magában foglalja a diftéria toxinnal szembeni antitestválaszt klinikai betegség után, vagy a diftéria toxinnal (formaldehid által inaktivált toxin) szembeni antitestválaszt immunizálás után.
Gyarmatosítás
Keveset tudunk a C. diphtheriae kolonizációját közvetítő tényezőkről. Az azonban egyértelmű, hogy a diftéria toxin termelésén kívül más tényezők is hozzájárulnak a virulenciához. Epidemiológiai vizsgálatok kimutatták, hogy egy adott lizotípus hosszú ideig fennmaradhat egy populációban. Később egy másik lizotípus válthatja fel. Egy új lizotípus megjelenése és azt követő dominanciája egy populációban feltehetően összefügg azzal a képességével, hogy hatékonyan kolonizálja és versenyezzen az orrgarati ökológiai niche szegmensében. A Corynebacterium diphtheriae képes neuraminidázt termelni, amely a sejtfelszíni sziálsavat piruvátra és N-acetilneuraminsavra bontja. A kordfaktor (6,6'-di-O-mikoloil-α, α'-D-trehalóz) a C. diphtheriae felszíni komponense, de az emberi gazdaszervezet kolonizációjában betöltött szerepe nem egyértelmű.
Diftéria toxinok termelése
A diftéria toxin strukturális génje, a tox, a szorosan rokon korinebakteriofágok családjába tartozik, amelyek közül a β-fág a legjobban tanulmányozott. A diftéria toxin expressziójának szabályozását egy vas által aktivált represszor, a DtxR közvetíti, amelyet a C. diphtheriae genom kódol. A toxin expressziója a C. diphtheriae fiziológiai állapotától függ. Olyan körülmények között, amikor a vas válik a növekedési sebességet korlátozó szubsztráttá, a vas disszociál a DtxR-ről, a toxikodendron gén aktiválódik, és a diftéria toxin szintetizálódik és maximális sebességgel szekretálódik a táptalajba.
A diftéria toxin szokatlanul erős; az érzékeny fajok (pl. emberek, majmok, nyulak, tengerimalacok) számára már 100-150 ng/testtömegkg dózis is halálos. A diftéria toxin egyetlen, 535 aminosavból álló polipeptidláncból áll. A biokémiai, genetikai és röntgen szerkezeti elemzések azt mutatják, hogy a toxin három szerkezeti/funkcionális doménből áll:
- N-terminális ADP-riboziltranszferáz (katalitikus domén);
- egy régió, amely elősegíti a katalitikus domén sejtmembránon keresztüli átjutását (transzmembrán domén);
- eukarióta sejtreceptor-kötő domén.
Enyhe tripszines emésztést és denaturáló körülmények között történő redukciót követően a diftéria toxin specifikusan hasítható a proteáz-érzékeny hurokjánál két polipeptid fragmensre (A és B). Az A fragmens a toxin N-terminális 21 kDa-os komponense, és tartalmazza az elongációs faktor 2 (EF-2) ADP-ribozilációjának katalitikus helyét.
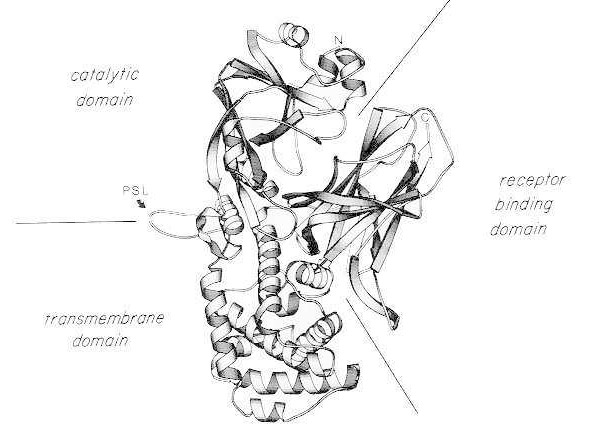
A monomer natív diftéria toxin röntgenkristályszerkezetének szalagdiagramja. (módosítva Bennett MJ, Choe S, Eisenberg D: Doméncsere: Összefonódó allianciák a fehérjék között. Proc Natl Acad Sci, USA, 91: 3127, 1994 alapján). A katalitikus, transzmembrán és receptorkötő domének relatív helyzete látható. Az ép toxint tripszinszerű proteázok hasíthatják az Arg190, Arg192 és/vagy Arg193 aminosavakon, amelyek a proteázérzékeny hurokban (PSL) helyezkednek el. A Cys186 és Cys201 közötti diszulfidhíd redukcióját követően a toxin A és B fragmensekre bontható. Az ép toxin amino-terminálisa (N) és karboxi-terminálisa (C) látható. A szalagdiagramot a MOLESCRIPT programmal készítettük.
A C-terminális fragmens, a B fragmens, a toxin transzmembrán és receptorkötő doménjeit hordozza.
Egyetlen eukarióta sejt diftéria toxinnal történő mérgezése legalább négy különálló lépésből áll:
- a toxin kötődése a sejtfelszínen található receptorához;
- a töltött receptorok bevonatos gödrökbe csoportosulása és a toxin internalizációja receptor-közvetített endocitózissal; az endocitikus vezikula membránhoz kapcsolódó, ATP-vezérelt protonpumpa általi savasítását követően,
- a transzmembrán domén beépülése a membránba és a katalitikus domén citoszolba juttatásának elősegítése, és
- Az EF-2 ADP-ribozilációja, ami a fehérjeszintézis visszafordíthatatlan elnyomásához vezet.
Kimutatták, hogy a katalitikus domén egyetlen molekulája, amelyet a citoszolba juttatnak, elegendő ahhoz, hogy halálos legyen a sejtre.
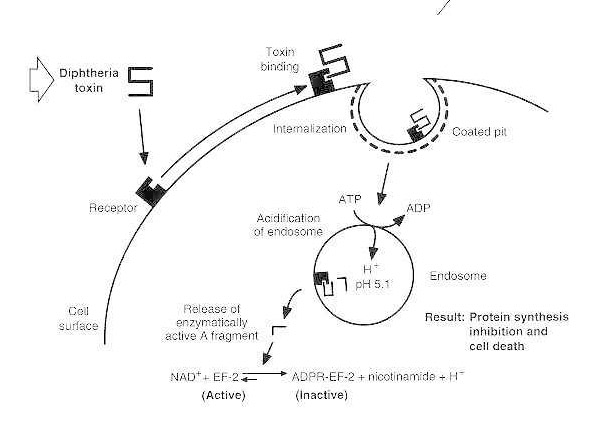
Diftéria-mérgezés vázlatos rajza egy fogékony eukarióta sejtben.
A toxin a sejtfelszíni receptorához kötődik, és receptor-közvetített endocitózissal internalizálódik; az endoszóma savasodásakor a transzmembrán domén beépül a vezikula membránjába; a katalitikus domén a citoszolba jut, ami a fehérjeszintézis gátlásához és a sejthalálhoz vezet.
Járványtan
Az amerikai lakosság diftéria toxoiddal történő tömeges immunizálása előtt a diftéria általában gyermekkori betegség volt. A diftéria toxoiddal történő tömeges immunizálás egyik figyelemre méltó aspektusa, hogy ahogy a lakosság azon százalékos aránya, amely rendelkezik védő antitoxin immunitással (≥ 0,01 NE/ml), úgy csökken a toxingén törzsek izolálásának gyakorisága a lakosságból. Ma az Egyesült Államokban, ahol a klinikai diftéria szinte teljesen eltűnt, a C. diphtheriae toxingén törzseinek izolálása ritka. Mivel a szubklinikai fertőzés már nem biztosít kitettséget a diftéria antigénnel, és hacsak nem erősítik meg az antitoxinnal szembeni immunitást, a felnőttek nagy százalékának (30-60%-ának) az antitoxin szintje a védő szint alatt van, és veszélyben vannak. Az Egyesült Államokban, Európában és Kelet-Európában a diftéria legújabb kitörései elsősorban az alkohol- és/vagy drogfüggők körében fordultak elő. Ezen a csoporton belül a toxingén C. diphtheriae hordozói mérsékelten magas antitoxin immunitással rendelkeznek. Az oroszországi közegészségügyi intézkedések közelmúltbeli összeomlása miatt a diftéria járványossá vált. 1994 végére több mint 80 000 esetet és több mint 2000 halálesetet jelentettek Oroszországban.
A diftéria gócos kitörései szinte mindig egy olyan immunhordozóhoz kapcsolódnak, aki olyan régióból tért vissza, ahol a diftéria endémiás. Valójában az Egyesült Államokban és Európában a közelmúltban kitört klinikai diftéria-kitörések Oroszországból és Kelet-Európából visszatérő utazókkal hozhatók összefüggésbe. A C. diphtheriae toxingén törzsei közvetlenül emberről emberre terjednek levegőben lévő cseppek útján. Ismert, hogy a toxingén törzsek közvetlenül kolonizálhatják az orrgarati üreget. Ezenkívül a toxingén gén közvetve is terjedhet toxingén korinebakteriofág felszabadulásával és a nem toxingén autochton C. diphtheriae in situ lizogén transzformációjával. [ 5 ]
A C. diphtheriae izolátumok biotípus- és lizotípus-meghatározása mellett ma már molekuláris biológiai technikák is alkalmazhatók a diftéria-járványok tanulmányozására. A C. diphtheriae kromoszómális DNS-ének restrikciós endonukleázos emésztési mintázatait használták klinikai járványok tanulmányozására, akárcsak a klónozott korinebakteriális inszerciós szekvenciák genetikai próbaként való alkalmazását.
A Schick-tesztet évek óta használják a diftéria toxinnal szembeni immunitás felmérésére, bár ma már sok területen felváltotta a diftéria toxinnal szembeni specifikus antitestek szerológiai tesztje. A Schick-teszt során kis mennyiségű diftéria toxint (körülbelül 0,8 ng 0,2 ml-ben) injektálnak intradermálisan az alkarba (teszthely), és 0,0124 μg diftéria toxint 0,2 ml-ben injektálnak intradermálisan a kontrollhelyre. A leolvasásokat 48 és 96 óra elteltével végzik. A nem specifikus bőrreakciók általában 48 óra elteltével tetőznek. 96 óra elteltével a teszthelyen esetlegesen előforduló eritémás reakció és némi nekrózis azt jelzi, hogy az antitoxikus immunitás nem elegendő a toxin semlegesítéséhez (≤ 0,03 NE/ml). A teszt- és a kontrollterületen 48 óra elteltével fellépő gyulladás az antigénkészítményre adott túlérzékenységi reakciót jelzi.
Forms
A Corynebacterium diphtheriae az orrgaratot vagy a bőrt fertőzi meg. A toxinképző törzsek erős exotoxint termelnek, amely diftériát okozhat. A diftéria tünetei közé tartozik a torokgyulladás, láz és a nyak vagy a bőrelváltozás körüli terület duzzanata. A diftéria okozta elváltozásokat álhártya borítja. A toxin a véráramon keresztül terjed a távoli szervekbe, és bénulást és pangásos szívelégtelenséget okozhat. [ 6 ]
A klinikai diftéria két típusa létezik: az orr-garatdiftéria és a bőrdiftéria. A garatdiftéria tünetei az enyhe torokgyulladástól a légutak álhártya okozta elzáródása miatti hipoxiáig terjednek. A nyaki nyirokcsomók érintettsége a nyak súlyos duzzanatát okozhatja (bikanyak-diftéria), és a beteg lázzal járó tüneteket tapasztalhat (≥ 38°C). A bőrdiftéria esetén a bőrelváltozásokat általában szürkésbarna álhártya borítja. A diftéria toxin perifériás motoros neuronokra és a szívizomra gyakorolt hatása következtében életveszélyes szisztémás szövődmények, főként a motoros funkciók elvesztése (pl. nyelési nehézség) és pangásos szívelégtelenség alakulhatnak ki.
Ellenőrzés
A diftéria elleni védekezés a megfelelő diftéria toxoiddal történő immunizálástól függ: ez a diftéria toxin formaldehiddel inaktivált, antigén szempontjából ép marad. A toxoidot úgy állítják elő, hogy a diftéria toxint formaldehiddel inkubálják 37°C-on, lúgos körülmények között. A diftéria elleni immunizálást az élet második hónapjában kell elkezdeni három alapoltásból álló sorozattal, 4-8 hetes időközönként, majd egy negyedik adaggal az utolsó alapoltás után körülbelül 1 évvel. A diftéria toxoidot széles körben alkalmazzák a diftéria-pertussis-tetanus (DPT) vakcina összetevőjeként. Epidemiológiai vizsgálatok kimutatták, hogy a diftéria elleni immunizálás körülbelül 97%-os hatékonyságú. Bár az Egyesült Államokban és Európában tömeges diftéria elleni immunizálás folyik, és a gyermekkori immunizációs arány megfelelő, a felnőtt lakosság nagy részénél az antitest titerek a védőszint alatt lehetnek. A felnőtteket 10 évente diftéria toxoiddal kell újraoltani. Valóban, diftéria-tetanusz toxoiddal történő emlékeztető oltást kell adni azoknak, akik olyan területekre utaznak, ahol magas az endémiás diftéria aránya (Közép- és Dél-Amerika, Afrika, Ázsia, Oroszország és Kelet-Európa). Az elmúlt években a nagy tisztaságú toxoid készítmények immunizálásra való alkalmazása minimalizálta az alkalmanként előforduló súlyos túlérzékenységi reakciókat. diftéria-tetanusz toxoiddal történő emlékeztető oltást kell adni azoknak, akik olyan területekre utaznak, ahol magas az endémiás diftéria aránya (Közép- és Dél-Amerika, Afrika, Ázsia, Oroszország és Kelet-Európa). Az elmúlt években a nagy tisztaságú toxoid készítmények immunizálásra való alkalmazása minimalizálta az alkalmanként előforduló súlyos túlérzékenységi reakciókat. diftéria-tetanusz toxoiddal történő emlékeztető oltást kell adni azoknak, akik olyan területekre utaznak, ahol magas az endémiás diftéria aránya (Közép- és Dél-Amerika, Afrika, Ázsia, Oroszország és Kelet-Európa). Az elmúlt években a nagy tisztaságú toxoid készítmények immunizálásra való alkalmazása minimalizálta az alkalmanként előforduló súlyos túlérzékenységi reakciókat.
Bár az antibiotikumokat (például a penicillint és az eritromicint) a diftéria kezelésének részeként alkalmazzák, a diftéria antitoxinnal történő gyors passzív immunizálás a leghatékonyabb a halálozási arány csökkentésében. A specifikus antitoxin hosszú felezési ideje a véráramban fontos tényező a diftéria toxin hatékony semlegesítésében; ahhoz azonban, hogy hatékony legyen, az antitoxinnak reagálnia kell a toxinnal, mielőtt bejuthatna a sejtbe.
Diftéria toxin újratervezése eukarióta receptor-specifikus citotoxinok előállításához
A fehérjemérnökség a molekuláris biológia egy új és gyorsan fejlődő területe; rekombináns DNS-módszereket és szilárd fázisú DNS-szintézist ötvöz olyan kiméra gének tervezéséhez és előállításához, amelyek termékei egyedi tulajdonságokkal rendelkeznek. A diftéria toxin szerkezet-funkció kapcsolatainak vizsgálata egyértelműen kimutatták, hogy ez a toxin egy három doménből álló fehérje: katalitikus, transzmembrán és receptor doménből. Lehetségessé vált a diftéria toxin natív receptorkötő doménjének genetikai helyettesítése különböző polipeptid hormonokkal és citokinekkel (pl. α-melanocita-stimuláló hormon [α-MSH], interleukin (IL) 2, IL-4, IL-6, IL-7, epidermális növekedési faktor). A kapott kiméra fehérjék vagy fúziós toxinok a citokin receptorkötő specificitását ötvözik a toxin transzmembrán és katalitikus doménjeivel. Minden esetben kimutatták, hogy a fúziós toxinok szelektíven csak azokat a sejteket mérgezik, amelyek a megfelelő célreceptort hordozzák. Ezen genetikailag módosított fúziós toxinok közül az elsőt, a DAB 389IL-2-t, jelenleg humán klinikai vizsgálatokban értékelik refrakter limfómák és autoimmun betegségek kezelésére, amelyekben a nagy affinitású IL-2 receptorokkal rendelkező sejtek fontos szerepet játszanak a patogenezisben.[ 7 ] A DAB 389 IL-2 beadása biztonságosnak, jól tolerálhatónak és tartós betegségremissziót kiváltónak bizonyult súlyos mellékhatások nélkül. Valószínű, hogy a diftéria toxinon alapuló fúziós toxinok fontos új biológiai szerré válnak majd specifikus daganatok vagy betegségek kezelésében, amelyekben specifikus sejtfelszíni receptorok célozhatók meg.


 [
[