A cikk orvosi szakértője
Új kiadványok
Fibroelastosis
Utolsó ellenőrzés: 05.07.2025

Minden iLive-tartalmat orvosi szempontból felülvizsgáltak vagy tényszerűen ellenőriznek, hogy a lehető legtöbb tényszerű pontosságot biztosítsák.
Szigorú beszerzési iránymutatásunk van, és csak a jó hírű média oldalakhoz, az akadémiai kutatóintézetekhez és, ha lehetséges, orvosilag felülvizsgált tanulmányokhoz kapcsolódik. Ne feledje, hogy a zárójelben ([1], [2] stb.) Szereplő számok ezekre a tanulmányokra kattintható linkek.
Ha úgy érzi, hogy a tartalom bármely pontatlan, elavult vagy más módon megkérdőjelezhető, jelölje ki, és nyomja meg a Ctrl + Enter billentyűt.
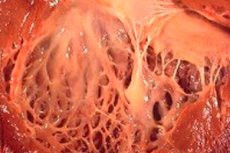
Az orvostudományban a „fibroelasztózis” kifejezés a belső szervek és az erek felszínét borító test kötőszövetének változásaira utal, amelyeket a rugalmas rostok növekedésének zavara okoz. Ugyanakkor a szervek falainak és szerkezeteiknek megvastagodása is megfigyelhető, ami szükségszerűen befolyásolja a test létfontosságú rendszereinek, különösen a szív- és érrendszer, valamint a légzőrendszer működését. Ez viszont a beteg közérzetének romlásához vezet, különösen fizikai megterhelés során, ami befolyásolja az életminőséget és az élet időtartamát.
Járványtan
Általánosságban elmondható, hogy a kötőszövet változásaival járó betegségek, amelyek a belső szervek membránjainak és válaszfalainak megvastagodását eredményezik, két csoportra oszthatók: szívfibroelasztózis és tüdőfibroelasztózis. A szívpatológia lehet veleszületett és szerzett is; a betegség tüdőformájában szerzett betegségről beszélünk.
A tüdőfibroelasztózis középkorban (közelebb az 55-57. évhez) kezd kialakulni, bár az esetek felében a betegség eredetét gyermekkorban kell keresni. Jellemző egy „enyhe” időszak, amikor a betegség tünetei hiányoznak. Ugyanakkor a betegségnek nincsenek nemi preferenciái, és egyformán érintheti mind a nőket, mind a férfiakat. Ezt a meglehetősen ritka patológiát a tüdő pleurájának és parenchymájának (funkcionális sejtjeinek) szöveteiben bekövetkező változások jellemzik, főként a tüdő felső lebenyében. Mivel a betegség etiológiája és patogenezise továbbra sem tisztázott, a betegséget idiopátiás patológiának minősítik. Az orvosi terminológia szerint „pleuroparenchimatózus fibroelasztózisnak” nevezik. [ 1 ]
A szívizom fibroelasztózisa a szívhártyák patológiájának általánosított elnevezése, amelyet megvastagodásuk és csökkent funkcionalitásuk jellemez. A patológia veleszületett formáit a szív belső hártyájának diffúz (széles körű) megvastagodása jellemzi. Ez egy vékony kötőszövet, amely a szív üregét (annak részeit) béleli és billentyűit alkotja.
Felnőtt betegeknél általában a betegség fókuszos formáját diagnosztizálják, amikor a szív belső felülete erősebb és vastagabb szövetek foltjaival borítottnak tűnik (nemcsak túlnőtt rostokat, hanem trombotikus tömegeket is tartalmazhat).
A szívizom fibroelasztózisának eseteinek felében nemcsak a szervfal vastagodik meg, hanem a billentyűk is (a kéthegyű mitrális billentyű a pitvar és az azonos nevű kamra között, a háromhegyű aorta billentyű a bal kamra és az aorta között, a tüdőbillentyű a jobb kamra és a tüdőartéria között). Ez viszont megzavarhatja a billentyűk működését, és az artérianyílás szűkületét okozhatja, amely már amúgy is kicsi a szív más üregeihez képest.
Az orvosi terminológiában az endokardiális fibroelasztózist endocardiális fibroelasztózisnak nevezik (prenatális fibroelasztózis, endocardiális szklerózis, magzati endocarditis stb.). De gyakran a szívhártya középső izomrétege is érintett lehet a folyamatban. [ 2 ]
A szívizom (a szív izomrétege, amely kardiomiocitákból áll) szerkezeti rendellenességei, génmutációk és súlyos fertőző folyamatok okozhatják a fibroelasztózis gyakori formáját, amikor nemcsak az endocardium, hanem a szívizom is érintett. Általában az endocardiumban különböző okok miatt kialakuló diszpláziás folyamatok az izomhártyával való érintkezés határán jelentkeznek, megzavarva a réteg összehúzódási képességét. Bizonyos esetekben a belső réteg benőhet a szívizomba, a kardiomiociták fibroblasztokkal és rostokkal helyettesítődhetnek, ami befolyásolja az idegimpulzusok vezetőképességét és a szív ritmikus munkáját.
A szívizom megvastagodott membránjának vastagságában lévő erek összenyomódása megzavarja a szívizom táplálkozását (miokardiális ischaemia), ami viszont a szívizom szöveteinek nekrózisához vezethet.
A szívizom károsodásával járó endokardiális fibroelasztózist szubendokardiális vagy endomyocardiális fibroelasztózisnak nevezik.
A statisztikák szerint e ritka betegség legtöbb esetben (az újszülöttek teljes számának mindössze 0,007%-ában) a szív bal kamrájának fibroelasztózisát diagnosztizálják, bár egyes esetekben a folyamat a jobb kamrára és a pitvarokra is átterjed, beleértve az azokat elválasztó billentyűket is.
A szív fibroelasztózisát gyakran a nagy, szintén kötőszövettel borított koszorúerek károsodása kíséri. Felnőttkorban gyakran progresszív érelmeszesedés hátterében fordul elő.
A betegséget gyakrabban regisztrálják trópusi afrikai országokban az alacsony életszínvonalú lakosság körében, amit a rossz táplálkozás, a gyakori fertőzések, valamint bizonyos élelmiszerek és növények fogyasztása elősegít.
Az endocardialis megvastagodás a Löffler-féle fibroplasztikus endocarditis utolsó szakaszában is megfigyelhető, amely főként középkorú férfiakat érint. A betegség patogenezise szintén fertőző ágensekkel van összefüggésben, amelyek súlyos eozinofília kialakulását okozzák, ami jellemzőbb a belső parazitafertőzésekre. Ebben az esetben a test szövetei (elsősorban a szívizom és az agy) oxigénhiányt (hipoxiát) kezdenek tapasztalni. A szív fibroelasztózisának és a Löffler-féle rostos endocarditisnek a tünetei hasonlóak, az orvosok teljesen különböző betegségeknek tekintik őket.
Okoz fibroelastosis
A fibroelasztózis a létfontosságú szervek – a szív és a tüdő – kötőszövetének elváltozásaira utal, melyeket a szervműködés zavara kísér, és amelyek a beteg megjelenésében és állapotában is tükröződnek. Az orvosok évtizedek óta tudnak a betegségről. A szív belső nyálkahártyájának (endokardium) fibroelasztózisát már a 18. század elején leírták, a tüdőben bekövetkező hasonló elváltozásokról pedig csak két és fél évszázaddal később kezdtek el beszélni. Az orvosok azonban még nem jutottak végleges megállapodásra a kötőszövet kóros burjánzásának okairól.
Továbbra sem világos, hogy pontosan mi okozza a kötőrostok növekedésének és fejlődésének zavarát. A tudósok azonban azonosítanak bizonyos kockázati tényezőket az ilyen változásokhoz, és ezeket a betegség lehetséges (de nem végleges) okaiként tartják számon.
Így a tüdőfibroelasztózis patogenezisében, amelyet az érett emberek betegségének tekintenek, különleges szerepet kapnak a szerv visszatérő fertőző elváltozásai, amelyek a betegek felében találhatók. A fertőzések a tüdőszövet és a mellhártya gyulladását provokálják, és a hosszú távú gyulladás hajlamosít rostos átalakulásra.
Néhány betegnél családi anamnézisben szerepel fibroelasztózis, ami örökletes hajlamra utal. Szervezetükben nem specifikus autoantitesteket találtak, amelyek bizonytalan etiológiájú, hosszú távú gyulladásos folyamatokat provokálnak.
Létezik egy olyan vélemény, hogy a tüdőszövet rostos elváltozásait a gastrooesophagealis reflux betegség okozhatja. Bár ez a kapcsolat valószínűleg közvetett. Azt is feltételezik, hogy a fibroelasztózis kockázata nagyobb azoknál, akik szív- és érrendszeri betegségekben vagy tüdőtrombózisban szenvednek.
A fiatal és serdülőkorban jelentkező tüdőfibroelasztózis terhesség alatt is jelentkezhet. Általában a betegség körülbelül 10 évig vagy tovább rejtve marad, de korábban is megnyilvánulhat, valószínűleg a várandós anya szervezetére nehezedő fokozott terhelés és a hormonális változások miatt, de pontos magyarázat még nincs. Mindazonáltal a vizsgált reproduktív korú betegek 30%-ánál a betegség kialakulásának hasonló képét figyelték meg.
A terhesség önmagában nem okozhatja a betegséget, de felgyorsíthatja az események kialakulását, ami nagyon szomorú, mert a betegség halálozási aránya nagyon magas, és a fibroelasztózissal várható élettartam rövid.
A legtöbb esetben a szív fibroelasztózisa gyermekkori betegségeknek tulajdonítható. A veleszületett patológiát a prenatális időszakban 4-7 hónapos magzatnál észlelik, de a diagnózis csak a gyermek születése után erősíthető meg. A betegség ezen formájának patogenezisében számos lehetséges negatív tényezőt vesznek figyelembe: az anya magzatra átterjedő fertőző és gyulladásos betegségei, a szívhártyák fejlődési rendellenességei, a szívszövet vérellátásának zavara, genetikai mutációk, oxigénhiány.
Úgy tartják, hogy a fertőzések közül a vírusok járulnak hozzá a legnagyobb patogenetikai szereppel a szívizom fibroelasztózisának kialakulásához, mivel beágyazódnak a szervezet sejtjeibe, elpusztítják azokat és megváltoztatják a szövetek tulajdonságait. A magzat kialakulatlan immunrendszere nem tud védelmet nyújtani ezekkel a kórokozókkal szemben, ellentétben a várandós anya immunitásával. Ez utóbbi esetleg nem tapasztalja a vírusfertőzés következményeit, míg a magzatban a méhen belüli fertőzés különféle rendellenességek megjelenését válthatja ki.
Egyes tudósok úgy vélik, hogy a fibroelasztózis fertőző formájának patogenezisében a döntő szerepet a magzatot legfeljebb 7 hónapos korig érintő fertőzés játssza. Később már csak a szív gyulladásos betegségeit (szívizomgyulladás, szívbelhártya-gyulladás) okozhatja.
A szív membránjainak és billentyűinek fejlődési rendellenességeit mind a gyulladásos folyamat, mind a nem megfelelő autoimmun reakciók kiválthatják, aminek következtében az immunrendszer sejtjei elkezdik támadni a szervezet saját sejtjeit.
A génmutációk a kötőszövet rendellenes fejlődését okozzák, mivel a gének információkat tartalmaznak a fehérjestruktúrák (különösen a kollagén- és elasztinfehérjék) szerkezetéről és viselkedéséről.
A szívizomzat hipoxiája és ischaemiája a rendellenes szívfejlődés következménye lehet. Ebben az esetben másodlagos fibroelasztózisról beszélünk, amelyet veleszületett szívhibák (CHD) okoznak. Ide tartoznak az olyan rendellenességek, amelyek elzáródást (a szív és ereinek károsodott átjárhatóságát) okozzák:
- az aorta szűkülete vagy szűkülete a billentyű közelében,
- az aorta koarktációja vagy szegmentális szűkülete az ív és a leszálló szakasz találkozásánál,
- atresia vagy a természetes nyílás hiánya az aortában,
- a szívszövet fejletlensége (leggyakrabban a bal kamra, ritkábban a jobb kamra és a pitvarok), ami befolyásolja a szív pumpáló funkcióját.
Véleményünk szerint a terhesség alatti toxikózis hajlamosító tényező lehet a magzati fibroelasztózis kialakulására.
A posztnatális időszakban a szívizom fibroelasztózisának kialakulását elősegíthetik a szervmembránok fertőző és gyulladásos betegségei, a sérülések következtében fellépő hemodinamikai zavarok, az érrendszeri tromboembólia, a miokardiális vérzés, az anyagcserezavarok (fokozott fibrinképződés, fehérje- és vasanyagcsere-zavarok: amiloidózis, hemokromatózis). Ugyanezek az okok okozzák a betegség kialakulását felnőtteknél is.
Pathogenezis
A kötőszövet az emberi test speciális szövete, amely szinte minden szerv részét képezi, de nem vesz részt aktívan azok működésében. A kötőszövetnek támasztó és védő funkciókat tulajdonítanak. Egyfajta vázat (vázat, sztrómát) képezve és korlátozva a szerv funkcionális sejtjeit, biztosítja annak végső alakját és méretét. Kellő szilárdsággal a kötőszövet védi a szerv sejtjeit a pusztulástól és a sérülésektől, megakadályozza a kórokozók bejutását, és speciális makrofágsejtek segítségével elnyeli az elavult struktúrákat: az elhalt szövetsejteket, az idegen fehérjéket, a vér salakanyagait stb.
Ez a szövet segédszövetnek nevezhető, mivel nem tartalmaz olyan sejtes elemeket, amelyek biztosítják az egyik vagy másik szerv működését. Mindazonáltal a test életében betöltött szerepe meglehetősen nagy. Az erek membránjainak részeként a kötőszövet biztosítja ezen struktúrák biztonságát és működését, aminek köszönhetően a test belső környezetének környező szöveteinek táplálkozása és légzése (trofizmusa) történik.
A kötőszövetnek több típusa létezik. A belső szerveket borító hártyát laza kötőszövetnek nevezzük. Ez egy félig folyékony, színtelen anyag, amely hullámos kollagénrostokat és egyenes elasztinrostokat tartalmaz, amelyek között véletlenszerűen elszórva különféle típusú sejtek helyezkednek el. Ezen sejtek egy része (fibroblasztok) felelős a rostos szerkezetek kialakulásáért, mások (endoteliociták és hízósejtek) áttetsző kötőszöveti mátrixot alkotnak és speciális anyagokat (heparin, hisztamin) termelnek, mások (makrofágok) fagocitózist biztosítanak stb.
A rostos szövet második típusa a sűrű kötőszövet, amely nem tartalmaz nagyszámú egyedi sejtet, és amely viszont fehérre és sárgára oszlik. A fehér szövet szorosan egymásba illeszkedő kollagénrostokból (szalagok, inak, csonthártya) áll, míg a sárga szövet kaotikusan összefonódó elasztinrostokból, fibroblasztok (szalagok, erek membránjai, tüdő része) zárványaival.
A kötőszövetek közé tartoznak még: a vér, a zsír, a csont és a porcszövet, de ezek minket egyelőre nem érdekelnek, mivel a fibroelasztózis alatt a rostos szerkezetek változásait értjük. Az elasztikus és rugalmas rostok pedig csak a laza és sűrű kötőszövetekben találhatók.
A fibroblasztok szintézise és a belőlük származó kötőszöveti rostok képződése agyi szinten szabályozott. Ez biztosítja a jellemzők (szilárdság, rugalmasság, vastagság) állandóságát. Ha valamilyen kóros ok miatt a segédszövet szintézise és fejlődése zavart szenved (a fibroblasztok száma megnő, "viselkedésük" megváltozik), akkor az erős kollagénrostok elszaporodnak, vagy megváltozik a rugalmasak növekedése (rövidek maradnak, csavarodnak), ami a szervmembrán és egyes kötőszövettel borított belső struktúrák tulajdonságainak megváltozásához vezet. A szükségesnél nagyobb vastagságot kapnak, sűrűbbé, erősebbé és rugalmatlanabbá válnak, a szalagokban és inakban található rostos szövetre hasonlítanak, amelynek nyújtása nagy erőfeszítést igényel.
Az ilyen szövet nem nyúlik jól, korlátozva a szerv mozgását (a szív és az erek automatikus ritmikus mozgása, a tüdő méretének változása belégzés és kilégzés során), ezért a vérellátás és a légzőszervek zavara jelentkezik, ami oxigénhiányhoz vezet.
A tény az, hogy a test vérellátását a szív, amely pumpaként működik, és a vérkeringés két köre végzi. A tüdőkeringés felelős a vérellátásért és a gázcseréért a tüdőben, ahonnan az oxigén a véráramlással a szívbe jut, onnan pedig a szisztémás keringésbe, és eloszlik a testben, biztosítva a szervek és szövetek légzését.
A szívizom összehúzódását korlátozó elasztikus membrán csökkenti a szív működését, amely így nem pumpálja olyan aktívan a vért, és vele együtt az oxigént. A tüdő fibroelasztózisa esetén a szellőzésük (oszcillációjuk) károsodik, és egyértelműen kevesebb oxigén jut be a vérbe, ami még normális szívműködés esetén is hozzájárul a szövetek és szervek oxigénhiányához (hipoxiájához). [ 3 ]
Tünetek fibroelastosis
A szív- és tüdőfibroelasztózis két olyan betegség, amelyet a kötőszövet rostszintézisének zavara jellemez. Különböző lokalizációjúak, de mindkettő potenciálisan életveszélyes, mivel progresszív vagy súlyos szív- és légzési elégtelenséggel jár.
A tüdőfibroelasztózis a légzőrendszer ezen fontos szervének ritka intersticiális betegsége. Ide tartoznak a tüdőparenchyma krónikus patológiái, amelyek az alveoláris falak károsodásával (gyulladás, szerkezetük és szerkezetük felborulása), a tüdőkapillárisok belső bélésével stb. járnak. A fibroelasztózist gyakran a progresszív tüdőgyulladás speciális, ritka formájának tekintik, amely hajlamos a tüdő és a mellhártya szöveteinek rostos változásaira.
A betegséget szinte lehetetlen a legelején kimutatni, mivel körülbelül 10 évig nem feltétlenül emlékezteti magát. Ezt az időszakot tiszta intervallumnak nevezzük. A tüdő térfogatát és a gázcserét még nem befolyásoló kóros elváltozások megjelenése véletlenül, a tüdő részletes vizsgálata során, a légzőrendszer más betegsége vagy sérülése kapcsán észlelhető.
A betegséget a tünetek lassú progressziója jellemzi, így a betegség első megnyilvánulásai jelentősen késhetnek a kezdetétől számítva. A tünetek fokozatosan erősödnek.
A betegség első jelei, amelyekre érdemes odafigyelni, a köhögés és a fokozódó légszomj. Ezek a tünetek gyakran egy korábbi légzőszervi betegség következményei, így hosszú ideig összefüggésben állhatnak egy megfázással és annak következményeivel. A légszomjat gyakran szívbetegségnek vagy életkorral összefüggő változásoknak tekintik. Végül is a betegséget az időskorhoz közeledő embereknél diagnosztizálják.
Hibákat mind a betegek, mind az őket vizsgáló orvosok elkövethetnek, ami egy veszélyes betegség késői felismeréséhez vezet. Érdemes odafigyelni a köhögésre, amely fibroelasztózis esetén improduktív, de a nyákoldók és köptetők nem serkentik, hanem köhögéscsillapítók állítják le. Az ilyen jellegű elhúzódó köhögés a tüdőfibroelasztózis jellegzetes tünete.
A nehézlégzést a tüdőalveoláris falak és a mellhártya megvastagodása, a tüdőalveoláris üregek térfogatának és számának csökkenése okozza, ami progresszív légzési elégtelenséghez vezet (a szerv parenchymája röntgenfelvételen méhsejtként látható). A tünet fizikai megterhelés hatására fokozódik, először jelentős, majd már kis mértékű is. A betegség előrehaladtával súlyosbodik, ami a beteg rokkantságát és halálát okozza.
A fibroelasztózis progresszióját az általános állapot romlása kíséri: a hipoxia gyengeséghez és szédüléshez vezet, a testsúly csökken (étvágytalanság alakul ki), a körömpercek dobverővé válnak, a bőr sápadttá válik és beteges megjelenésű.
A betegek fele nem specifikus tüneteket, például légzési nehézséget és mellkasi fájdalmat tapasztal, amelyek a pneumothoraxra (gázok felhalmozódása a pleurális üregben) jellemzőek. Ez az anomália sérülések, primer és szekunder tüdőbetegségek, nem megfelelő kezelés következtében is előfordulhat, így nem diagnosztizálható.
A szív fibroelasztózisát, valamint a tüdő kötőszöveti növekedésének patológiáját a következők jellemzik: sápadt bőr, fogyás, gyengeség, amely gyakran rohamokban jelentkezik, légszomj. Tartós szubfebrilis hőmérséklet is megfigyelhető megfázás vagy fertőzés jelei nélkül.
Sok betegnél a máj mérete megváltozik. A máj mérete a diszfunkció tünetei nélkül növekszik. A lábak, az arc, a karok és a keresztcsonti régió duzzanata is előfordulhat.
A betegség jellegzetes megnyilvánulása a szívműködés zavarával járó, fokozódó keringési elégtelenség. Ilyenkor tachycardiát (gyakran ritmuszavarral kombinált megnövekedett pulzusszám), légszomjat (beleértve a fizikai aktivitás hiányát is), szöveti cianózist (kékes elszíneződés, amelyet a vérben felhalmozódó karboxihemoglobin, azaz a hemoglobin szén-dioxiddal alkotott vegyületének felhalmozódása okoz a megzavart véráramlás, és ennek megfelelően a gázcsere miatt) diagnosztizálnak.
Ebben az esetben a tünetek jelentkezhetnek közvetlenül a gyermek születése után, vagy egy idő után. Idősebb gyermekek és felnőttek esetében a súlyos szívelégtelenség jelei általában egy légúti fertőzés hátterében jelentkeznek, amely kiváltó okként szolgál. [ 4 ]
Fibroelasztózis gyermekeknél
Ha a tüdőfibroelasztózis felnőttek betegsége, amely gyakran gyermekkorban kezdődik, de sokáig nem jelentkezik, akkor a szív endokardiumának hasonló patológiája gyakran már a baba születése előtt megjelenik, és a születés első pillanataitól kezdve befolyásolja az életét. Ez a ritka, de súlyos patológia a nehezen korrigálható szívelégtelenség kialakulásának oka csecsemőknél, akik közül sokan 2 éven belül meghalnak. [ 5 ]
Az újszülöttek endokardiális fibroelasztózisa a legtöbb esetben a baba testében prenatális korban lezajló kóros folyamatok eredménye. Az anyától kapott fertőzések, a genetikai mutációk, a szív- és érrendszer fejlődésének rendellenességei, örökletes anyagcsere-betegségek - mindez a tudósok szerint a szív membránjainak kötőszövetének megváltozásához vezethet. Különösen akkor, ha egy 4-7 hónapos magzat egyszerre két vagy több tényezőnek van kitéve.
Például a szív és a koszorúerek fejlődésében bekövetkező rendellenességek (szűkület, atresia, aorta koarctációja, a szívizomsejtek rendellenes fejlődése, endokardiális gyengeség stb.) kombinációja, amelyek hozzájárulnak a szöveti ischaemiához, a fertőzés okozta gyulladásos folyamattal kombinálva gyakorlatilag esélytelenné teszi a gyermek túlélését. Míg a szervfejlődési rendellenességek még gyorsan korrigálhatók, a progresszív fibroelasztózis csak lassítható, de nem gyógyítható.
A magzati szívizom fibroelasztózisát általában már a terhesség alatt, a második vagy harmadik trimeszterben végzett ultrahangvizsgálat során észlelik. A 20-38. héten végzett ultrahang- és echokardiográfia hiperekogenitást mutatott, ami az endocardium megvastagodását és tömörödését (általában diffúz, ritkábban fokális) jelzi, a szív méretének és alakjának megváltozását (a szerv megnagyobbodik, golyó vagy golyó alakját ölti fel, a belső struktúrák fokozatosan kisimulnak). [ 6 ]
Az esetek 30-35%-ában a fibroelasztózist a terhesség 26. hete előtt, 65-70%-ában pedig a későbbi időszakban észlelték. Az újszülöttek több mint 80%-ánál a fibroelasztózis obstruktív szívhibákkal kombinálódik, azaz másodlagos, a felismerés korai szakasza ellenére. Az érintett gyermekek felénél bal kamrai hiperpláziát észleltek, ami magyarázza a fibroelasztózis magas prevalenciáját ebben a szívszerkezetben. Az aorta és billentyűjének patológiái, amelyeket az endokardiális proliferációban szenvedő gyermekek egyharmadánál észlelnek, szintén a bal kamra kamrájának növekedéséhez (dilatációjához) és működésének zavarához vezetnek.
Műszeresen igazolt szívfibroelasztózis esetén az orvosok a terhesség megszakítását javasolják. Szinte minden olyan gyermeknél, akinek az édesanyja elutasította a gyógyszeres abortuszt, a betegség jelei beigazolódtak. A fibroelasztózisra jellemző szívelégtelenség tünetei egy éven belül jelentkeznek (ritkán az élet 2-3. évében). A betegség kombinált formájában szenvedő gyermekeknél a szívelégtelenség jelei az élet első napjaitól észlelhetők.
A primer és kombinált fibroelasztózis veleszületett formái gyermekeknél leggyakrabban gyors lefolyásúak, súlyos szívelégtelenség kialakulásával. Az alacsony aktivitás, a gyermek levertsége, a szoptatás megtagadása a gyors fáradtság miatt, az étvágytalanság, a fokozott izzadás rossz egészségi állapotra utal. Mindez ahhoz vezet, hogy a gyermek nem hízik jól. A baba bőre fájdalmasan sápadt, némelyiknél kékes árnyalatú, leggyakrabban a nasolabiális háromszögben.
A gyenge immunitás jelei mutatkoznak, ezért az ilyen gyermekek gyakran és gyorsan elkapnak légúti fertőzéseket, ami bonyolítja a helyzetet. Előfordul, hogy az élet első napjaiban és hónapjaiban a gyermek nem mutat semmilyen keringési zavart, de a gyakori fertőzések és tüdőbetegségek a pangásos szívelégtelenség kialakulásának kiváltó okaivá válnak.
Az újszülöttek és a korábban fibroelasztózis gyanújával diagnosztizált vagy korábban diagnosztizált kisgyermekek kiegészítő egészségügyi vizsgálatai alacsony vérnyomást (hipotenziót), megnagyobbodott szívet (kardiomegáliát), tompa hangot mutattak a szív hallgatásakor, néha a mitrális billentyű elégtelenségére jellemző szisztolés zörejt, tachycardiát és dyspnoét. A tüdő meghallgatása zihálást mutat, ami a tüdő pangására utal.
A bal kamra endokardiális károsodása gyakran a szív izomrétegének (szívizom) gyengüléséhez vezet. A normális szívritmus két ritmikusan váltakozó hangból áll. Fibroelasztózis esetén egy harmadik (és néha egy negyedik) hang is megjelenhet. Az ilyen kóros ritmus tisztán hallható, és hangjában a ló háromütemű járására (galopp) hasonlít, ezért galoppritmusnak nevezik.
A fibroelasztózis egy másik tünete kisgyermekeknél a szívpúp megjelenése. A helyzet az, hogy a gyermek bordái a korai posztnatális időszakban nem csontosodnak el, és porcos szövet képviseli őket. A szív méretének növekedése ahhoz vezet, hogy nyomást gyakorol a "puha" bordákra, aminek következtében azok meghajlanak és állandó előre ívelt formát vesznek fel (szívpúp). Felnőtteknél a fibroelasztózisban a bordák csontszövetének erőssége és merevsége miatt nem alakul ki szívpúp, még a szív összes struktúrájának növekedése esetén sem.
A szívpúp kialakulása önmagában csak veleszületett szívhibára utal, annak természetét nem részletezve. Mindenesetre a szív és a kamrák méretének növekedésével jár.
A fibroelasztózisban szenvedő gyermekek ödémás szindrómáját ritkán diagnosztizálják, de sok gyermeknél megnagyobbodott máj tapasztalható, amely átlagosan 3 cm-rel kezd kinyúlni a bordaív szélétől.
Ha fibroelasztózis alakul ki (például a szív membránjainak gyulladásos betegségeinek következménye), a klinikai kép leggyakrabban lassan progresszív. Egy ideig a tünetek teljesen hiányozhatnak, majd a szívműködési zavar enyhe jelei jelentkeznek légszomj formájában fizikai megterheléskor, fokozott pulzusszám, gyors fáradtság és alacsony fizikai állóképesség formájában. Kicsit később a máj megnagyobbodni kezd, ödéma és szédülés jelentkezik.
A szerzett fibroelasztózis minden tünete nem specifikus, ami megnehezíti a betegség diagnózisát, hasonlít a kardiomiopátiára, a máj- és vesebetegségre. A betegséget leggyakrabban súlyos szívelégtelenség stádiumában diagnosztizálják, ami negatívan befolyásolja a kezelés eredményeit.
Komplikációk és következmények
Meg kell mondani, hogy a szív és a tüdő fibroelasztózisa súlyos patológiák, amelyek lefolyása különböző körülményektől függ. A veleszületett szívhibák jelentősen bonyolítják a helyzetet, amelyeket korai életkorban sebészeti úton el lehet távolítani, de ugyanakkor továbbra is meglehetősen magas a halálozás kockázata (körülbelül 10%).
Úgy vélik, hogy minél korábban alakul ki a betegség, annál súlyosabbak lesznek a következményei. Ezt megerősíti az a tény, hogy a veleszületett fibroelasztózis a legtöbb esetben fulmináns vagy akut lefolyású, a szívelégtelenség gyors progressziójával. Az akut szívelégtelenség kialakulása 6 hónaposnál fiatalabb gyermeknél rossz prognosztikai jelnek számít.
A kezelés azonban nem garantálja a szívműködés teljes helyreállítását, csak lassítja a szívelégtelenség tüneteinek progresszióját. Másrészt az ilyen támogató kezelés hiánya a baba életének első két évében halálhoz vezet.
Ha a baba életének első napjaiban és hónapjaiban szívelégtelenséget észlelnek, a gyermek nagy valószínűséggel még egy hetet sem él túl. A kezelésre adott válasz gyermekeknél változó. Terápiás hatás hiányában gyakorlatilag nincs remény. De a nyújtott segítséggel a beteg gyermek várható élettartama rövid (több hónaptól több évig).
A fibroelasztózist okozó veleszületett szívhibák műtéti beavatkozása és korrekciója általában javítja a beteg állapotát. A bal kamrai hiperplázia sikeres sebészeti kezelésével és az orvos előírásainak betartásával a betegség jóindulatú lefolyásúvá válhat: a szívelégtelenség krónikus lefolyású lesz, progresszió jelei nélkül. Bár az ilyen eredmény reménye csekély.
Ami a szív fibroelasztózisának szerzett formáját illeti, az gyorsan krónikussá válik és fokozatosan progrediál. A gyógyszeres kezelés lelassíthatja a folyamatot, de nem állíthatja meg.
A tüdőfibroelasztózis, függetlenül attól, hogy a szerv parenchymájában és membránjaiban bekövetkező változások mikor jelennek meg a világos időszak után, gyorsan progrediál, és néhány éven belül halálhoz vezet, súlyos légzési elégtelenséget okozva. A szomorú az, hogy a betegség kezelésére még nem fejlesztettek ki hatékony módszereket. [ 7 ]
Diagnostics fibroelastosis
Az endomyocardialis fibroelastosis, amelynek tünetei a legtöbb esetben már korán jelentkeznek, veleszületett betegség. Ha kizárjuk azokat a ritka eseteket, amikor a betegség késői gyermekkorban és felnőttkorban kezdett kialakulni sérülések és szomatikus betegségek szövődményeként, akkor a patológia már a prenatális időszakban, azaz a gyermek születése előtt azonosítható.
Az orvosok úgy vélik, hogy a fibroelasztózisra jellemző endokardiális szövetek kóros elváltozásai, a magzati szív alakjának változásai és működésének egyes jellemzői már a terhesség 14. hetében meghatározhatók. De ez még mindig meglehetősen rövid időszak, és nem zárható ki, hogy a betegség valamivel később, a terhesség harmadik trimeszteréhez közelebb, és néha a szülés előtt néhány hónappal is megnyilvánulhat. Ezért a terhes nők megfigyelése során ajánlott a magzati szív klinikai ultrahangvizsgálatát több hetes időközönként elvégezni.
Milyen jelek alapján gyanakodhatnak az orvosok a betegségre a következő ultrahangvizsgálat során? Sok múlik a betegség formáján. Leggyakrabban a fibroelasztózist a bal kamra területén diagnosztizálják, de ez a struktúra nem mindig megnagyobbodott. A betegség tágult formáját, a szív bal kamrájának megnagyobbodásával könnyen meg lehet állapítani ultrahangvizsgálat során a szív gömb alakú alakja alapján, amelynek csúcsát a bal kamra képviseli, a szerv méretének általános növekedése és az interventricularis septum jobb kamra felé történő kidudorodása alapján. A fibroelasztózis fő jele azonban az endocardium, valamint a szívizom-sövények megvastagodása, amelyek jellemzően megnövekedett echogenitással járnak, amit egy specifikus ultrahangvizsgálat határoz meg.
A vizsgálatot speciális ultrahangkészülékkel, kardiológiai programokkal végzik. A magzati echokardiográfia nem károsítja sem az anyát, sem a magzatot, hanem nemcsak a szív anatómiai változásainak azonosítását teszi lehetővé, hanem a koszorúerek állapotának, a bennük lévő vérrögök jelenlétének és a szívhártyák vastagságának változásainak meghatározását is.
A magzati echokardiográfiát nemcsak az ultrahangvizsgálat eredményeinek dekódolása során fellépő eltérések esetén, hanem anyai fertőzés (különösen vírusos) esetén, erős gyógyszerek szedése, örökletes hajlam, anyagcserezavarok jelenléte, valamint idősebb gyermekek veleszületett szívbetegségei esetén is felírják.
A magzati echokardiográfia más veleszületett fibroelasztózis formákat is képes kimutatni. Például a jobb kamra fibroelasztózisa, egy széles körben elterjedt folyamat, amely egyidejűleg károsítja a bal kamrát és a szomszédos struktúrákat: a jobb kamrát, a szívbillentyűket, a pitvarokat, a fibroelasztózis kombinált formáit, az endomyocardiális fibroelasztózist, amely a kamrák belső nyálkahártyájának megvastagodásával és a szívizom egy részének kóros folyamatban való érintettségével jár (általában a fal trombózisával kombinálva).
A prenatális korban észlelt endokardiális fibroelasztózis prognózisa nagyon rossz, ezért az orvosok ebben az esetben a terhesség megszakítását javasolják. A téves diagnózis lehetőségét a magzati szív ismételt ultrahangvizsgálata zárja ki, amelyet az első, a patológiát feltáró vizsgálat után 4 héttel végeznek. Egyértelmű, hogy a terhesség megszakításáról vagy fenntartásáról szóló végső döntés a szülőké, de tisztában kell lenniük azzal, hogy milyen életre kárhoztatják a gyermeket.
Az endokardiális fibroelasztózist nem mindig észlelik terhesség alatt, különösen figyelembe véve azt a tényt, hogy nem minden várandós anya regisztrál a nőgyógyászati klinikán és vesz részt megelőző ultrahangvizsgálaton. A méhben lévő gyermek betegsége gyakorlatilag semmilyen hatással nincs a terhes nő állapotára, így egy beteg baba születése gyakran kellemetlen meglepetés.
Bizonyos esetekben mind a szülők, mind az orvosok csak hónapokkal a gyermek születése után értesülnek a baba betegségéről. Ebben az esetben a laboratóriumi vérvizsgálatok a nátriumkoncentráció emelkedésén (hipernatrémia) kívül semmit sem mutathatnak. Eredményeik azonban hasznosak lesznek a gyulladásos betegségek kizárására szolgáló differenciáldiagnózis elvégzésében.
Még van remény a műszeres diagnosztikára. A standard szívvizsgálat (EKG) nem különösebben indikatív fibroelasztózis esetén. Segít azonosítani a szívműködési zavarokat és a szívizom elektromos vezetőképességét, de nem határozza meg pontosan az ilyen rendellenességek okait. Így az EKG-feszültség változása (fiatalabb korban általában alábecsült, idősebb korban éppen ellenkezőleg, túlzottan magas) kardiomiopátiára utal, amely nemcsak szívbetegségekkel, hanem anyagcserezavarokkal is összefüggésben lehet. A tachycardia a szívbetegségek tünete. És ha a szív mindkét kamrája érintett, a kardiogram általában normálisnak tűnhet. [ 8 ]
A komputertomográfia (CT) kiváló, nem invazív eszköz a szív- és érrendszeri meszesedés kimutatására és a szívburokgyulladás kizárására.[ 9 ]
A mágneses rezonancia képalkotás (MRI) hasznos lehet a fibroelastosis kimutatásában, mivel a biopszia invazív. A miokardiális perfúziós szekvencián látható hipointenz szegély és a késleltetett kontrasztanyag-halmozási szekvencián látható hiperintenz szegély fibroelastosisra utalhat.[ 10 ]
De ez nem jelenti azt, hogy a tanulmányt el kell hagyni, mert segít meghatározni a szív munkájának jellegét és a szívelégtelenség kialakulásának mértékét.
Amikor a szívelégtelenség tünetei jelentkeznek, és a beteg ezzel kapcsolatban orvoshoz fordul, a betegnek mellkasröntgent, a szív komputertomográfiáját vagy mágneses rezonancia képalkotását, echokardiográfiát (EchoCG) is felírnak. Kétes esetekben szívszövet-biopsziát kell végezni, amelyet később szövettani vizsgálatnak vetnek alá. A diagnózis nagyon súlyos, ezért ugyanazt a diagnózishoz való megközelítést igényli, bár a kezelés nem sokban különbözik a koszorúér-betegség és a szívelégtelenség tüneti terápiájától.
De még egy ilyen aprólékos vizsgálat sem lesz hasznos, ha az eredményeit nem használják fel a differenciáldiagnosztikában. Az EKG-eredmények felhasználhatók az akut fibroelasztózis megkülönböztetésére az idiopátiás szívizomgyulladástól, az exudatív perikarditisztől és az aorta-szűkülettől. Ugyanakkor a laboratóriumi vizsgálatok nem mutatnak gyulladás jeleit (leukocitózis, megnövekedett ESR stb.), és a hőmérsékletmérés nem mutat hipertermiát.
A szívhangok és zörejek elemzése, a pitvarok méretének változása és az anamnézis tanulmányozása segít megkülönböztetni az endokardiális fibroelasztózist az izolált mitrálisbillentyű-elégtelenségtől és a mitrálisbillentyű-hibától.
Az anamnesztikus adatok elemzése hasznos a fibroelasztózis és a szív, valamint az aorta-szűkület elkülönítésében. Aorta-szűkület esetén érdemes figyelni a sinusritmus megőrzésére és a tromboembólia hiányára is. Szívritmuszavarok és trombuslerakódás exudatív pericarditisben sem figyelhetők meg, de a betegség hőmérséklet-emelkedéssel és lázzal jelentkezik.
A legnagyobb nehézséget az endokardiális fibroelasztózis és a pangásos kardiomiopátia elkülönítése jelenti. Ebben az esetben a fibroelasztózis, bár a legtöbb esetben nem jár kifejezett szívvezetési zavarokkal, kevésbé kedvező kezelési prognózissal rendelkezik.
Kombinált patológiák esetén figyelni kell a szív tomográfiája vagy ultrahangvizsgálata során feltárt eltérésekre, mivel a veleszületett rendellenességek jelentősen bonyolítják a fibroelasztózis lefolyását. Ha a méhen belüli időszakban kombinált endokardiális fibroelasztózist észlelnek, a terhesség fenntartása nem helyénvaló. Sokkal humánusabb a terhesség megszakítása.
A tüdőfibroelasztózis diagnózisa
A tüdőfibroelasztózis diagnózisa bizonyos ismereteket és készségeket igényel az orvostól. A helyzet az, hogy a betegség tünetei meglehetősen heterogének. Egyrészt pangásos tüdőbetegségekre utalnak (impregnált köhögés, légszomj), másrészt a szívbetegség megnyilvánulása is lehet. Ezért a betegség diagnózisa nem korlátozódhat pusztán a tünetek megállapítására és az hallgatásra.
A beteg vérvizsgálata segít kizárni a gyulladásos tüdőbetegségeket, de nem ad információt a szövetek mennyiségi és minőségi változásairól. Az eozinofília jeleinek jelenléte segít megkülönböztetni a betegséget a tüdőfibrózistól, amely hasonló tüneteket mutat, de nem cáfolja és nem erősíti meg a fibroelasztózis tényét.
A műszeres vizsgálatokat indikatívabbnak tekintik: a mellkasröntgent és a légzőszervek tomográfiás vizsgálatát, valamint a funkcionális elemzéseket, amelyek a légzési térfogatok, a tüdő létfontosságú kapacitása és a szervben lévő nyomás meghatározásából állnak.
Pulmonális fibroelasztózis esetén érdemes figyelmet fordítani a külső légzés funkciójának csökkenésére, amelyet spirometria során mérnek. Az aktív alveoláris üregek csökkenése jelentősen befolyásolja a tüdő vitálkapacitását (VCL), a belső struktúrák falainak megvastagodása pedig a szerv diffúziós kapacitását (DCL), amely biztosítja a szellőzést és a gázcsere funkcióit (egyszerűen fogalmazva: a szén-dioxid felszívódását a vérből és az oxigén leadását).
A pleuroparenchimális fibroelasztózis jellegzetes jelei a tüdőbe jutó korlátozott légáramlás (elzáródás) és a belégzés során a tüdő tágulási zavara (restrikció), a külső légzésfunkció romlása, a mérsékelt pulmonális hipertónia (megnövekedett nyomás a tüdőben) kombinációja, amelyet a betegek felénél diagnosztizálnak.
A tüdőszövet-biopszia a szerv belső szerkezetében jellegzetes változásokat mutat. Ezek közé tartozik: a mellhártya és a parenchyma fibrózisa az alveoláris falak elasztózisával kombinálva, limfociták felhalmozódása a tömörödött alveoláris szeptumok területén, a fibroblasztok átalakulása izomszövetté, amely nem jellemző rájuk, és ödémás folyadék jelenléte.
A tomográfia a tüdő felső szakaszainak károsodását mutatja pleurális tömörödés gócainak és a parenchyma szerkezeti változásainak formájában. A tüdő megnagyobbodott kötőszövete színében és tulajdonságaiban az izomszövetre hasonlít, de a tüdő térfogata csökken. A parenchymában meglehetősen nagy, levegőt tartalmazó üregek (ciszták) találhatók. Jellemző a hörgők és hörgőcskék visszafordíthatatlan fokális (vagy diffúz) tágulása (trakciós bronchiektázia) és a rekeszizom alacsony kupolája.
A radiológiai vizsgálatok sok betegnél „őrölt üveg” és „méhsejtszerű tüdő” területeket mutatnak, ami a tüdő egyenetlen szellőzésére utal a szöveti tömörödés gócai miatt. A betegek körülbelül felénél megnagyobbodott nyirokcsomók és máj található.
A tüdőfibroelasztózist meg kell különböztetni a parazitafertőzés és a kapcsolódó eozinofília okozta fibrózistól, az endokardiális fibroelasztózistól, a károsodott légzéssel és a "méhsejtes tüdő" képével járó tüdőbetegségektől, az autoimmun betegségtől, a hisztikotitisz X-től (ennek a tüdőkárosodással járó patológiának az egyik formáját Hand-Schüller-Christian betegségnek nevezik), a szarkoidózis és a tüdőtuberkulózis megnyilvánulásaitól.
Kezelés fibroelastosis
A fibroelasztózis, bárhol is lokalizálódik, veszélyes és gyakorlatilag gyógyíthatatlan betegségnek számít. A mellhártya és a tüdő parenchyma kóros elváltozásai gyógyszeres kezeléssel nem állíthatók vissza. És még a hormonális gyulladáscsökkentő gyógyszerek (kortikoszteroidok) hörgőtágítókkal kombinált alkalmazása sem adja meg a kívánt eredményt. A hörgőtágítók kismértékben enyhítik a beteg állapotát, enyhítik az obstruktív szindrómát, de nem befolyásolják a tüdőben zajló folyamatokat, így csak támogató terápiaként alkalmazhatók.
A tüdőfibroelasztózis sebészeti kezelése szintén hatástalan. Az egyetlen műtét, ami megváltoztathatja a helyzetet, a donor szervátültetés. A tüdőátültetés azonban sajnos ugyanolyan kedvezőtlen prognózissal jár. [ 11 ]
Külföldi tudósok szerint a fibroelasztózis a tüdő- vagy csontvelő-őssejt-transzplantáció egyik gyakori szövődményének is tekinthető. Mindkét esetben a tüdő kötőszöveti rostjaiban változások következnek be, amelyek befolyásolják a külső légzés működését.
A betegség kezelés nélkül lefolyása megszűnik (és jelenleg nincs hatékony kezelés), és a betegek körülbelül 40%-a 1,5-2 éven belül légzési elégtelenségben hal meg. A betegben maradók várható élettartama is jelentősen korlátozott (akár 10-20 év), akárcsak a munkaképességük. A személy rokkanttá válik.
A szív fibroelasztózisát orvosilag gyógyíthatatlan betegségnek is tekintik, különösen, ha veleszületett patológiáról van szó. A gyermekek általában nem élik meg a 2 éves kort. Csak szívátültetéssel lehet megmenteni őket, ami önmagában is egy nehéz műtét, magas kockázattal és kiszámíthatatlan következményekkel, különösen ilyen fiatal korban.
Egyes csecsemőknél a veleszületett szívhibák műtéti úton korrigálhatók, hogy azok ne rontsák a beteg gyermek állapotát. Artéria-szűkület esetén ér-tágítót - shuntöt (aortokoronáris bypass) - helyeznek be. A szív bal kamrájának tágulása esetén annak alakja gyorsan helyreáll. De még egy ilyen műtét sem garantálja, hogy a gyermek transzplantáció nélkül is boldogulni fog. A csecsemők körülbelül 20-25%-a túléli, és egész életükben szívelégtelenségben szenvednek, azaz nem tekinthetők egészségesnek.
Ha a betegség megszerzett, érdemes gyógyszerek segítségével küzdeni a gyermek életéért. Fontos azonban megérteni, hogy minél korábban manifesztálódik a betegség, annál nehezebb lesz leküzdeni.
A gyógyszeres kezelés célja a szívelégtelenség súlyosbodásának leküzdése és megelőzése. A betegeknek a következő szívgyógyszereket írják fel:
- angiotenzin-konvertáló enzim (ACE) gátlók, amelyek befolyásolják a vérnyomást és a normál tartományon belül tartják (kaptopril, enalapril, benazepril stb.),
- béta-blokkolók, amelyeket szívritmuszavarok, artériás magas vérnyomás kezelésére és miokardiális infarktus megelőzésére használnak (anaprilin, biszoprolol, metoprolol),
- szívglikozidok, amelyek hosszú távú alkalmazás esetén nemcsak a szív működését támogatják (növelik a káliumtartalmat a szívizomsejtekben és javítják a szívizom vezetőképességét), hanem képesek némileg csökkenteni az endokardiális megvastagodás mértékét is (digoxin, gitoxin, strofantin),
- kálium-megtakarító diuretikumok (spironolakton, veroshpiron, decriz), amelyek megakadályozzák a szöveti ödémát,
- antitrombotikus terápia antikoagulánsokkal (cardiomagnyl, magnicor), amely megakadályozza a vérrögök kialakulását és a keringési zavarokat a koszorúerekben.
Az endokardiális fibroelasztózis veleszületett formájában a támogató kezelés nem segíti elő a gyógyulást, de 70-75%-kal csökkenti a szívelégtelenség vagy tromboembólia okozta halálozás kockázatát [ 12 ].
Gyógyszerek
Amint láthatjuk, az endokardiális fibroelasztózis kezelése gyakorlatilag nem különbözik a szívelégtelenség kezelésétől. Mindkét esetben a kardiológusok figyelembe veszik a kardiopátia súlyosságát. A gyógyszerek felírása szigorúan egyéni, figyelembe véve a beteg életkorát, az egyidejűleg fennálló betegségeket, a szívelégtelenség formáját és mértékét.
A szerzett endokardiális fibroelasztózis kezelésében 5 csoportba tartozó gyógyszereket alkalmaznak. Tekintsünk egy-egy gyógyszert minden csoportból.
Az „Enalapril” az ACE-gátlók csoportjába tartozó gyógyszer, amelyet különböző dózisú tabletták formájában állítanak elő. A gyógyszer fokozza a koszorúér-véráramlást, tágítja az artériákat, csökkenti a vérnyomást az agyi keringés befolyásolása nélkül, lelassítja és csökkenti a szív bal kamrájának tágulását. A gyógyszer javítja a szívizom vérellátását, csökkenti az ischaemia hatásait, enyhén csökkenti a véralvadást, megakadályozza a vérrögök kialakulását, enyhe vízhajtó hatású.
Szívelégtelenség esetén a gyógyszert hat hónapnál hosszabb ideig vagy állandó jelleggel írják fel. A gyógyszeres kezelést minimális adaggal (2,5 mg) kezdik, majd fokozatosan 3-4 naponta 2,5-5 mg-mal emelik. Az állandó adag az lesz, amelyet a beteg jól tolerál, és amely a vérnyomást a normál tartományon belül tartja.
A maximális napi adag 40 mg. Egyszeri adagban vagy két részre osztva is bevehető.
Ha a vérnyomás a normális érték alatt van, az adagot fokozatosan kell csökkenteni. Az Enalapril-kezelést nem szabad hirtelen abbahagyni. Naponta 5 mg fenntartó adag szedése javasolt.
A gyógyszer felnőtt betegek kezelésére szolgál, de gyermeknek is felírható (a biztonságosságot hivatalosan nem állapították meg, de fibroelasztózis esetén egy kis beteg élete forog kockán, ezért a kockázati arányt figyelembe veszik). Az ACE-gátlót nem írják fel olyan betegeknek, akiknél intolerancia lép fel a gyógyszer összetevőivel szemben, porfíria, terhesség és szoptatás alatt. Ha a beteg korábban Quincke ödémát tapasztalt a csoportba tartozó gyógyszerek szedése alatt, az Enalapril tilos.
Óvatosan kell eljárni a gyógyszer felírásakor olyan betegeknél, akiknek egyidejűleg patológiái vannak: súlyos vese- és májbetegségek, hiperkalémia, hiperaldoszteronizmus, aorta- vagy mitrális billentyű szűkület, szisztémás kötőszöveti patológiák, szív ischaemia, agyi betegség, cukorbetegség.
A gyógyszerrel történő kezelés során ne szedjen hagyományos vízhajtókat a kiszáradás és az erős vérnyomáscsökkentő hatás elkerülése érdekében. A kálium-megtakarító diuretikumokkal való egyidejű alkalmazás dózismódosítást igényel, mivel nagy a hiperkalémia kockázata, ami viszont szívritmuszavarokat, görcsrohamokat, csökkent izomtónust, fokozott gyengeséget stb. okozhat.
Az "Enalapril" gyógyszer általában jól tolerálható, de egyes betegeknél mellékhatások jelentkezhetnek. A leggyakoribbak a következők: a vérnyomás erős csökkenése akár összeomlásig, fejfájás és szédülés, alvászavarok, fokozott fáradtság, visszafordítható egyensúlyvesztés, hallás- és látászavarok, fülzúgás megjelenése, légszomj, köpet nélküli köhögés, a vér és a vizelet összetételének változásai, amelyek általában a máj és a vesék nem megfelelő működését jelzik. Lehetséges: hajhullás, csökkent szexuális vágy, "hőhullámok" tünetei (hőérzet és szívdobogás, az arc bőrének kipirosodása stb.).
A „bizoprolol” egy szelektív hatású béta-blokkoló, amely vérnyomáscsökkentő és antiischaemiás hatásokkal rendelkezik, segít leküzdeni a tachycardia és az aritmia megnyilvánulásait. Tabletta formájában kapható, megfizethető gyógyszer, amely megakadályozza a szívelégtelenség progresszióját endokardiális fibroelasztózisban. [ 13 ]
Sok más, koszorúér-betegség és szívelégtelenség kezelésére felírt gyógyszerhez hasonlóan a biszoprololt is hosszú távon kell alkalmazni. Célszerű reggel, étkezés előtt vagy közben bevenni.
Ami az ajánlott adagokat illeti, azokat egyénileg választják ki a vérnyomásértékek és a gyógyszerrel párhuzamosan felírt gyógyszerek alapján. Átlagosan az egyszeri (szintén napi) adag 5-10 mg, de enyhe nyomásemelkedéssel 2,5 mg-ra csökkenthető. A normálisan működő vesékkel rendelkező betegeknek a maximális adag 20 mg, de csak tartósan magas vérnyomás esetén.
A feltüntetett adagok emelése csak orvos engedélyével lehetséges. Súlyos máj- és vesebetegségek esetén azonban a maximálisan megengedett adag 10 mg.
A bal kamrai diszfunkció hátterében fellépő szívelégtelenség komplex kezelésében, amely leggyakrabban fibroelasztózissal fordul elő, a hatékony dózist az adag 1,25 mg-os fokozatos növelésével választják ki. Ebben az esetben a lehető legkisebb dózissal (1,25 mg) kezdik. Az adagot 1 hetes időközönként növelik.
Amikor az adag eléri az 5 mg-ot, az intervallum 28 napra nő. 4 hét elteltével az adag 2,5 mg-mal nő. Ezt az intervallumot és a normát betartva elérik a 10 mg-ot, amelyet a betegnek hosszú ideig vagy folyamatosan kell szednie.
Ha egy ilyen adagot a beteg rosszul tolerál, fokozatosan csökkenteni kell a kényelmes szintre. A béta-blokkolóval végzett kezelés leállítása sem lehet hirtelen.
A gyógyszert nem szabad felírni a hatóanyaggal és segédanyagokkal szembeni túlérzékenység, akut és dekompenzált szívelégtelenség, kardiogén sokk, 2-3. fokú pitvar-kamrai blokk, bradycardia, tartósan alacsony vérnyomás és néhány más szívbetegség, súlyos hörgőasztma, hörgőelzáródás, súlyos perifériás keringési zavarok, metabolikus acidózis esetén.
Komplex kezelés felírásakor óvatosan kell eljárni. Ezért a bizoprolol kombinációja bizonyos antiaritmiás szerekkel (kinidin, lidokain, fenitoin stb.), kalciumantagonistákkal és központi vérnyomáscsökkentő gyógyszerekkel nem ajánlott.
A Bisoprolol-kezelés során lehetséges kellemetlen tünetek és rendellenességek: fokozott fáradtság, fejfájás, hőhullámok, alvászavarok, vérnyomásesés és szédülés felkeléskor, halláskárosodás, gyomor-bélrendszeri tünetek, máj- és vesebetegségek, potenciacsökkenés, izomgyengeség és görcsök. A betegek néha perifériás keringési zavarokra panaszkodnak, amelyek a végtagok, különösen az ujjak és lábujjak hőmérsékletének csökkenésében vagy zsibbadásában nyilvánulnak meg.
A bronchopulmonális rendszer, a vesék, a máj és a cukorbetegség egyidejű betegségeinek jelenlétében a mellékhatások kockázata nagyobb, ami a betegség súlyosbodását jelzi.
A "digoxin" egy népszerű, olcsó szívglikozid, amely a gyűszűvirág növényen alapul, és amelyet szigorúan receptre (tablettákban) adnak ki, és az ő felügyelete alatt kell alkalmazni. Az injekciós kezelést kórházi környezetben végzik a koszorúér-betegség és a szívelégtelenség súlyosbodása során, a tablettákat folyamatosan, minimálisan hatékony dózisokban írják fel, mivel a gyógyszer mérgező és narkotikus hatású.
A terápiás hatás a szívizom-összehúzódások erősségének és amplitúdójának megváltoztatásából áll (energiát ad a szívnek, támogatja azt ischaemiás állapotokban). A gyógyszer értágító (csökkenti a pangást) és némi vízhajtó hatású is, ami segít enyhíteni a duzzanatot és csökkenteni a légzési elégtelenség súlyosságát, ami légszomjként nyilvánul meg.
A digoxin és más szívglikozidok veszélye, hogy túladagolás esetén szívritmuszavart okozhatnak, amelyet a szívizom fokozott ingerlékenysége okoz.
A szívelégtelenség súlyosbodása esetén a gyógyszert injekció formájában írják fel, az egyéni adagot a betegség súlyossága és a beteg életkora alapján választják ki. Amikor az állapot stabilizálódik, tablettákra váltanak.
A gyógyszer standard egyszeri adagja általában 0,25 mg. Az adagolás gyakorisága napi 1-5 alkalommal változhat, egyenlő időközönként. A CHF akut stádiumában a napi adag elérheti az 1,25 mg-ot, amikor az állapot tartósan stabilizálódik, napi 0,25 (ritkábban 0,5) mg fenntartó adagot kell bevenni.
A gyógyszer gyermekeknek történő felírásakor figyelembe veszik a beteg testsúlyát. A hatékony és biztonságos adagot 0,05-0,08 mg/testtömegkilogrammnak számítják. A gyógyszert azonban nem folyamatosan, hanem 1-7 napig írják fel.
A szívglikozid adagolását orvosnak kell előírnia, figyelembe véve a beteg állapotát és életkorát. Ugyanakkor nagyon veszélyes az adagok önálló beállítása, vagy két ilyen hatású gyógyszer egyidejű szedése.
A „digoxint” nem írják fel instabil angina, súlyos szívritmuszavarok, 2-3. fokú AV-blokk, szívtamponád, Adams-Stokes-Morgagni szindróma, izolált kéthegyű billentyű szűkület és aorta szűkület, Wolff-Parkinson-White szindróma nevű veleszületett szívizom-rendellenesség, hipertrófiás obstruktív kardiomiopátia, endo-, peri- és miokarditisz, mellkasi aorta aneurizma, hiperkalcémia, hipokalémia és néhány más patológia esetén. Az ellenjavallatok listája meglehetősen hosszú, és többféle manifesztációval járó szindrómákat is tartalmaz, így a gyógyszer alkalmazásának lehetőségéről csak szakember dönthet.
A digoxinnak is vannak mellékhatásai. Ezek közé tartoznak a szívritmuszavarok (helytelenül megválasztott adag és túladagolás következtében), étvágytalanság, hányinger (gyakran hányással), székletzavarok, súlyos gyengeség és fokozott fáradtság, fejfájás, a "legyek" megjelenése a szem előtt, a vérlemezkeszám csökkenése és a véralvadási zavarok, allergiás reakciók. Leggyakrabban ezek és más tünetek megjelenése a gyógyszer nagy dózisainak bevételével, ritkábban a hosszú távú terápiával jár.
A "spironolakton" egy mineralokortikoid antagonista. Vízhajtó hatású, elősegíti a nátrium, a klór és a víz kiválasztását, de megtartja a káliumot, ami a szív normális működéséhez szükséges, mivel vezetőképessége főként ezen az elemen alapul. Segít enyhíteni az ödémát. Pangásos szívelégtelenség esetén adjuvánsként alkalmazzák.
Szívelégtelenség esetén a gyógyszert a betegség fázisától függően írják fel. Súlyosbodás esetén a gyógyszer injekciók és tabletták formájában is felírható napi 50-100 mg-os dózisban. Amikor az állapot stabilizálódik, hosszú távon 25-50 mg-os fenntartó adagot írnak fel. Ha a kálium és a nátrium egyensúlya az előbbi csökkenése felé zavart szenved, az adagot addig lehet növelni, amíg a nyomelemek normális koncentrációja be nem áll.
Gyermekgyógyászatban a hatékony dózist a beteg testtömegkilogrammjára vonatkoztatott 1-3 mg spironolakton arány alapján számítják ki.
Mint láthatjuk, itt is egyéni az ajánlott adag kiválasztása, ahogyan sok más, a kardiológiában használt gyógyszer felírásánál is.
A diuretikum alkalmazásának ellenjavallatai lehetnek: a szervezetben a kálium feleslege vagy az alacsony nátriumszint, a vizelési inger hiányával járó patológia (anuria), súlyos vesebetegség, amely károsodott teljesítménnyel jár. A gyógyszert nem írják fel terhes nőknek és szoptató anyáknak, valamint azoknak, akik intoleranciában szenvednek a gyógyszer összetevőivel szemben.
Óvatosan kell eljárni a gyógyszer alkalmazása során AV szívblokkban (súlyosbodhat), túlzott kalciumszinttel (hiperkalcémia), metabolikus acidózissal, cukorbetegséggel, menstruációs zavarokkal és májbetegséggel küzdő betegeknél.
A gyógyszer szedése fejfájást, álmosságot, egyensúly- és mozgáskoordinációs zavarokat (ataxiát), férfiaknál az emlőmirigyek megnagyobbodását (ginekomasztia) és impotenciát, a menstruáció jellegének megváltozását, nőknél a hang eldurvulását és fokozott szőrnövekedést (hirsutizmust), gyomortáji fájdalmat és gyomor-bélrendszeri zavarokat, bélkólikát, veseműködési zavarokat és ásványianyag-egyensúly felborulását okozhatja. Bőr- és allergiás reakciók is előfordulhatnak.
Mellékhatások általában akkor jelentkeznek, ha a szükséges adagot túllépik. Ödéma léphet fel, ha az adag nem elegendő.
A „Magnicor” egy vérrögképződést gátló gyógyszer, amely acetilszalicilsav és magnézium-hidroxid alapú. A szívelégtelenség esetén felírt antitrombotikus terápia egyik hatékony eszköze. Fájdalomcsillapító, gyulladáscsökkentő, vérlemezke-gátló hatással rendelkezik, és befolyásolja a légzésfunkciót. A magnézium-hidroxid csökkenti az acetilszalicilsav negatív hatását a gyomor-bél nyálkahártyájára.
Endomyocardiális fibroelastosis esetén a gyógyszert profilaktikus célokra írják fel, ezért a minimális hatásos dózist - 75 mg-ot, ami 1 tablettának felel meg - betartják. Trombusképződés és a koszorúerek lumenének későbbi szűkülése miatti szívizom-ischaemia esetén a kezdeti dózis 2 tabletta, a fenntartó dózis pedig a profilaktikus dózisnak felel meg.
Az ajánlott adag túllépése jelentősen növeli a nehezen megállítható vérzés kockázatát.
Az adagolás felnőtt betegek számára javallt, mivel a gyógyszer acetilszalicilsavat tartalmaz, amelynek alkalmazása 15 év alatti korban súlyos következményekkel járhat.
A gyógyszert nem írják fel gyermekkori és korai serdülőkori betegeknek, acetilszalicilsav és a gyógyszer egyéb összetevőinek intoleranciája, "aszpirin" asztma (a kórtörténetben), akut erozív gasztritisz, gyomorfekély, vérzéses diatézis, súlyos máj- és vesebetegségek, súlyos dekompenzált szívelégtelenség esetén.
Terhesség alatt a Magnicort csak rendkívüli szükség esetén és csak az 1-2. trimeszterben írják fel, figyelembe véve a magzatra és a terhesség lefolyására gyakorolt lehetséges negatív hatást. A terhesség 3. trimeszterében az ilyen kezelés nem kívánatos, mivel hozzájárul a méh összehúzódási képességének csökkenéséhez (elhúzódó vajúdás), és súlyos vérzést okozhat. A magzatnál pulmonális hipertónia és veseelégtelenség alakulhat ki.
A gyógyszer mellékhatásai közé tartoznak a gyomor-bél traktus tünetei (diszpepszia, gyomortáji és hasi fájdalom, gyomorvérzés kockázata vashiányos vérszegénység kialakulásával). A gyógyszer szedésének hátterében orrvérzés, ínyvérzés és húgyúti szervek vérzése lehetséges.
A túladagolás szédülést, ájulást és fülzúgást okozhat. Az allergiás reakciók nem ritkák, különösen szalicilátokkal szembeni túlérzékenység esetén. Az anafilaxia és a légzési elégtelenség azonban ritka mellékhatások.
A komplex terápiában alkalmazott gyógyszerek kiválasztásának és az ajánlott adagoknak szigorúan egyéninek kell lenniük. Különös óvatossággal kell eljárni terhes nők, szoptató anyák, gyermekek és idős betegek kezelésében.
Hagyományos orvoslás és homeopátia
A szív fibroelasztózisa egy súlyos és súlyos betegség, jellegzetes progresszív lefolyással és gyakorlatilag esélytelen gyógyulással. Nyilvánvaló, hogy egy ilyen betegség hatékony kezelése népi gyógymódokkal lehetetlen. A hagyományos orvosi receptek, amelyek főként gyógynövényes kezelésre korlátozódnak, csak segédeszközként és csak orvos engedélyével alkalmazhatók, hogy ne bonyolítsák a már amúgy is rossz prognózist.
Ami a homeopátiás szereket illeti, alkalmazásuk nem tiltott, és a szívelégtelenség átfogó kezelésének részét képezhetik. Ebben az esetben azonban nem annyira a kezelésről beszélünk, mint inkább a szívelégtelenség progressziójának megelőzéséről.
A gyógyszereket tapasztalt homeopatának kell felírnia, és a komplex terápiába való bevonásának lehetősége a kezelőorvos hatáskörébe tartozik.
Milyen homeopátiás gyógyszerek segítenek késleltetni a szívelégtelenség progresszióját fibroelasztózisban? Akut szívelégtelenség esetén a homeopaták a következő gyógyszerekhez fordulnak segítségért: Arsenicum album, Antimonium tartaricum, Carbo vegetabilis, Acidum oxalicum. A javallatok hasonlósága ellenére a hatékony gyógyszer kiválasztásakor az orvosok az ischaemia külső megnyilvánulásaira, a cianózisra (annak mértékére és prevalenciájára), valamint a fájdalom szindróma jellegére támaszkodnak.
Szívelégtelenség esetén a fenntartó terápia részeként alkalmazhatók a Lachesis és Nayu gyógynövekedést gátló szerek, Lycopus (a szívnagyobbodás kezdeti szakaszában), Laurocerasus (nyugalmi légszomj esetén), Latrodectus mactans (billentyűbetegségek esetén), galagonyakészítmények (különösen hasznosak endomyocardialis elváltozások esetén).
Erős szívverés esetén tüneti kezelésre a következőket írhatják fel: Spigelia, Glonoinum (tachycardia esetén), Aurum metallicum (magas vérnyomás esetén).
A légszomj súlyosságának csökkentésére a következők segítenek: Grindelia, Spongia és Lahegis. A szívfájdalom enyhítésére a következők írhatók fel: Cactus, Cereus, Naya, Cuprum, a szorongás enyhítésére pedig az Aconitum. Szív eredetű asztma kialakulásában a következők javallottak: Digitalis, Laurocerasus, Lycopus.
Megelőzés
A szív és a tüdő szerzett fibroelasztózisának megelőzése a fertőző és gyulladásos betegségek megelőzéséből és időben történő kezeléséből áll, különösen, ha létfontosságú szervek károsodásáról van szó. Az alapbetegség hatékony kezelése segít megelőzni a veszélyes következményeket, amelyek közé tartozik a fibroelasztózis is. Ez kiváló ok arra, hogy gondoskodjon az egészségéről és a jövő generációinak egészségéről, az úgynevezett egészséges jövőért és hosszú életért végzett munkáról.
Előrejelzés
A szív- és tüdőfibroelasztózissal járó kötőszöveti elváltozásokat visszafordíthatatlannak tekintik. Bár egyes gyógyszerek hosszú távú terápiával némileg csökkenthetik az endocardium vastagságát, nem garantálják a gyógyulást. Bár az állapot nem mindig halálos, a prognózis még mindig viszonylag rossz. A 4 éves túlélési arány 77%. [ 14 ]
A legrosszabb prognózis, ahogy már említettük, a veleszületett szívizom fibroelasztózis esetében van, amelynek szívelégtelenség tünetei már a gyermek életének első heteiben és hónapjaiban is láthatók. Csak a szívátültetés mentheti meg a babát, ami önmagában is kockázatos műtét ilyen korai időszakban, és 2 éves kor előtt el kell végezni. Az ilyen gyermekek általában nem élnek tovább.
Más műtétek csak a gyermek korai halálának elkerülését teszik lehetővé (és nem mindig), de nem tudják teljesen meggyógyítani a szívelégtelenségből. A halál dekompenzációval és légzési elégtelenség kialakulásával következik be.
A tüdőfibroelasztózis prognózisa a betegség jellemzőitől függ. Ha a tünetek gyorsan alakulnak ki, az esélyek rendkívül kicsik. Ha a betegség fokozatosan progrediál, a beteg körülbelül 10-20 évig élhet, amíg a tüdő alveolusaiban bekövetkező változások miatt légzési elégtelenség nem lép fel.
Sok nehezen kezelhető patológia elkerülhető megelőző intézkedésekkel. A szív fibroelasztózisa esetében ez elsősorban azoknak a tényezőknek a megelőzése, amelyek befolyásolhatják a magzat szív- és keringési rendszerének fejlődését (kivéve az örökletes hajlamot és a mutációkat, amelyekkel szemben az orvosok tehetetlenek). Ha ezek nem kerülhetők el, a korai diagnózis segít azonosítani a patológiát abban a szakaszban, amikor a terhességmegszakítás lehetséges, ami ebben a helyzetben humánusnak tekinthető.

