A cikk orvosi szakértője
Új kiadványok
A hepatitis B patogenezise
Utolsó ellenőrzés: 07.07.2025

Minden iLive-tartalmat orvosi szempontból felülvizsgáltak vagy tényszerűen ellenőriznek, hogy a lehető legtöbb tényszerű pontosságot biztosítsák.
Szigorú beszerzési iránymutatásunk van, és csak a jó hírű média oldalakhoz, az akadémiai kutatóintézetekhez és, ha lehetséges, orvosilag felülvizsgált tanulmányokhoz kapcsolódik. Ne feledje, hogy a zárójelben ([1], [2] stb.) Szereplő számok ezekre a tanulmányokra kattintható linkek.
Ha úgy érzi, hogy a tartalom bármely pontatlan, elavult vagy más módon megkérdőjelezhető, jelölje ki, és nyomja meg a Ctrl + Enter billentyűt.
A hepatitis B patogenezisében a patogenetikai láncban számos vezető láncszem azonosítható:
- a kórokozó bejuttatása - fertőzés;
- rögzítés a hepatocitán és behatolás a sejtbe;
- a vírus szaporodása és „kiszorulása” a hepatocita felszínére, valamint a vérbe;
- immunológiai reakciók aktiválása, amelyek célja a kórokozó eltávolítása;
- immunkomplex károsodás szervekben és rendszerekben;
- immunitás kialakulása, a kórokozótól való megszabadulás, felépülés.
Mivel a hepatitis B fertőzés mindig parenterálisan történik, úgy tekinthető, hogy a fertőzés pillanata gyakorlatilag egyezik a vírus vérbe jutásával. Egyes kutatók azon kísérletei, hogy megkülönböztetjék a hepatitis B enterális és regionális fázisát, kevéssé megalapozottak. Több okunk van azt feltételezni, hogy a vírus a vérárammal azonnal bejut a májba.
A hepatitis B vírus májszövettel szembeni tropizmusát egy speciális receptor jelenléte határozza meg a HBsAg-ben - egy 31 000 Da molekulatömegű (P31) polipeptid, amely albuminkötő aktivitással rendelkezik. Hasonló albuminzóna található az emberi és csimpánz máj hepatocitáinak membránján is, amely lényegében meghatározza a HBV tropizmusát az emberi és csimpánz májjal szemben.
Amikor a vírus behatol a májsejtbe, vírus DNS szabadul fel, amely a májsejt magjába jutva és a nukleinsavak szintézisének mátrixaként működve egymást követő biológiai reakciók sorozatát indítja el, amelyek eredményeként a vírus nukleokapszidja összeáll. A nukleokapszid a sejtmag membránján keresztül a citoplazmába vándorol, ahol a Dane-részecskék végső összeszerelése - a teljes hepatitis B vírus - történik.
Meg kell azonban jegyezni, hogy amikor egy hepatocita megfertőződik, a folyamat kétféleképpen folytatódhat - replikatív és integratív. Az első esetben akut vagy krónikus hepatitisz képe alakul ki, a másodikban pedig vírushordozás.
A vírus DNS és a hepatociták közötti kétféle kölcsönhatást meghatározó okokat még nem sikerült pontosan megállapítani. Valószínűleg a válasz típusa genetikailag meghatározott.
A replikatív kölcsönhatás eredménye a mag antigénstruktúrák összeállódása (a sejtmagban) és a teljes vírus összeállódása (a citoplazmában), majd a teljes vírus vagy antigénjeinek bemutatása a membránon vagy a hepatocita membránjának szerkezetében.
Általánosan elfogadott, hogy a vírusreplikáció nem okoz sejtkárosodást a hepatociták szintjén, mivel a hepatitis B vírusnak nincs citopatogén hatása. Ez az álláspont nem tekinthető vitathatatlannak, mivel kísérleti adatokon alapul, amelyek bár a hepatitis B vírus citopatogén hatásának hiányát jelzik, szövetkultúrákon nyerték őket, és ezért nem extrapolálhatók teljes mértékben az emberi vírusos hepatitis B-re. Mindenesetre a replikációs fázis során a hepatocita-károsodás hiányának kérdése további vizsgálatokat igényel.
Azonban, függetlenül a vírus és a sejt közötti kölcsönhatás jellegétől, a máj szükségszerűen részt vesz az immunopatológiai folyamatban. Ebben az esetben a hepatociták károsodása azzal jár, hogy a vírusantigének a hepatocita membránon történő expressziója és a vírusantigének szabad keringésbe való felszabadulása következtében egymást követő sejtes és humorális immunreakciók láncolata játszódik le, amelyek végső soron a vírus eltávolítását célozzák a szervezetből. Ez a folyamat a vírusfertőzésekre adott immunválasz általános mintázatainak teljes betartásával zajlik. A kórokozó eliminálása érdekében sejtes citotoxikus reakciók lépnek fel, amelyeket az effektor sejtek különböző osztályai közvetítenek: K-sejtek, T-sejtek, természetes ölősejtek, makrofágok. Ezen reakciók során a fertőzött hepatociták elpusztulnak, amit vírusantigének (HBcAg, HBeAg, HBsAg) felszabadulása kísér, amelyek beindítják az antitestképződési rendszert, aminek következtében specifikus antitestek halmozódnak fel a vérben, elsősorban a mag - anti-HBc és e-antigén - anti-HBE ellen. Következésképpen a májsejt felszabadulása a vírusból a sejtes citolízis reakciói miatt bekövetkező halálának folyamatában történik.
Ugyanakkor a vérben felhalmozódó specifikus antitestek kötődnek a vírus antigénjeihez, immunkomplexeket képezve, amelyeket a makrofágok fagocitálnak, és a vesék választanak ki. Ebben az esetben különféle immunkomplex-elváltozások léphetnek fel glomerulonephritis, arteritis, artralgia, bőrkiütés stb. formájában. A specifikus antitestek részvételével a szervezet megtisztul a kórokozótól, és teljes felépülés következik be.
A hepatitis B patogenezisének vázolt koncepciójával összhangban a betegség lefolyásának klinikai változatainak sokféleségét általában a vírus kölcsönhatásának és az immunkompetens sejtek együttműködésének sajátosságai, vagyis a vírusantigének jelenlétére adott immunválasz erősségével magyarázzák. A modern koncepciók szerint az immunválasz erőssége genetikailag meghatározott, és az első osztályú HLA-lókusz hisztokompatibilitási antigénjeihez kapcsolódik.
Általánosan elfogadott, hogy a vírusantigénekkel szembeni megfelelő immunválasz esetén az akut hepatitis klinikailag ciklikus lefolyással és teljes felépüléssel alakul ki. A vírusantigénekkel szembeni immunválasz csökkenésének hátterében az immunközvetített citolízis jelentéktelen mértékben expresszálódik, ezért a fertőzött májsejtek hatékony eliminációja nem következik be, ami enyhe klinikai tünetekhez vezet, a vírus hosszú távú perzisztenciájával és esetleg krónikus hepatitisz kialakulásával. Ugyanakkor, éppen ellenkezőleg, genetikailag meghatározott erős immunválasz és masszív fertőzés (hemotranszfúzió) esetén a májsejtek kiterjedt károsodása alakul ki, amelyek klinikailag a betegség súlyos és rosszindulatú formáinak felelnek meg.
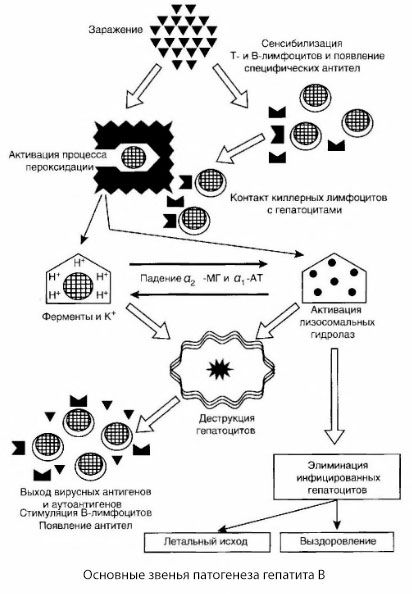
A hepatitis B patogenezisének bemutatott sémáját koherenciája jellemzi, azonban számos ellentmondásos és kevéssé tanulmányozott pontot tartalmaz.
Ha a hepatitis B-t immunopatológiai betegségként tekintjük, akkor a betegség súlyosságának növekedésével a sejtes citotoxicitási reakciók növekedésére számíthatunk. Súlyos formákban azonban az immunitás sejtes kapcsolatának mutatói jelentősen csökkennek, beleértve a többszörös csökkenést is az egészséges gyermekeknél mért értékekhez képest, valamint a K-sejt citotoxicitási indexe. Malignus formában, a masszív májnekrózis és különösen a májkóma kialakulása során a limfociták teljesen képtelenek blaszt transzformációra fitohemattlutinin, staphylococcus endotoxin és HBsAg hatására. Ezenkívül a leukociták nem képesek a leukocita migráció gátlási reakció (LMIC) szerinti migrációra, és a limfocita membránok permeabilitásának hirtelen növekedése figyelhető meg a fluoreszcens tetraciklin próbával végzett vizsgálatok eredményei szerint.
Tehát, ha az egészséges emberekben a limfociták fluoreszcencia indexei 9,9±2%, és jóindulatú lefolyású tipikus hepatitis B esetén 22,3±2,7%-ra emelkednek, akkor rosszindulatú formákban a fluoreszcens limfociták száma átlagosan eléri a 63,5±5,8%-ot. Mivel a sejtmembránok permeabilitásának növekedését az irodalom egyértelműen a funkcionális inferioritásuk megbízható mutatójaként értékeli, arra lehet következtetni, hogy hepatitis B esetén, különösen rosszindulatú formában, a limfociták súlyos károsodása figyelhető meg. Ezt a K-sejtek citotoxicitásának indexei is bizonyítják. Súlyos formában, a betegség 1-2. hetében a citotoxicitás 15,5±8,8%, rosszindulatú formában pedig az 1. héten 6,0±2,6, a 2. héten pedig 22,0±6,3%, a normál érték 44,8±2,6%.
A bemutatott adatok egyértelműen a hepatitis B súlyos formáiban szenvedő betegek immunitásának sejtes kapcsolatában jelentkező kifejezett zavarokra utalnak. Az is nyilvánvaló, hogy ezek a változások másodlagosan jelentkeznek, az immunkompetens sejtek toxikus metabolitok és esetleg keringő immunkomplexek általi károsodása következtében.
Amint azt a tanulmányok kimutatták, súlyos hepatitis B formájú betegeknél, különösen masszív májnekrózis kialakulása esetén, a HBsAg és a HBeAg titere a vérszérumban csökken, és ugyanakkor a felszíni antigén elleni antitestek magas titerben kezdenek kimutatni, ami teljesen jellemző a betegség jóindulatú formáira, amelyekben az anti-HBV csak a betegség 3-5. hónapjában jelenik meg.
A hepatitis B vírus antigének gyors eltűnése a vírusellenes antitestek magas titerének egyidejű megjelenésével az immunkomplexek intenzív képződésére és a masszív májnekrózis kialakulásának patogenezisében való esetleges részvételükre utal.
Így a tényszerű anyagok nem teszik lehetővé, hogy a hepatitis B-t egyértelműen csak az immunpatológiai agresszió szempontjából értelmezzük. És a lényeg nem csak az, hogy nem találtak összefüggést egyrészt a máj morfológiai változásainak mélysége és előfordulási gyakorisága, másrészt a sejtes immunitási faktorok súlyossága között. Elméletileg ez a körülmény a sejtes immunitás indikátorainak tanulmányozásának késői szakaszaival magyarázható, amikor az immunkompetens sejteket erős toxikus hatások érték a máj fokozódó funkcionális elégtelensége miatt. Természetesen feltételezhető, hogy a hepatociták immuncitolízise a fertőző folyamat legkorábbi szakaszában, esetleg még a súlyos májkárosodás klinikai tüneteinek megjelenése előtt is bekövetkezik. Ez a feltételezés azonban valószínűtlen, mivel a sejtes immunitás hasonló indikátorait a betegség legakutabb (villámgyors) lefolyású betegeknél is észlelték, és emellett a májszövet morfológiai vizsgálata során nem észleltek masszív limfocitás infiltrációt, ugyanakkor a nekrotikus hám folyamatos mezőit észlelték a felszívódás és a limfocitás agresszió jelensége nélkül.
Nagyon nehéz az akut hepatitisz morfológiai képét csak az immunsejtes citolízis szempontjából megmagyarázni, ezért a korai vizsgálatokban a hepatitis B vírus citotoxikus hatását nem zárták ki.
Jelenleg ezt a feltételezést részben megerősítette a hepatitis B vírus felfedezése. Amint azt a tanulmányok kimutatták, a hepatitis D markerek kimutatásának gyakorisága közvetlenül függ a betegség súlyosságától: enyhe formákban a betegek 14%-ánál, közepesen súlyos - 18%-ánál, súlyos - 30%-ánál, rosszindulatú - pedig 52%-ánál észlelhetők. Figyelembe véve, hogy a hepatitis D vírus nekrogén citopátiás hatást fejt ki, megállapítottnak tekinthető, hogy a hepatitis B és D vírusokkal való koinfekció nagy jelentőséggel bír a hepatitis B fulmináns formáinak kialakulásában.
A hepatitis B patogenezise a következőképpen mutatható be. Miután a hepatitis B vírus bejut a hepatocitákba, a T-killerek immunológiai támadást indítanak el a fertőzött hepatociták ellen, amelyek limfotoxinokat választanak ki a májsejtek irányába.
A hepatitis B májsejt-károsodásának intim mechanizmusai még nem tisztázottak. A vezető szerepet a lipidperoxidáció és a lizoszomális hidrolázok aktivált folyamatai játsszák. A kiváltó ok lehet a limfotoxinok felszabadulása az effektor sejtekből a hepatocitákkal való érintkezéskor, de lehetséges, hogy maga a vírus is a peroxidációs folyamatok iniciátora. Ezt követően a kóros folyamat valószínűleg a következő sorrendben alakul ki.
- Az agressziót kiváltó faktor (limfotoxinok vagy vírus) kölcsönhatása biológiai makromolekulákkal (esetleg az endoplazmatikus retikulum membránjainak olyan komponenseivel, amelyek képesek részt venni a méregtelenítő folyamatokban, más károsító szerekkel analóg módon, ahogyan azt a szén-tetrakloriddal kapcsolatban is kimutatták).
- Szabad gyökök képződése, a lipidperoxidációs folyamatok aktiválódása és az összes májsejtmembrán permeabilitásának növekedése (citolízis szindróma).
- Biológiailag aktív anyagok mozgása a koncentrációgradiens mentén - különböző intracelluláris lokalizációjú enzimek, energiadonorok, kálium stb. elvesztése. Nátrium és kalcium felhalmozódása a sejtekben, a pH eltolódása az intracelluláris acidózis felé.
- Lizoszómális hidrolázok (RNS-áz, DNS-áz, katepszin stb.) aktiválódása és felszabadulása a májsejtek lebomlásával és autoantigének felszabadulásával.
- A T- és B-immunrendszer stimulálása a T-limfociták máj lipoproteinre gyakorolt specifikus szenzitizációjának kialakulásával, valamint antihepatikus humorális autoantitestek képződésével.
A hepatitis B patogenezisének javasolt sémájában a kiváltó tényező a vírusantigének, amelyek intenzív termelését a betegség legkorábbi szakaszaiban és az egész akut időszakban figyelik meg, kivéve a rosszindulatú formákat, amelyekben a vírusantigének termelése gyakorlatilag megszűnik a masszív májnekrózis kialakulásakor, ami a vírusreplikáció gyors csökkenését határozza meg.
Az is nyilvánvaló, hogy a vírusantigének aktiválják az immunitás T- és B-rendszerét. E folyamat során a T-limfocita alpopulációk jellegzetes újraeloszlása következik be, amelynek célja a megfelelő immunválasz megszervezése, a fertőzött hepatociták eltávolítása, a vírusantigének semlegesítése, a sanogenezis és a gyógyulás.
Amikor az immunkompetens sejtek kölcsönhatásba lépnek a vírusantigénekkel a hepatocita membránjain vagy a vírus szaporodása során a hepatocitában, feltételek alakulnak ki a lipidperoxidációs folyamatok aktiválódásához, amelyek, mint ismert, szabályozzák az összes sejtes és szubcelluláris membrán permeabilitását.
Ebből a pozícióból érthetővé válik a citolízis szindróma előfordulása, a sejtmembránok fokozott permeabilitása, amely annyira természetes és a vírusos hepatitiszre nagyon jellemző.
A citolízis szindróma végeredménye az oxidatív foszforiláció teljes szétkapcsolódása, a sejtes anyag szivárgása és a máj parenchyma elhalása lehet.
Az esetek túlnyomó többségében azonban ezek a folyamatok nem válnak ilyen végzetessé. Csak a betegség rosszindulatú formáiban zajlik le a kóros folyamat lavinaszerűen és visszafordíthatatlanul, mivel masszív fertőzés, kifejezett immunfolyamat, a peroxidációs folyamatok és a lizoszomális hidrodázok túlzott aktiválódása, valamint autoimmun agressziós jelenségek lépnek fel.
Ugyanezek a mechanizmusok figyelhetők meg a hepatitis B kedvező lefolyásában is, azzal az egyetlen sajátossággal, hogy mindegyik minőségileg eltérő szinten valósul meg. A masszív májnekrózis eseteivel ellentétben a betegség kedvező lefolyásában a fertőzött hepatociták száma, és így az immunpatológiai citolízis zónája is kisebb, a lipidperoxidációs folyamatok nem fokozódnak olyan jelentősen, a savas hidrolázok aktiválódása csak korlátozott autolízist eredményez, jelentéktelen autoantigének felszabadulásával, ezért masszív autoagresszió nélkül, azaz a kedvező lefolyásban a patogenezis minden szakasza a máj parenchyma megőrzött szerkezeti szerveződésének keretében zajlik, és védekező rendszerek (antioxidánsok, inhibitorok stb.) által korlátozva van, ezért nincs ilyen romboló hatásuk.
A vírusos hepatitisz mérgezési tüneteinek okait még nem vizsgálták teljes mértékben. Az úgynevezett primer vagy vírusos mérgezés és a másodlagos (csere- vagy metabolikus) megkülönböztetésére irányuló javaslat pozitívnak tekinthető, bár ez nem tárja fel az általános toxikus szindróma előfordulásának intim mechanizmusát. Először is, a hepatitiszvírusok nem rendelkeznek toxikus tulajdonságokkal, másodszor pedig számos metabolit koncentrációja nem mindig korrelál a betegség súlyosságával és a toxikózis tüneteinek kifejeződésének mértékével. Az is ismert, hogy a vírusantigének koncentrációja nem mindig korrelál szigorúan a mérgezés súlyosságával. Épp ellenkezőleg, a betegség súlyosságának növekedésével, és ennek következtében a toxikózis mértékének növekedésével a HBsAg koncentrációja csökken, és a rosszindulatú formákban a mély májkóma kialakulásának idején a legalacsonyabb. Ugyanakkor a specifikus vírusellenes antitestek kimutatásának gyakorisága és titere közvetlenül függ a betegség súlyosságától.
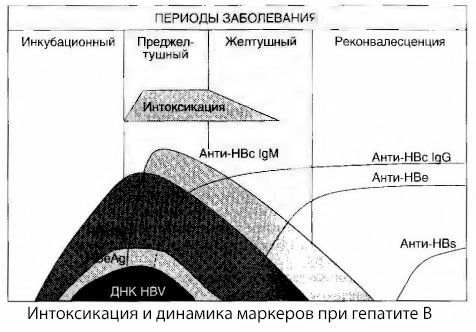
A mérgezés nem a vírusantigének regisztrálásának pillanatában, hanem a tehénantigénnel és az E rendszer antigénjével szembeni IgM osztályú vírusellenes antitestek vérkeringésének időszakában jelentkezik. Súlyos és különösen rosszindulatú formákban a betegek jelentős részénél még anti-HBs is jelen van a vérben, ami általában soha nem figyelhető meg a betegség enyhe és közepes formáiban.
A bemutatott adatok arra engednek következtetni, hogy a vírusos hepatitiszben, és különösen a hepatitis B-ben fellépő toxikózis szindróma nem a vírusantigének vérben való megjelenésének eredményeként alakul ki, hanem a vírusantigének és az IgM osztályú vírusellenes antitestek kölcsönhatásának következménye. Az ilyen kölcsönhatás eredménye, mint ismert, immunkomplexek és esetleg aktív toxikus anyagok képződése.
A mérgezés tünetei az immunkomplexek szabad keringésben való megjelenésének pillanatában jelentkeznek, de később ilyen összefüggést nem figyelnek meg.
Ennek részleges magyarázata az immunkomplexek összetételének vizsgálatában található. Súlyos formákban szenvedő betegeknél túlnyomórészt közepes méretű komplexek keringenek a vérben, és összetételükben a toxikus szindróma csúcspontján az osztályba tartozó antitestek dominálnak, míg a klinikai tünetek hanyatlásának és a lábadozás időszakában a komplexek nagyobbak lesznek, és összetételükben az IgG osztályú antitestek kezdenek dominálni.
A bemutatott adatok a toxikus szindróma kialakulásának mechanizmusaira vonatkoznak a betegség kezdeti szakaszában, de a klinikai tünetek csúcspontján jelentkező toxikózis esetén csak részleges jelentőségük van, különösen a májkóma kialakulásában.
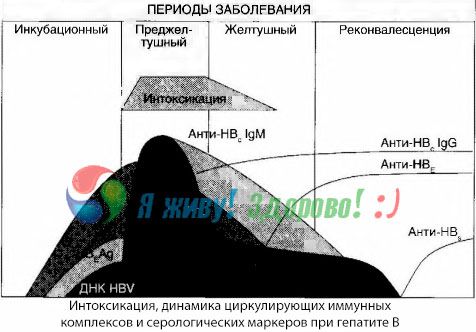
A vérkultúrás módszer kimutatta, hogy a hepatitis B esetén a toxinok folyamatosan felhalmozódnak a vérben, amelyek a sérült, bomló májszövetből szabadulnak fel. Ezeknek a toxinoknak a koncentrációja arányos a betegség súlyosságával, fehérje jellegűek.
A felépülési időszak alatt a toxin elleni antitestek megjelennek a vérben; de májkóma esetén a toxin koncentrációja a vérben hirtelen megnő, és az antitestek nem mutathatók ki a vérben.
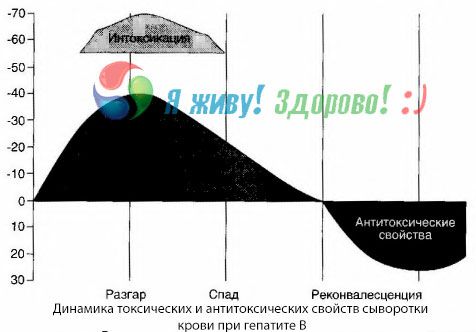
A hepatitis B patomorfológiája
A morfológiai változások jellege alapján az akut hepatitis B három formáját különböztetjük meg:
- ciklikus forma,
- masszív májnekrózis;
- cholestaticus pericholangiolitikus hepatitis.
A hepatitis B ciklikus formájában a disztrófiás, gyulladásos és proliferatív változások a lebenykék középpontjában hangsúlyosabbak, míg hepatitis A esetén a lebenykék perifériája mentén lokalizálódnak, és a középpont felé terjednek. Ezeket a különbségeket a vírus máj parenchymába való behatolásának eltérő útjai magyarázzák. A hepatitis A vírus a portális vénán keresztül jut be a májba, és a lebenykék középpontjáig terjed, a hepatitis B vírus a májartérián és a kapilláris ágakon keresztül hatol be, amelyek egyenletesen ellátóak az összes lebenykékben, egészen a közepükig.
A máj parenchyma károsodásának mértéke a legtöbb esetben megfelel a betegség klinikai megnyilvánulásainak súlyosságának. Enyhe formákban általában a hepatociták fokális nekrózisa figyelhető meg, közepes és súlyos formákban pedig zonális nekrózis (a betegség súlyos formáiban hajlamos az összeolvadásra és hídszerű nekrózis kialakulására).
A parenchyma legnagyobb morfológiai változásai a klinikai tünetek csúcspontján figyelhetők meg, ami általában egybeesik a betegség első évtizedével. A második és különösen a harmadik évtizedben a regenerációs folyamatok felerősödnek. Erre az időszakra a nekrobiotikus változások szinte teljesen eltűnnek, és a sejtes infiltrációs folyamatok kezdenek dominálni, a májsejtlemezek szerkezetének lassú helyreállításával. A máj parenchyma szerkezetének és funkciójának teljes helyreállítása azonban csak a betegség kezdete után 3-6 hónappal következik be, és nem minden betegnél.
A hepatitis B fertőzés generalizált jellegét a HBsAg kimutatása nemcsak a hepatocitákban, hanem a vesékben, a tüdőben, a lépben, a hasnyálmirigyben, a csontvelősejtekben stb. is megerősíti.
A kolesztatikus (perikolangiolitikus) hepatitis a betegség egy speciális formája, amelyben a legnagyobb morfológiai változások az intrahepatikus epeutak részén figyelhetők meg, kolangiolitisz és perikolangiolitisz képével. A kolesztatikus formában a kolesztázis az epevezetékek kitágulásával, az epe pangásával, a kolangiolák és a körülöttük lévő sejtes infiltrátumok proliferációjával jelentkezik. A májsejteket ebben a hepatitiszformában jelentéktelenül érinti. Klinikailag a betegséget elhúzódó lefolyás jellemzi, hosszan tartó sárgasággal. Kimutatták, hogy a betegség ilyen sajátos lefolyásának oka a vírus domináns hatása a kolangiolák falára, a hepatocitákra gyakorolt jelentéktelen hatással.

