A cikk orvosi szakértője
Új kiadványok
Máj amiloidózis
Utolsó ellenőrzés: 29.06.2025

Minden iLive-tartalmat orvosi szempontból felülvizsgáltak vagy tényszerűen ellenőriznek, hogy a lehető legtöbb tényszerű pontosságot biztosítsák.
Szigorú beszerzési iránymutatásunk van, és csak a jó hírű média oldalakhoz, az akadémiai kutatóintézetekhez és, ha lehetséges, orvosilag felülvizsgált tanulmányokhoz kapcsolódik. Ne feledje, hogy a zárójelben ([1], [2] stb.) Szereplő számok ezekre a tanulmányokra kattintható linkek.
Ha úgy érzi, hogy a tartalom bármely pontatlan, elavult vagy más módon megkérdőjelezhető, jelölje ki, és nyomja meg a Ctrl + Enter billentyűt.
Az amiloidózis általában egy szisztémás, általános patológia, amelyet az amiloid (egy specifikus glikoprotein) felhalmozódása jellemez a szövetekben, és ennek következtében a normális szervműködés megzavarása. A májamiloidózis sokkal ritkább, mint a vese és a lép amiloidózisa [ 1 ], de szinte mindig a szervezet szisztémás károsodásával jár. A meglévő képalkotó technikák egyike sem képes specifikusan kimutatni az amiloid jelenlétét. Még klinikai és radiológiai gyanú esetén is az amiloidózis diagnózisa a szövetbiopsziától függ, amely megerősíti az amiloid lerakódások jelenlétét. [ 3 ] A kezelés összetett, átfogó, és immunszuppresszív és tüneti intézkedéseket foglal magában. Súlyos esetekben májátültetésre lehet szükség.
Járványtan
A kezelés sikere közvetlenül függ a betegség időben történő diagnózisától, amely fehérje-poliszacharid komplex (amiloid) képződését okozza különböző szervekben és a májban. A gyakorlat azt mutatja, hogy az amiloidózist nehéz feltételezni vagy gyanítani, bár azonosítani és megerősíteni lehetséges. A tény az, hogy a fel nem ismert esetek több mint 80%-ában a betegséget klinikailag májpatológia maszkolja. A leghatékonyabb diagnosztikai módszer a biopszia.
A májamiloidózis ritkább probléma a veseamiloidózishoz képest. Ugyanakkor a májkárosodás minden esetét más szervek károsodása kíséri. A patológia leggyakrabban a májtriász strukturális részeit érinti, ami meghatározza a tünetek minimális és nem specifikus jellegét. A hepatocelluláris hiány és a portális hipertónia klinikai és morfológiai képe diffúz és intralobuláris típusú patológiában nyilvánul meg.
Májbiopszia indokolt, ha hepatomegalia áll fenn korábbi májtünetek nélkül, és nincs nephrotikus szindróma.
Az esetek körülbelül 25%-ában diffúz májérintettség fordul elő, a betegek 75%-ánál pedig csak a portális traktusok érintettek.
Az elsődleges amiloidózis az esetek 90%-ában a májat érinti, míg a másodlagos amiloidózis csak az esetek 47%-ában.
Izolált májérintettség rendkívül ritka. A vesék (az esetek körülbelül 93%-a), a lép (72%), a szív (57%), a hasnyálmirigy (36%), a mellékvesék (29%), a belek és a tüdő (mindegyik 21%) általában egyszerre érintettek.
A nők majdnem kétszer olyan gyakran kapják el a betegséget, mint a férfiak. Az amiloidózisban szenvedő betegek átlagos várható élettartama 52-64 év.
Okoz májamyloidosis
Az amiloidózis egy komplex poliszacharid-fehérje komplex - amiloid - képződésével és felhalmozódásával jár a májszövetben. Az elsődleges elváltozás előfordulásának problémáját a mai napig nem vizsgálták kellőképpen. Ami a másodlagos patológiát illeti, megjelenése általában az ilyen betegségekkel jár:
- Krónikus fertőző folyamatok (tuberkulózis, szifilisz, aktinomikózis);
- Gennyes gyulladásos folyamatok (mikrobiális endocarditis, osteomyelitis, bronchiectaticus betegség stb.);
- Rosszindulatú betegségek (leukémia, zsigeri rák, limfogranulomatózis).
Az amiloidózis reaktív formája olyan betegeknél fordul elő, akik egyidejűleg ateroszklerózissal, reumatológiai betegségekkel (Bechterew-kór, reumatoid artritisz), pikkelysömörrel, krónikus gyulladásos és több szervrendszert érintő folyamatokkal (beleértve a szarkoidózist is) is küzdenek. A fő kockázati tényezők: örökletes hajlam, sejtes immunitás zavarai, hiperglobulinémia.
Pathogenezis
Számos feltételezés létezik a máj amiloidózis eredetével kapcsolatban. A legtöbb szakember a diszproteinózis, a betegség immunológiai és mutációs jellege, valamint a lokális sejtgenezis változatát vallja. A sejtgenezis változata magában foglalja a sejtek szintjén ható reakciók változásait (az amiloid fibrilláris prekurzorainak képződése makrofágok komplexe által), bár az amiloid a sejtszerkezeteken kívül is képződik és halmozódik fel.
A diszproteinózis azon a tényen alapul, hogy az amiloid a nem megfelelő fehérje-anyagcsere terméke. A probléma alapvető patogenetikai kapcsolata a diszproteinémia és a hiperfibrinogenémia, amelyek a durva diszpergált fehérje- és paraproteinfrakciók felhalmozódásához vezetnek a plazmában.
Az immunológiai változat szerint az amiloid képződését antigén-antitest reakció okozza, ahol a szöveti bomlástermékek vagy idegen fehérjék antigénként működnek. Az amiloid felhalmozódása főként az antitestképződés és az antigének túlzott jelenléte területén található.
A tudósok a mutációelméletet tartják a leghihetőbb változatnak, amely figyelembe veszi a fehérjeszintézis rendellenességeihez vezető különféle mutagén tényezőket.
Az amiloid egy komplex hipoprotein, amely globuláris és fibrilláris fehérjékből, valamint poliszacharidokból áll. Az amiloid felhalmozódások befolyásolják az érhálózat intimáját és adventiciáját, a parenchymás szervek stromáját, a mirigyek szerkezetét stb. Az amiloid felhalmozódások nem okoznak funkcionális károsodást. A kis felhalmozódások nem okoznak funkcionális zavarokat, de intenzív amiloid jelenlét esetén a máj térfogata megnő, megváltozik a szerv megjelenése, és funkcióvesztés alakul ki.
A máj amiloidózist az amiloid fibrillumok lerakódása jellemzi a Dysse-térben, ami általában a periportális régióban kezdődik, bár néha centrilobuláris jellegű, és a máj érrendszerében is lerakódhat. [ 4 ], [ 5 ] Súlyos esetekben az amiloid lerakódás a hepatociták nyomás miatti atrófiájához vezet, ami megakadályozza az epe átjutását, ami epepangást eredményez, vagy elzárhatja a sinusoidokat, ami portális hipertóniát eredményez. [ 6 ], [ 7 ], [ 8 ]
Tünetek májamyloidosis
A máj amiloidózis klinikai képe változatos, az amiloid felhalmozódásának intenzitásától, biokémiai jellemzőitől, a kóros folyamat időtartamától, a szervkárosodás mértékétől és funkcionális állapotuk zavarától függ.
Az amiloidózis látens stádiumában, amikor az amiloid felhalmozódása a májban csak mikroszkópos vizsgálattal kimutatható, a betegség első jelei hiányoznak. A további fejlődéssel és a szerv növekvő funkcionális deficitjével a tünetek súlyosbodnak.
A máj fokozatosan vastagszik, megnagyobbodik. A tapintás módszerével a szerv megváltozott, de sima és fájdalommentes határai tapinthatók. Ritkán a patológiát a jobb oldali szubkostális régióban jelentkező fájdalom, emésztési zavarok, a lép megnagyobbodása, a bőr, a nyálkahártyák és az ínhártyák sárgulása, vérzéses szindróma kíséri.
A máj amiloidózis legjellemzőbb tünetei: [ 9 ], [ 10 ]
- Az amiloid felhalmozódása a májban a betegek 33-92%-ánál hepatomegaliát okoz;
- Enyhe sárgaság
- Portális hipertónia;
- Közepes vagy súlyos epeúti elzáródás.
Mivel az amiloidózis nagyon ritkán érinti csak egy szervet, általában további tünetek is jelen vannak:
- Vesekárosodás esetén nephrotikus szindróma és artériás magas vérnyomás alakul ki, további veseelégtelenséggel, ödémával, néha vesevénás trombózissal, leukocituriával, hematuriával, hipoproteinémiával, azotémiával és így tovább;
- Amikor a szív érintett, a restriktív kardiomiopátiához hasonló állapot alakul ki (ritmuszavarok, kardiomegalia, növekvő szívdeficit, gyengeség és nehézlégzés, ödéma, ritkábban - folyadék felhalmozódása a hasüregben és a pleurális üregben, szívburokgyulladás);
- Ha az emésztőrendszer érintett, makroglossia, gyengeség és nyelőcső-perisztaltika, hányinger és gyomorégés, székrekedés vagy hasmenés stb. előfordulhat;
- Amikor a hasnyálmirigy érintett, krónikus hasnyálmirigy-gyulladás tünetei jelentkeznek;
- Ha a mozgásszervi mechanizmus érintett, szimmetrikus polyarthritis, carpalis alagút szindróma, myopathiák alakulnak ki, és ha az idegrendszer érintett, polyneuropatiák, bénulás, ortosztatikus alacsony vérnyomás, fokozott izzadás, demencia alakul ki.
Ha a kóros reakció átterjed a bőrre, számos viaszos plakk jelenik meg az arcon, a nyakon, a bőrredőkben. Lehetséges a neurodermatitisz, a vörös laphámláz és a szkleroderma képe.
A többszörös amiloid elváltozások kombinációja és a tünetek sokfélesége sokkal nehezebbé teszi a máj amiloidózis azonosítását, és átfogó és teljes diagnózist igényel.
Forms
A WHO osztályozása szerint az amiloidózis öt típusát különböztetik meg:
- AL (elsődleges);
- AA (másodlagos);
- ATTR (örökletes és szenilis szisztémás);
- Aβ2M (hemodialízisben részesülő betegeknél);
- AIAPP (inzulin-független cukorbetegségben szenvedő betegeknél);
- AB (Alzheimer-kór esetén);
- AANF (szenilis pitvari amiloidózis).
Lokális májamiloidózis létezik, de gyakrabban szisztémás elváltozásról van szó, amelyben a kóros folyamat a veséket, a szívet, a lépet, az idegrendszert, valamint más szerveket és szöveteket is érinti.
Komplikációk és következmények
A szisztémás amiloidózis fokozatosan akut kóros folyamatok kialakulásához vezet, amelyek viszont halálhoz vezethetnek. A leggyakoribb és életveszélyes szövődmények közé tartoznak a következők:
- Gyakori fertőző (bakteriális, vírusos) patológiák, beleértve a tüdőgyulladást, pyelonephritist, glomerulonephritist;
- Krónikus máj- és veseelégtelenség;
- Krónikus szívelégtelenség (megelőzheti a miokardiális infarktust);
- Vérzéses stroke-ok.
A vénás trombózis a fehérjék vénás falakon történő felhalmozódása és lerakódása következtében alakul ki. Az érintett erek lumenje szűkül, szervleállás alakul ki. Idővel, a hosszú távú hiperproteinémia hátterében az ér teljesen elzáródhat. Bármelyik szövődmény kedvezőtlen kimenetelhez - halálhoz - vezethet.
Diagnostics májamyloidosis
Májamiloidózis gyanúja esetén a diagnosztikai intézkedéseket kötelező konzultációk után végzik, mind gasztroenterológussal és terapeutával, mind reumatológussal, kardiológussal, bőrgyógyásszal, neurológussal, urológussal. Fontos az anamnézis és a klinikai tünetek átfogó értékelése, átfogó laboratóriumi és műszeres diagnosztika elvégzése.
A vizsgálatok szükségszerűen magukban foglalják a vizelet- és vérvizsgálatot. Májamiloidózis esetén gyakran leukocituria, proteinuria és cilindruria kombinációja, hipoproteinémia pedig hiperlipidémiával, vérszegénységgel, hiponatrémiával és hipokalcémiával, valamint csökkent vérlemezkeszámmal társul. A paraproteineket vizeletben és szérumelektroforézisben mutatják ki.
Az instrumentális diagnosztika a következőket tartalmazza:
- EKG, visszhang;
- Hasi ultrahang;
- A gyomor, a nyelőcső röntgenfelvételei;
- Irrigográfia, bárium röntgen;
- Endoszkópia.
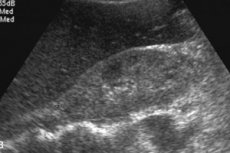
A máj amiloidózis radiológiai leletei közé tartozik a nem specifikus hepatomegalia, a fokozott echogenitás ultrahangon vagy a sűrűség komputertomográfián (CT), valamint a megnövekedett T1 jelintenzitás mágneses rezonancia képalkotáson (MRI). [ 12 ] A Tc-99m-mel kapcsolatos indikátorokkal végzett szcintigráfia heterogén felvételt mutat, de ez nem specifikus. [ 13 ], [ 14 ] Kimutatták, hogy a GC növeli a máj elasztográfiával mért merevségét; [ 15 ], [ 16 ], [ 17 ], de kevés esetismertetés áll rendelkezésre. A mágneses rezonancia elasztográfia (MRE) jelenleg a legpontosabb, nem invazív módszer a májfibrózis kimutatására és stádiumának meghatározására, [ 18 ], [ 19 ] Az MRE hasznos a progresszió, a kezelésre adott válasz kimutatására és a májdekompenzáció előrejelzésére májfibrózisban szenvedő betegeknél. [ 20 ]
Az ultrahanggal kimutatható máj amiloidózis nehezen meghatározható: a szerv megnagyobbodása figyelhető meg, a legspecifikusabb hepatomegalia meghaladja a 15 cm-t. Ultrahangvezérléssel biopsziát végeznek, amely meghatározó indikátorrá válik a diagnózisban. Egy speciális tű segítségével kis mennyiségű májszövetet vesznek, majd egy speciális festékkel festik és mikroszkóp alatt vizsgálják, ami lehetővé teszi az amiloid lerakódások közvetlen vizsgálatát.
A végleges diagnózist csak az amiloid fibrillumok kimutatása után állítják fel a máj és más szervek szövetében. Az amiloidózis genetikailag meghatározott típusát a törzskönyv gondos genetikai-orvosi vizsgálata határozza meg.
Megkülönböztető diagnózis
Amiloidózis gyanúja merül fel minden olyan betegnél, akinél veseelégtelenségben szenvedő betegnél proteinuria, restriktív kardiomiopátia, autonóm vagy perifériás neuropátia és hepatomielia kombinációja áll fenn, még monoklonális paraprotein hiányában is. Az amiloidózis típusának ellenőrzése nagyon fontos, mivel a különböző etiológiájú elváltozások kezelése nagyon eltérő.
A szövettani diagnózis kongóvörös festést, majd polarizáló fényben végzett mikroszkópos vizsgálatot foglal magában. Célszerű egyszerre több szövetmintát biopsziával venni. Ha a festés eredménye pozitív, immunhisztokémiai analízist végeznek prekurzor fehérjék elleni monoklonális antitestekkel az amiloid típusának azonosítására.
A DNS-analízist az elsődleges amiloidózis és a genetikailag meghatározott amiloidózis különböző variációinak megkülönböztetésére végzik. Az amiloid fibrillumok biopsziás mintákból izolálhatók és egyedi aminosavakra bonthatók.
További vizsgálatok a plazmasejtes diszkrázia meghatározására:
- A vér és a vizelet szérumfehérjéinek elektroforézise;
- Szabad könnyűláncok immunvizsgálata;
- Szérumfehérjék immunfixációja (immunoblotolás);
- Csontvelő-aspiráció és trepanobiopszia.
A máj amiloidózis diagnózisa hosszadalmas és munkaigényes folyamat, amely fokozott figyelmet igényel a szakemberektől, valamint a klinikák és laboratóriumok minőségi felszerelését.
Ki kapcsolódni?
Kezelés májamyloidosis
A kezelési intézkedések célja a már meglévő amiloid fehérjék koncentrációjának csökkentése a vérben (az amiloidózis okának kiküszöbölése) és a megfelelő májfunkció támogatása.
A másodlagos amiloidózis a gyulladásos folyamat blokkolását igényli (krónikus fertőző és autoimmun patológiákban). Autoimmun betegségek esetén citosztatikumok alkalmazása ajánlott. A krónikus fertőző folyamatok kiküszöbölése érdekében a gyulladás területét gyakran sebészeti úton eltávolítják. Ez a megközelítés gyakran megállíthatja az amiloidózis további progresszióját és javíthatja a májfunkciót.
Az elsődleges amiloidózis kemopreventív gyógyszerek alkalmazását és néha csontvelő-átültetést igényel.
A jelenlegi irányelvek a ciklofoszfamid, bortezomib, dexametazon (CyBorD) és daratumumab kombinációját javasolják első vonalbeli terápiaként az újonnan diagnosztizált AL-betegeknél.
A bortezomib egy proteaszóma-gátló. A proteaszómák részt vesznek a proteotoxicitás csökkentésében és a sejtek progresszióját és az apoptózist szabályozó fehérjék szabályozásában. Az amiloidot termelő plazmasejtek különösen érzékenyek a proteaszóma-gátlásra, mivel a proteaszómára támaszkodnak a könnyűláncok toxikus hatásainak csökkentésében és az apoptózis megelőzésében.
A daratumumumab egy monoklonális antitest (mAb), amely a CD38-hoz, egy a plazmasejtek felszínén expresszált transzmembrán glikoproteinhez kötődik, apoptózist indukálva. Ez az egyetlen olyan gyógyszer, amelyet kifejezetten az AL amiloidózis kezelésére engedélyeztek, ha CyBorD-val együtt alkalmazzák. A CyBorD-daratumumab hatékonysága nagyon magas, a betegek 78%-ánál jelentős hematológiai választ értek el (teljes válaszként vagy nagyon jó részleges válaszként definiálva). A CyBorD-t kapó betegek kis csoportjában (n = 15) a medián túlélés 655 nap volt, szemben a más melfalán-dexametazon alapú kezelést kapó betegek 178 napjával (n = 10).4
Ezeknek a terápiáknak azonban számos mellékhatása van, beleértve a kardiotoxicitást is, ami a dózis csökkentésének vagy a kezelés felfüggesztésének szükségességéhez, valamint más, kevésbé hatékony, de jobban tolerálható terápiás stratégiák alkalmazásához vezet.
Az isatuximabot, egy a daratumumabhoz hasonló CD38 elleni monoklonális antitestet, az AL alapjául szolgáló plazmasejtes diszkrázia kezelésében vizsgálják.
Jelenleg három monoklonális antitestet, a birtamimabot, a CAEL-101-et és az AT-03-at vizsgálják az amiloid fibrillumok eltávolítására a beteg szervekből. Ezen vizsgálatok eredményei közvetlen bizonyítékot szolgáltathatnak arra a hipotézisre, hogy a könnyűlánc-lerakódási fibrillumok eltávolításával a szervek működése javul. [ 21 ]
A májfunkció támogatása érdekében urso-dezoxikólsav alapú gyógyszereket írnak fel (például Ursosan). Az urso-dezoxikólsav segít stabilizálni a sejtmembránokat, csökkenti a mérgező zsírsavak káros hatását az amiloid lerakódások által kiváltott epepangásra, és segít helyreállítani a normális epe kiáramlását.
Ezenkívül tüneti terápia és más létfontosságú struktúrák, például az idegrendszer, a szív, a vesék stb. működésének támogatása. A májamiloidózisban szenvedő betegek támogató terápiája különféle klinikai szempontokat foglal magában, beleértve a szívelégtelenség, az aritmiák, az ingerületvezetési zavarok, a tromboembólia és az aorta-szűkület egyidejű jelenlétének kezelését.
Az egyéb kezelési módok az amiloidózis típusától és az érintett testrészektől függenek. A kezelések a következők lehetnek: [ 22 ]
- Tüneti gyógyszerek, például fájdalomcsillapítók, hányingercsillapítók vagy duzzanatot csökkentő gyógyszerek (vízhajtók);
- Az amiloidszint csökkentésére szolgáló gyógyszerek;
- Vese dialízis;
- Májátültetés.
A máj termeli a TTR (transztiretin, a tiroxin (T4) transzportjában részt vevő fehérje és retinol-kötő fehérje) 95%-át. A transztiretin főként a májban szintetizálódik, és gazdag béta-szálakban, amelyek hajlamosak oldhatatlan amiloid fibrillumokká aggregálódni) a szérumban mérve. Ezért a májátültetést történelmileg (1990 óta) első vonalbeli terápiaként javasolták az amiloidogén TTR fő forrásának kiküszöbölésére a familiáris formában (ATTRv) szenvedő betegeknél, míg az ATTR-wt formában nem javallt. A betegség korai stádiumában lévő fiatal betegek májátültetése magas 20 éves túlélési aránnyal jár. A májátültetés egyes mutációkban hatékonyabbnak, másokban, például a V122I-ben (kardiomiopátiával társulva) kevésbé hatékonynak tűnik. Kombinált máj- és szívátültetés is lehetséges fiatal ATTRv-betegeknél, akik kardiomiopátiát szenvednek, és a betegek egy kis csoportjára vonatkozó irodalmi adatok arra utalnak, hogy ez a kombináció jobb prognózissal jár, mint a szívátültetés önmagában.
Májamiloidózisban szenvedő betegeknél ellenjavallt a szívglikozidok és a kalciumantagonisták, például a diltiazem vagy a verapamil szedése, amelyek felhalmozódhatnak az amiloidban. Az ACE-gátlókat és a béta-adrenoblokkolókat óvatosan kell alkalmazni.
Ortosztatikus hipotenzió esetén mineralokortikoidokat vagy glükokortikoszteroidokat írnak fel, figyelembe véve, hogy ezek a szívelégtelenség dekompenzációját okozhatják. Az alfa-adrenomimetikus midodrint (Gutron) is óvatosan alkalmazzák.
Neuropátiák esetén az antikonvulzívumok és az antidepresszánsok megfelelőek.
A máj amiloidózis egyes eseteiben az orvosoknak mérlegelniük kell a szervátültetést.
Megelőzés
A májamiloidózis patogenezisével kapcsolatos információk hiánya miatt a szakemberek nem tudnak specifikus betegségmegelőzést kidolgozni. Ezért a fő erőfeszítések a rendellenesség kialakulását kiváltó krónikus patológiák időben történő felismerésére és kezelésére irányulnak. Ha a családban bármilyen lokalizációjú amiloidózis esetei vannak, ajánlott szisztematikusan felkeresni az orvosokat ambuláns vizsgálatokra.
Általánosságban elmondható, hogy a megelőző intézkedések a fertőző betegségek, különösen a krónikussá válásra hajlamosak időben történő megszüntetésére korlátozódnak. A tuberkulózis, a tüdőfertőzések stb. kialakulásának megelőzéséről van szó. Fontos a streptococcus fertőzések időben történő felismerése és megfelelő kezelése, amelyek az autoimmun gyulladásos folyamatok krónikus formáinak okává válhatnak. Skarlatináról, streptococcus okozta mandulagyulladásról stb. beszélünk.
Ha a betegnek már van autoimmun betegsége, akkor szisztematikusan konzultálnia kell orvosával, figyelnie kell a patológia aktivitását, alkalmaznia kell a szükséges gyógyszereket az orvos által előírt módon, és a jelzéseknek megfelelően módosítania kell az adagokat.
Előrejelzés
A májamiloidózisban szenvedő betegek prognózisa kedvezőtlen. A betegség lassan, de folyamatosan súlyosbodik, ami végül az érintett szervek diszfunkciójához és halálhoz vezet - különösen a szerv elégtelenség miatt.
A szisztémás patológiában szenvedő betegek főként krónikus veseelégtelenség kialakulásának következtében halnak meg, bár egyes esetekben a hemodialízis vagy a folyamatos ambuláns peritoneális dialízis javítja az ilyen betegek prognózisát. A hemodialízisben részesülő betegek túlélési aránya, típusától függetlenül, összehasonlítható más szisztémás patológiákban és cukorbetegségben szenvedőkével.
A hemodialízis során bekövetkező halálozás fő oka a szív- és érrendszeri szövődmények kialakulása.
A májátültetést régóta a betegség egyik fő kezelési módjának tekintik, és a legoptimistább túlélési arányokat azoknál a betegeknél figyelik meg, akiknek életkora nem haladja meg az 50 évet (feltéve, hogy a kóros folyamat rövid életű és a testtömegindex normális). A perifériás neuropátiával kombinált májamiloidózisban szenvedő betegek prognózisa valamivel rosszabb.

