A cikk orvosi szakértője
Új kiadványok
A prosztatarák stádiumainak diagnózisa
Utolsó ellenőrzés: 04.07.2025

Minden iLive-tartalmat orvosi szempontból felülvizsgáltak vagy tényszerűen ellenőriznek, hogy a lehető legtöbb tényszerű pontosságot biztosítsák.
Szigorú beszerzési iránymutatásunk van, és csak a jó hírű média oldalakhoz, az akadémiai kutatóintézetekhez és, ha lehetséges, orvosilag felülvizsgált tanulmányokhoz kapcsolódik. Ne feledje, hogy a zárójelben ([1], [2] stb.) Szereplő számok ezekre a tanulmányokra kattintható linkek.
Ha úgy érzi, hogy a tartalom bármely pontatlan, elavult vagy más módon megkérdőjelezhető, jelölje ki, és nyomja meg a Ctrl + Enter billentyűt.
Klinikailag megkülönböztetünk lokalizált (T1-2 , N0 , M0 ), lokálisan előrehaladott (T3-4 , N0-1 , M0 ) és generalizált rák (T1-4 , N0-1 , M1 ) között.
A klinikailag lokalizált és lokálisan előrehaladott stádiumú betegeket a kockázat mértéke szerint osztályozzák (D'Amico A V. et al., 2003):
- alacsony: T1a -c stádium; PSA-szint kevesebb, mint 10 ig/ml: Gleason-skála - 2-5; biopsziában - egyoldali elváltozás kevesebb, mint 50%:
- közepesen súlyos: T2a stádium; PSA-szint kevesebb, mint 10 ng/ml; Gleason-pontszám - 3 + 4 = 7; biopsziában - kétoldali lézió kevesebb, mint 50%;
- magas stádiumú T2b , T3a -b; PSA-szint - 10-20 ng/ml; Gleason-skála - több mint 4 + 3 - 7; biopsziában - 50%-nál nagyobb károsodás, perineurális invázió;
- nagyon magas: T4 stádium ; PSA-szint 20 ng/ml felett; Gleason-pontszám 8 felett; a biopszia nyirokavaszkuláris inváziót mutat.
Miután a diagnózist tisztázták és megállapították a folyamat kiterjedését (lokalizált, lokálisan előrehaladott vagy generalizált), az orvos és a beteg a kezelési módszer kiválasztásával szembesül. A modern társadalomban nagy jelentőséget tulajdonítanak a betegek életminőségének a kezelés megkezdése után. A kezelés nélküli életminőség megfelel az alapbetegség lefolyásának, és az onkológiai folyamat progressziójától függ. Az életminőség változásai főként a kezelés megkezdése és a terápiás vagy sebészeti módszerek valamelyikének alkalmazása után következnek be. A folyamat stádiumának egyértelmű megállapítása nemcsak az optimális kezelési módszer kiválasztását teszi lehetővé, hanem a betegség további lefolyásának előrejelzését is.
A PSA-szint meghatározása a prosztatarák klinikai képével és a daganat Gleason-skála szerinti fokozatosságával kombinálva jelentősen növeli a felsorolt indikátorok mindegyikének információtartalmát a rák kóros stádiumának megállapításában. AV Partin és munkatársai (1997) prognosztikai táblázatokat javasoltak, amelyek lehetővé teszik a daganat további terjedésének előrejelzését, a kezelési módszer megválasztását, a radikalitás mértékét és a kezelés hatékonyságának prognózisát.
A daganat terjedésének felmérésére a leggyakrabban használt módszerek a DRE, a TRUS, a PSA-szint meghatározása és a csontszcintigráfia. Szükség esetén komputertomográfiát (CT) vagy mágneses rezonancia képalkotást (MRI) és mellkasröntgent is felírnak.
Bármelyik képalkotó módszer célja a stádium meghatározása és a kezelés hatékonyságának felmérése. A diagnózis ellenőrzése után az urológusnak tisztáznia kell az elsődleges daganat térfogatát, határait, a daganat invazív vagy metasztatikus potenciálját. Mindezek a mutatók nagy jelentőséggel bírnak a betegség prognózisa és a kezelési módszer kiválasztása szempontjából.
Elsődleges tumor (T)
Először is meg kell állapítani, hogy a daganat a prosztatára korlátozódik-e (T 1-2 ), vagy túlnyúlik-e a tokon (T 3-4 ). A digitális vizsgálat gyakran nem teszi lehetővé a daganat terjedésének felmérését. Egyes adatok szerint a DRE eredményei a betegek kevesebb mint 50%-ánál felelnek meg a szövettani vizsgálat eredményeinek. Részletesebb vizsgálat azonban csak a radikális kezelés eldöntésekor indokolt.
A PSA-szint tükrözheti a daganat kiterjedését, de nem teszi lehetővé a morfológiai stádium pontos meghatározását. A PSA-szint, a Gleason-index és a tapintási adatok kombinációja lehetővé teszi a morfológiai stádium jobb előrejelzését, mint ezen paraméterek külön-külön történő meghatározása. A szabad PSA értéke vitatott: egy tanulmányban a szabad PSA-tartalom meghatározása segített tisztázni a lokalizált daganatok stádiumát, de más tanulmányok ezt nem erősítették meg. Csak mélyreható vizsgálatok segíthetnek a kérdés megoldásában.
A transzrektális ultrahangot leggyakrabban a prosztata állapotának vizsgálatára használják. Ez a módszer a daganatok csak 60%-át képes kimutatni, és nem mindig mutatja ki a tok invázióját. A T3 stádiumú betegek közel 60%-a ... Az ultrahang egy kevésbé gyakori folyamatot jelez. A tok inváziójának ultrahangjelei a mirigy kontúrjának kidudorodása, egyenetlensége és repedése. A tumorsejtek inváziója az ondóhólyagokba rossz prognosztikai jel, de az erről szóló információk rendkívül fontosak a kezelési módszer kiválasztásához. A TRUS elvégzésekor figyelmet kell fordítani a hólyagok echostruktúrájára (hiperechogenitás), aszimmetriájukra, deformációjukra és tágulásukra. Az ondóhólyagok károsodását a mirigy tövében lévő kerekdedség és tömörödés elvesztése is jelzi. Ezek a jelek meglehetősen szubjektívek, ezért nem helyénvaló teljes mértékben az ultrahangadatokra hagyatkozni. Az ondóhólyagok inváziója a lokális kiújulás és áttétek magas kockázatát jelzi, és biopsziájuk a tisztázás érdekében (műtét előtt) javallt. A vizsgálatot nem szabad ezzel az eljárással kezdeni, de ha az invázió kockázata magas, és a kezelés megválasztása a biopszia eredményétől függ, akkor annak alkalmazása indokolt. A negatív eredmény nem zárja ki a mikroszkopikus inváziót. Általában a T2b és magasabb klinikai stádiumokban, és a PSA-tartalom meghaladja a 10 ng/ml-t, ondóhólyag biopsziát végzik. Az eredményt pozitívnak tekintik, ha legalább egy, a prosztata bázisáról vett biopszia tumorsejteket tartalmaz. Nemcsak a további vizsgálatok, hanem az elsődleges biopszia eredményeinek alapos elemzése is lehetővé teszi a stádium klinikai meghatározásának pontosságának növelését (a tumorgócok száma és kiterjedése, valamint a tok inváziója szerepet játszik). A differenciálódás mértéke is fontos: 6-nál kisebb Gleason-index esetén a tumor az esetek 70%-ában lokalizálódik.
A prosztatarákban a véráramlás nagyobb, mint egy normál mirigyben vagy hiperpláziában. A kasztráció után a mirigyben a véráramlás intenzitása csökken. Az echo-dopplerográfiai térképek fejlesztése a prosztatarák diagnosztizálására és monitorozására ígéretes, de jelenleg nincsenek megbízható adatok az echo-dopplerográfia alkalmazásáról a lokális folyamat stádiumának meghatározásában. Ezzel a módszerrel további anyagot lehet nyerni a célzott biopszia során a kóros vaszkularizáció gócaiból.
A prosztatarák vizualizációjának eredményei közvetlenül függenek a klinika technikai felszereltségétől és a szakember tapasztalatától. Ezért minden modern vizualizációs módszer nem meghatározó, hanem tisztázó szerepet játszik, és a kezelési módszer kiválasztása a klinikai vizsgálati adatok és a műszeres vizsgálatok kombinációján alapul.
Az MRI rendelkezik a legjobb képességekkel a prosztata szerkezetének vizualizálására. A kismedencei szervek MRI-módszerrel történő vizsgálatának modern szabványa az endorektális érzékelő használata, amely lehetővé teszi a lehető legnagyobb, 0,5-1 mm-es térbeli felbontású kép előállítását. A levegő endorektális érzékelőbe történő bejuttatása biztosítja a prosztata tok, a rectoprostaticus szögek és a Denonvilliers-féle rectoprostaticus fascia tiszta vizualizációját. Az endorektális érzékelő használata MRI-ben nem korlátozza a regionális nyirokcsomók (a hasi aorta elágazásának szintjéig) vizualizációját. A prosztatarákot alacsony jelintenzitás jellemzi a T-súlyozott képeken, a mirigy változatlan perifériás zónájából származó nagy intenzitású jel hátterében. A szabálytalan forma, a diffúz terjedés tömeghatással, a homályos és egyenetlen kontúrok a prosztata perifériás zónájában található alacsony jelintenzitású gócok morfológiai jellemzői, ami az elváltozás neoplasztikus jellegére utal. Dinamikus kontrasztanyag alkalmazásakor a rákos gócok gyorsan felhalmozzák a kontrasztanyagot az artériás fázisban, és gyorsan eltávolítják azt, ami tükrözi az angiogenezis mértékét, és ennek megfelelően a daganat rosszindulatúságának mértékét. Az alacsony jelintenzitás jellemző a biopszia utáni vérzések gócaira, a prosztatagyulladásra, a mirigy semleges zónájának stromális jóindulatú hiperpláziájára, a rostos-heges elváltozásokra, a fibromuszkuláris hiperpláziára, valamint a hormon- vagy sugárterápia következményeire. A dinamikus kontrasztanyag nélküli MRI nem teszi lehetővé a felsorolt változások és betegségek többségének megbízható differenciálását.
Amint azt fentebb említettük, a prosztatarák képalkotó módszereinek egyik fő feladata a mirigylézió térfogatának és a daganat tokon túli terjedésének meghatározása. A daganat térfogatának meghatározása fontos a prognózis szempontjából. A 4 cm3-nél kisebb daganattérfogat távoli áttéteket jelez, a 12 cm3 pedig rendkívül magas áttétvalószínűséget. Kutatások szerint az MRI pontossága a prosztatarák neoplasztikus elváltozásainak gócainak kimutatásában 50-90% között mozog. Az MRI érzékenysége a prosztatarák lokalizációjának meghatározásában körülbelül 70-80%, míg a rákos mikroszkopikus gócok (gócok) MRI-vel nem mutathatók ki.
Az endorektális MRI legfontosabb előnye, hogy képes lokalizálni a neoplasztikus elváltozásokat olyan területeken, amelyek más diagnosztikai módszerekkel nem hozzáférhetők, valamint tisztázni a tumor növekedésének jellegét és irányát. Például az MRI lehetővé teszi a prosztata perifériás zónájának elülső részein található neoplasztikus elváltozások kimutatását, amelyek transzrektális biopsziával nem hozzáférhetők. Általánosságban elmondható, hogy az MRI jelentősen kiegészíti a DRE és a TRUS adatait a tumor lokalizációjáról.
Az endorektális MRI lehetővé teszi a mirigytok, az ér-ideg kötegek, az ondóhólyagok, a mirigycsúcs, a periprosztatikus vénás fonat vizualizálását, valamint a mirigytumor lokális prevalenciájának meghatározását. Hangsúlyozni kell, hogy a tok penetrációja mikroszkopikus jelnek tekinthető, és még a modern MRI-készülékek (endorektális tekercs) sem képesek ilyen információt szolgáltatni. Csak a mirigytokot meghaladó növekedésről lehet adatokat nyerni.
Az extrakapszuláris kiterjesztés diagnosztikai kritériumai MRI segítségével:
- extrakapszuláris tumor jelenléte;
- a mirigy egyenetlen kontúrja (deformáció, szögletesség);
- a neurovaszkuláris kötegek aszimmetriája;
- a rectoprostatikus szögek elzáródása;
- a daganat széles érintkezése a kapszulával.
Az MRI-eredmények legmagasabb specificitását (akár 95-98%-át) és pontosságát közepes vagy magas extrakapszuláris invázió kockázatú betegek vizsgálatakor érik el. Úgy vélik, hogy az extrakapszuláris invázió (az MRI-adatok szerint) a sebészeti kezelés helytelenségére és a betegség kedvezőtlen prognózisára utal. A hormonális vagy sugárterápia nem befolyásolja a prosztatarák extrakapszuláris terjedésének kimutatásának pontosságát. A rákos gócok és a daganat extrakapszuláris terjedésének kimutatásának fő nehézsége a tomogramok értelmezésének nagyfokú változékonysága a különböző szakemberek között. A sugárdiagnosztikai szakember elsődleges feladata a magas diagnosztikai specificitás elérése (akár az érzékenység rovására is), hogy ne fossza meg a műthető betegeket a radikális kezelés lehetőségétől.
A rákos, hiperplasztikus és normál prosztataszövet sűrűségének hasonlósága a CT-vizsgálatban kevéssé teszi ezt a módszert a daganat lokális terjedésének felmérésére. Az ondóhólyagokba való bejutás fontosabb, mint a tokokba való bejutás, de még ebben az esetben is a CT csak előrehaladott esetekben ad információt. Ezt a módszert azonban aktívan alkalmazzák a sugárterápia előtti támadáspont kijelölésére.
Hazánkban a sugárdiagnosztika lassú fejlődése a prosztatarák késői diagnosztizálásához, és ennek következtében a prosztatarák radikális kezelési módszereinek (például prosztatektómia) elégtelen elterjedtségéhez, a modern tomográfok alacsony elérhetőségéhez, valamint a sugárdiagnosztikai szakemberek és urológusok megfelelő képzési programjainak hiányához vezetett. Annak ellenére, hogy a CT és az MRI ma már széles körben elterjedt, a rendelők felszereltsége és a sugárdiagnosztikai szakemberek képzettsége nem elegendő ahhoz, hogy a kapott információk döntő fontosságúak legyenek a prosztatarákos betegek kezelési módjának kiválasztásában.
Regionális nyirokcsomók (N)
A regionális nyirokcsomókat csak akkor kell vizsgálni, ha ez közvetlenül befolyásolja a kezelési stratégiát (általában radikális kezelés tervezésekor). A magas PSA-szint, a T2c -T3a tumorok, a rossz differenciálódási stádium és a perineurális invázió a nyirokcsomó-áttétek magas kockázatával jár. A nyirokcsomók állapotának PSA-szinten alapuló felmérése nem tekinthető elégségesnek.
Csak a nyirokcsomó-eltávolítás (nyílt vagy laparoszkópos) biztosítja a szükséges információkat. A kiterjesztett nyirokcsomó-eltávolítással kapcsolatos legújabb tanulmányok kimutatták, hogy a prosztatarák nem mindig érinti az elzáró nyirokcsomókat. Tünetmentes daganatok és 20 kg/ml alatti PSA-szint esetén a CT csak az esetek 1%-ában igazolja a megnagyobbodott nyirokcsomókat. Az MRI vagy CT alkalmazása magas áttétveszély esetén indokolt, mivel ezeknek a módszereknek a specificitása eléri a 93-96%-ot. Azonban még a pozitív eredmény is hamis lehet alkalmazásuk során, és csak egy gyanús nyirokcsomó szúrása teszi lehetővé a nyirokcsomó-eltávolítás elutasítását. Retrospektív elemzés szerint a nyirokcsomó mérete nem mindig jelzi az áttétek jelenlétét benne; az érintett nyirokcsomók aszimmetriája informatívabb jelnek tekinthető. Jelenleg a lokalizált prosztatarák miatt radikális prosztatektómián átesett betegeknek csak 2-3%-ánál diagnosztizálnak áttétet a nyirokcsomókban a posztoperatív szövettani vizsgálat alapján.
A nyirokcsomók áttéteinek kimutatására a pozitronemissziós tomográfia (PET) és a jelzett antitestekkel végzett szcintigráfia ajánlott, de alkalmazásuk még mindig korlátozott az elégtelen érzékenység miatt.
Partin nomogramjai (2001) felhasználhatók a regionális nyirokcsomó-érintettség kockázatának felmérésére. A nomogramok matematikai algoritmusok, amelyeket egy adott beteg vagy betegcsoport esetében alkalmaznak. Ezek a táblázatok lehetővé teszik a lokális daganat terjedésének (a tokba, az ondóhólyagokba) és a nyirokcsomó-érintettség valószínűségének meghatározását a klinikai stádium, a PSA-szint és a Gleason-index alapján. Különösen lehetővé teszik azon betegek csoportjának azonosítását, akiknél alacsony (kevesebb, mint 10%) a nyirokcsomó-áttét valószínűsége (20 ng/md feletti PSA-szint, T1-2a stádium és 2-6 Gleason-index); ebben a csoportban a nyirokcsomók állapota a radikális kezelés előtt nem határozható meg. A nyirokcsomó-áttét kockázata a kifejezett anapláziával (4-5 pont) rendelkező daganatos területek kimutatásával is felmérhető: ha ilyen területeket találnak négy vagy több biopsziában, vagy legalább egy biopsziában dominálnak, a kockázat eléri a 20-45%-ot. Más betegeknél nem haladja meg a 2,5%-ot. Ilyen esetekben további vizsgálat nem szükséges.
Távoli áttétek (M)
A prosztatarákban elhunyt betegek 85%-ánál a tengelyirányú váz elváltozásait észlelik. A csontáttétek a rákos sejtek vérárammal történő csontvelőbe jutása miatt alakulnak ki, ami tumornövekedéshez és a csontszerkezetek líziséhez vezet. A csontáttétek előfordulása befolyásolja a prognózist, és korai felismerésük figyelmezteti az orvost a lehetséges szövődményekre. Az esetek 70%-ában az áttétek az alkalikus foszfatáz (ALP) csontizoenzim aktivitásának növekedésével járnak. Az ALP aktivitásának és a PSA-szintnek a meghatározása az esetek túlnyomó többségében lehetővé teszi a csontáttétek kimutatását. A többváltozós elemzés szerint ezeket a mutatókat csak a csontáttétek száma befolyásolja. Fontos, hogy az ALP csontizoenzim aktivitása pontosabban tükrözze a csontkárosodás mértékét, mint a PSA-szint.
A szcintigráfiát tartják a csontáttétek kimutatásának legérzékenyebb módszerének (felsőbb a radiográfiánál és az alkalikus és savas foszfatáz aktivitás meghatározásánál). A technécium-difoszfonátok jobban alkalmazhatók radiofarmakonként, mivel a csontokban való felhalmozódásuk sokkal aktívabb, mint a lágy szövetekben. Összefüggést mutattak ki a csontkárosodás szemikvantitatív értékelése és a túlélés között. A távoli áttétek kimutatása bármely szervben lehetséges. Leggyakrabban nem regionális nyirokcsomókban, tüdőben, májban, agyban és bőrben fordulnak elő. Megfelelő panaszok és tünetek esetén mellkasröntgen, ultrahang, CT és MRI alkalmazható a kimutatásukra. A feltételezett csontáttétek taktikáját az ábra mutatja.
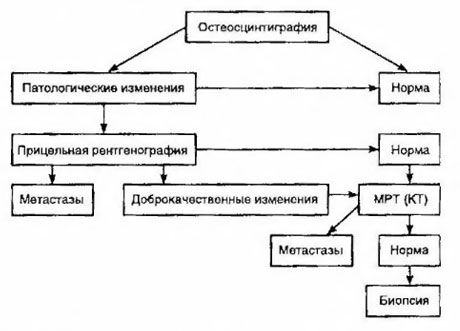
A metasztázis mértékének meghatározásában segítő legmegbízhatóbb laboratóriumi mutató a PSA-szint. Kimutatták, hogy 100 ng/ml feletti növekedése az egyetlen paraméter, amely megbízhatóan jelzi a távoli áttéteket. A PSA-szint meghatározása csökkenti a csontszcintigráfiára szoruló betegek számát. A PSA-szint csökkenésével a csontáttétek kimutatásának valószínűsége nagyon alacsony. Panaszok hiányában és 20 ng/ml alatti kezdeti PSA-tartalom esetén a magas és közepesen differenciált tumorok kimutatása elkerülhető. Ugyanakkor rosszul differenciált tumorok és tok invázió esetén a szcintigráfia javallt (függetlenül a PSA-szinttől).


 [
[